La pathologie hémorroïdaire est un motif fréquent de consultation. La prise en charge ne se limite pas à l’application d’une crème ou à une opération chirurgicale ; elle est fonction des symptômes, et est de plus en plus personnalisée. Quels sont les traitements de la crise ? Quelle prévention ? Quelles nouveautés ? Quelles particularités chez la femme enceinte ?
Les hémorroïdes sont des formations vasculaires normales de l’anus. En position physiologique, elles participent à la continence anale fine (discrimination selles/gaz et solide/liquide) et représentent 20 % du tonus de repos du canal anal. La pathogénie de la maladie hémorroïdaire n’est pas totalement comprise : elle fait intervenir des facteurs vasculaires (hyperplasie vasculaire responsable d’une distension des plexus) et mécaniques (destruction du tissu conjonctif et musculaire générant une hyperlaxité du tissu de soutien et un déséquilibre des flux vasculaires).
Les symptômes ne sont pas spécifiques : prolapsus, douleurs ou prurit. Ainsi, pour poser le diagnostic, un examen proctologique est nécessaire (à réaliser en décubitus latéral gauche ou mieux en position génupectorale) : inspection de la marge anale avec déplissement des plis radiés (lésion dermatologique, fissure anale, collection, tumeur ?), toucher anal puis rectal après en avoir informé le patient (collection, masse suspecte du canal anal ou du bas rectum ?), et anuscopie pour visualiser les plexus hémorroïdaires.
Hémorroïdes internes
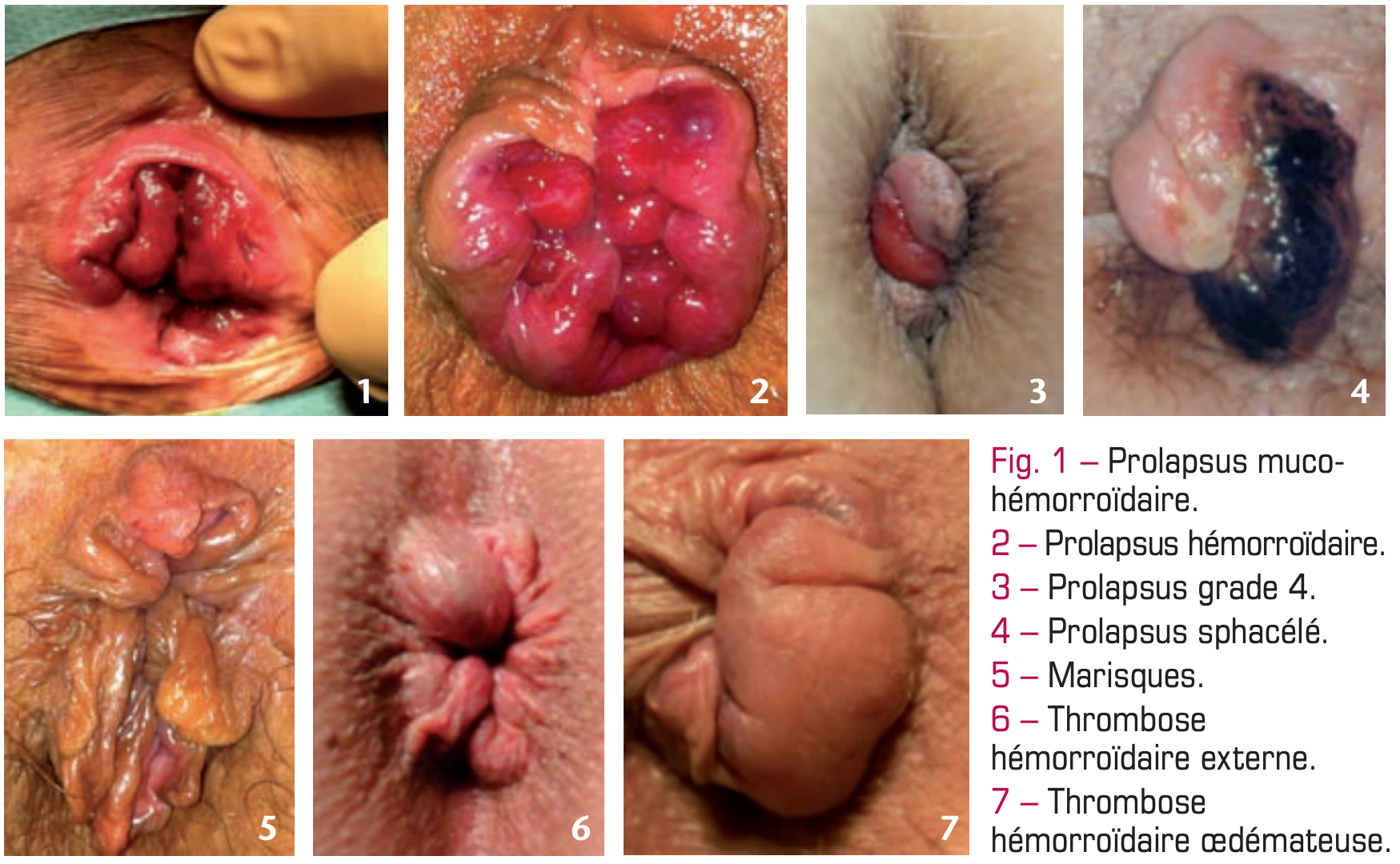
Les rectorragies sont indolores : il s’agit de sang rouge rutilant éclaboussant la cuvette lors du passage des selles. Elles sont parfois plus abondantes, déclenchées par l’émission de gaz ou la position accroupie (souillant alors les sous-vêtements). En fonction de leur quantité – favorisée par la prise d’anticoagulants ou d’antiagrégants – et de leur ancienneté, elles peuvent être responsables d’une anémie ferriprive. Le prolapsus correspond à l’extériorisation des plexus hémorroïdaires internes par l’orifice anal. Il peut concerner un ou plusieurs paquets hémorroïdaires (fig. 1), être circulaire (fig. 2) ou accompagné d’une procidence de la muqueuse du bas rectum (muco-hémorroïdaire). Chez la femme, il s’agit souvent du paquet antéro-droit (fig. 3). La procidence apparaît à la défécation ou à l’effort, avec une réintégration spontanée ou manuelle. Elle peut être permanente, responsable alors de suintements séro-sanglants, voire de souillures fécales entraînant un prurit. Une sensation de gonflement, de pesanteur intracanalaire est parfois décrite, en rapport avec une congestion des plexus hémorroïdaires. Ces « crises » peuvent notamment survenir en période prémenstruelle.
Les thromboses hémorroïdaires, si non extériorisées, provoquent une douleur intracanalaire permanente ; le toucher anal retrouve une masse arrondie douloureuse en « grain de plomb » (bleutée en anuscopie). Elles sont le plus souvent extériorisées, localisées ou circulaires avec un prolapsus irréductible extrêmement douloureux. S’y associe un œdème réactionnel avec une coloration violacée voire noirâtre (fig. 4). Elles peuvent évoluer vers le sphacèle ou régresser, laissant comme séquelle un repli cutané : la marisque (fig. 5).
Hémorroïdes externes
La seule manifestation est la thrombose hémorroïdaire externe (un ou plusieurs caillots), soit une tuméfaction bleutée, dure, souvent – mais pas toujours – douloureuse, sous la peau de la marge anale (fig. 6). Elle peut être associée à un œdème parfois important, allant jusqu’à masquer le thrombus (fig. 7). L’évolution spontanée se fait en quelques semaines vers son énucléation (accompagnée de saignements minimes) ou sa résorption, avec des marisques résiduelles. Ces dernières sont parfois volumineuses, gênant l’essuyage, responsables d’un prurit et de gonflements prémenstruels.
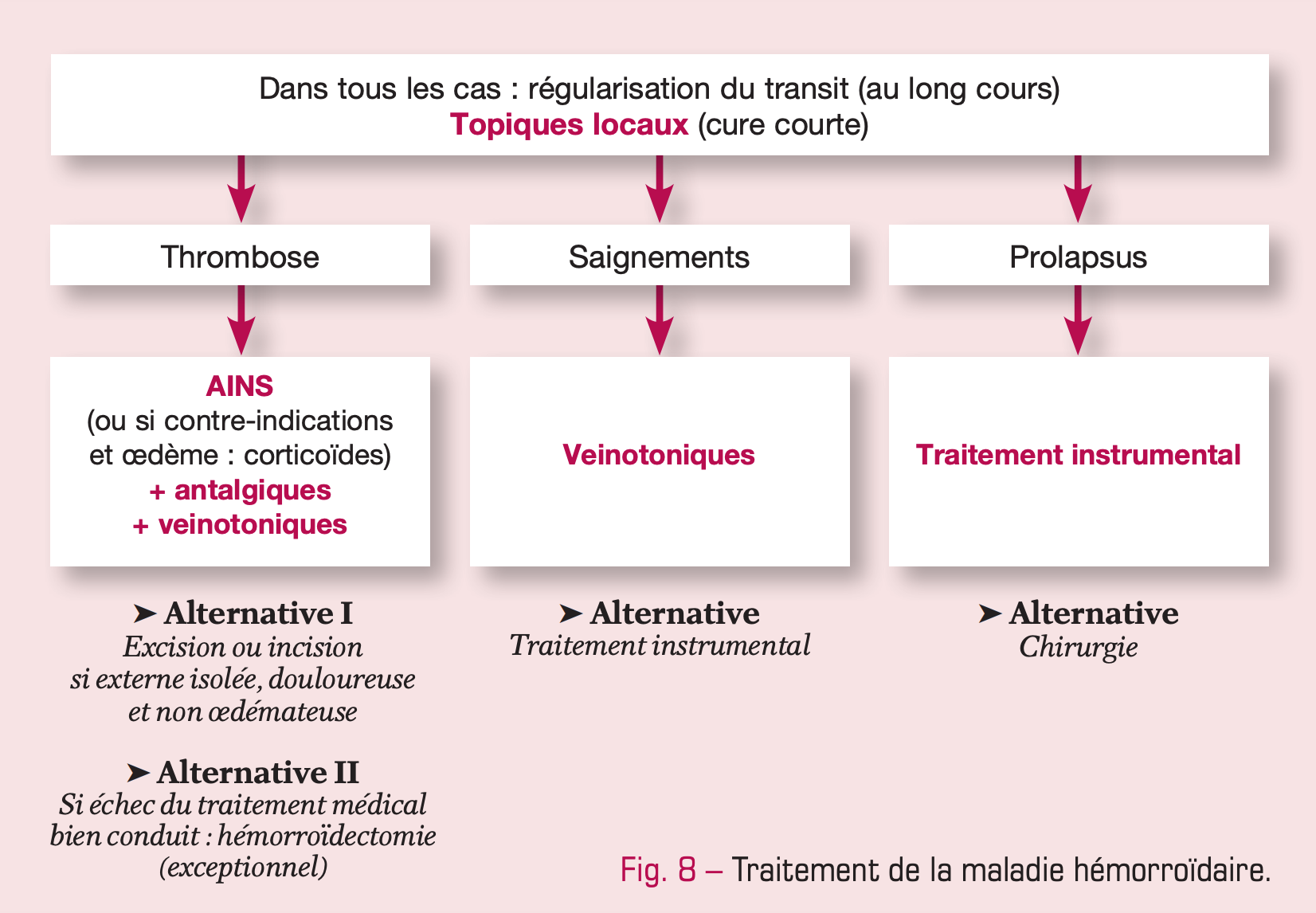
Quels traitements ? (fig. 8)
Le traitement médical doit toujours être proposé en première intention, pendant 7 à 21 jours – ce qui peut être suffisant pour les manifestations aiguës (fig. 2).
Plusieurs topiques sont disponibles, en suppositoires, crèmes ou pommades. L’efficacité à court terme est de 90 %, sans bénéfice au long cours ni action préventive démontrée.
Il n’y a pas d’étude étayant clairement l’intérêt des corticoïdes locaux, anesthésique, phlébotrope, lubrifiant et/ou protecteur mécanique. Il semble utile de prescrire des produits cortisonés en cas d’œdème ou d’inflammation (thrombose hémorroïdaire), Ultraproct par exemple, et ceux avec anesthésique si douleur (Tronothane).
La régularisation du transit est recommandée en curatif et en préventif. On préconise un apport suffisant en fibres alimentaires parfois aidé par un ajout de mucilages, de laxatifs osmotiques ou de freinateurs du transit, selon le trouble. C’est la seule mesure préventive au long cours ayant une efficacité démontrée. La constipation étant le plus fréquemment en cause, son traitement est une priorité. Diminuer le nombre d’évacuations irritantes en cas de diarrhées semble tout aussi important.
Les phlébotropes (diosmine, troxérutine, dérivés du Ginkgo biloba, hydroxyéthylrutoside), qui visent la composante vasculaire, auraient un effet sur le prurit, les rectorragies et le suintement, selon deux méta-analyses. Ils sont recommandés lors des manifestations aiguës (excepté le prolapsus) à court terme.
Les AINS agissent sur la douleur et l’inflammation ; les antalgiques périphériques et centraux (éventuellement associés aux AINS) peuvent être prescrits en cas de douleur insuffisamment contrôlée et les corticoïdes per os chez les patients ayant une thrombose externe œdémateuse si les AINS sont contre-indiqués.
En pratique, malgré l’absence de données publiées, la coprescription est fréquente. Devant une thrombose hémorroïdaire (interne ou externe), on propose d’associer AINS, antalgiques, régulateurs du transit et topiques. Pour une pathologie hémorroïdaire interne, on préfère des régulateurs du transit et des topiques ; les phlébotropes sont autorisés.
En en 2e ligne ?
En cas d’échec du traitement médical, on peut proposer des méthodes instrumentales, utilisant un procédé chimique (injections sclérosantes), physique (photocoagulation infrarouge, cryothérapie) ou mécanique (ligature élastique). Elles sont contre-indiquées en cas de maladie inflammatoire intestinale active et suppuration anopérinéale et, en ce qui concerne les ligatures élastiques et les injections sclérosantes, chez la femme enceinte et l’immunodéprimé sévère.
La chirurgie est indiquée en cas d’échec du traitement médical et/ou instrumental ou d’emblée pour les prolapsus évolués. La technique classique – l’hémorroïdectomie tripédiculaire – a certes fait ses preuves avec peu de complications, mais les suites opératoires sont douloureuses, avec des soins locaux pluriquotidiens et un arrêt d’activité prolongé (2 à 3 semaines). Aujourd’hui, de méthodes modernes dites « mini-invasives », en développement depuis une vingtaine d’années, ont modifié la prise en charge. Parmi celles-ci, la ligature des artères hémorroïdaires sous contrôle doppler (DGHAL) + mucopexie et la radio fréquence sont préférées, aujourd’hui, à l’anopexie circulaire (risque de complications).
Quels traitements autorisés chez la femme enceinte ?
La pathologie hémorroïdaire est fréquente chez la parturiente, ce sont essentiellement des thromboses hémorroïdaires externes souvent œdémateuses relevant en général d’un traitement médical. Seule la régulation du transit peut diminuer le risque de poussée. Les topiques, le paracétamol, les laxatifs et les phlébotropes sont autorisés. Il est fortement recommandé – pour les AINS, les corticoïdes et les antalgiques – de se référer aux données actualisées du Centre de référence sur les agents tératogènes (CRAT). Il est préférable d’éviter tout geste local ou chirurgical pendant cette période.
Cinzia Nobile, La Revue du Praticien
D’après :
Higuero T. Pathologie hémorroïdaire.Rev Prat Med Gen 2017;31(990):784-5.
Higuero T. Traitement de la maladie hémorroïdaire : de nouvelles recommandations.Rev Prat 2017;67(10);1059-62.
À lire aussi :
Fathallah N, De Parades V. Hémorroïdes internes, traitements modernes.Rev Prat Med Gen 2019;33(1026);627-8.