L’incidence des tumeurs pancréatiques – et surtout de l’adénocarcinome – est en augmentation. Il est important d’en connaître les manifestations cliniques, dont le type et la chronologie dépendent du site de la tumeur primitive et de son stade au diagnostic. L’essentiel pour le MG.
Adénocarcinome, la plus fréquente des tumeurs solides pancréatiques
Il s’agit d’une tumeur développée à partir des cellules épithéliales des canaux pancréatiques. Son incidence est en augmentation : en France, environ 15 000 nouveaux cas sont diagnostiqués tous les ans, dont 54 % chez des hommes. L’incidence annuelle est de 9 à 10 pour 100 000 habitants.
L’âge moyen au diagnostic est de 73 ans chez la femme et de 68 ans chez l’homme. L’adénocarcinome est rapidement évolutif, avec une extension locale et métastatique par voies lymphatique, nerveuse et sanguine.
Le taux de mortalité est proche de celui de l’incidence, traduisant son mauvais pronostic, lié au diagnostic souvent tardif, avec des premiers symptômes parfois aspécifiques. La survie cumulée à 5 ans tous stades confondus ne dépasse pas 5 %.
Les facteurs de risque sont de mieux en mieux connus. Certains facteurs génétiques ont été identifiés. Des formes familiales de cancer (comme le syndrome seins-ovaires ou le syndrome de Lynch) peuvent prédisposer (patients porteurs de mutations de BRCA1, BRCA2, PALB2, CDKN2A ou du gène MMR). Le syndrome de Peutz-Jeghers (affection rare à l’origine d’une polypose hamartomateuse intestinale) est aussi un facteur de risque (mutation du gène LKB1/STK11). Enfin, il existe des formes familiales avec deux ou trois cas d’adénocarcinomes du pancréas chez des apparentés au premier ou deuxième degré pour lesquelles le gène en cause n’est pas connu. La plupart de ces formes génétiques doivent bénéficier d’un dépistage par examens radiologiques annuels.
L’obésité, avec un risque relatif à 2,76, et le diabète, avec un risque relatif à 1,94 (diabète ancien), sont les deux principaux facteurs de risque endogènes non génétiques.
Le rôle du tabac est bien établi (risque relatif [RR] : 1,6-2,6). Il l’est moins pour une alimentation riche en protéines et en graisses animales, une activité physique réduite, la consommation d’alcool, de café, l’exposition aux métaux lourds (RR : 1,1-1,5).
Il existe également des tumeurs kystiques à potentiel dégénératif (cf. ci-dessous).
Enfin, les affections pancréatiques chroniques prédisposant à l’adénocarcinome sont la pancréatite chronique calcifiante alcoolique et la pancréatite chronique héréditaire.
Quels signes cliniques ?
Les symptômes varient en fonction de la localisation de la tumeur et de son degré d’évolution. Il existe une phase préclinique souvent muette et parfois longue, expliquant un diagnostic tardif.
• L’ictère est le signe essentiel du cancer de la tête du pancréas (70 à 80 % des cas). Il est cholestatique (selles décolorées « mastic », urines foncées « bière brune », prurit qui précède parfois l’apparition de l’ictère). Il se caractérise par son installation insidieuse, avec une évolution continue, sans rémission et sans crise douloureuse ou épisode hyperthermique (on parle « d’ictère nu »). Il peut s’accompagner de troubles digestifs (dyspepsie et constipation fréquentes), anorexie, stéatorrhée et amaigrissement. On peut palper une masse oblongue indolore, correspondant à une grosse vésicule, au niveau de l’hypochondre droit.
• Le syndrome douloureux abdominal est classiquement l’apanage des localisations corporéales et caudales (20 à 30 % des cas). Il est de siège sus-ombilical à irradiation transfixiante vers l’arrière. Les crises douloureuses, d’abord peu intenses, s’accentuent rapidement pour aboutir à des paroxysmes extrêmement intenses, interdisant le décubitus dorsal et imposant souvent des attitudes antalgiques (antéflexion du tronc, attitude en chien de fusil, compression de la région sus-ombilicale). Cette douleur nécessite rapidement un antalgique de palier 3. Cependant, cette symptomatologie douloureuse n’est pas toujours aussi évocatrice et peut simuler pendant plusieurs semaines ou mois une colopathie fonctionnelle, un syndrome dyspeptique ou une affection rhumatismale (dorsalgies).
• La triade amaigrissement, asthénie et anorexie est constante en phase avancée, mais peut aussi apparaître précocement et précéder les autres symptômes.
• Le diabète est présent dans 50 % des cas, souvent récent (quelques mois), alors causé par le cancer lui-même.
• D’autres manifestations cliniques représentent entre 10 et 20 % des circonstances de diagnostic mais peuvent aussi accompagner ou précéder les autres symptômes : amaigrissement isolé, diarrhée chronique ou stéatorrhée, syndrome tumoral abdominal isolé, hémorragie digestive, thrombophlébite profonde et/ou embolie pulmonaire, syndrome anxiodépressif.
Attention : en cas de pancréatite aiguë dite « a priori idiopathique » (pancréatite sans cause évidente [pas de lithiase biliaire, pas d’alcool] lors la poussée aiguë mais nécessitant un bilan à distance par cholangiopancréatographie-IRM et écho-endoscopie bilio-pancréatique) chez un patient de plus de 50 ans, la recherche d’une tumeur pancréatique – en particulier un adénocarcinome – doit être systématique.
Diagnostic et prise en charge
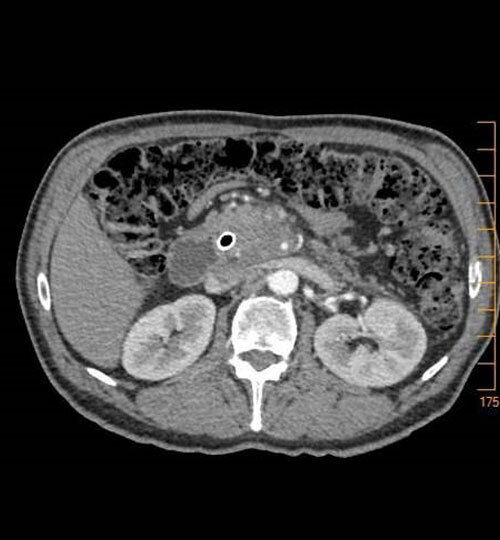
Les examens paracliniques sont hiérarchisés : d’abord, l’échographie, qui permet de détecter un syndrome tumoral mais aussi des signes indirects (dilatation des voies biliaires et/ou des voies pancréatiques). Elle précède l’examen-clé du diagnostic et du bilan d’extension, qui est le scanner thoraco-abdomino-pelvien avec injection de produit de contraste. L’obtention d’une histologie est nécessaire pour décider du traitement (écho-endoscopie avec cytoponction).
Le traitement curatif est chirurgical, mais il n’est malheureusement possible que dans 15 % des cas. Les tumeurs avec des métastases ou localement avancées non résécables relèvent d’une chimiothérapie, en essayant de préserver la qualité de la survie des patients.
Tumeurs neuroendocrines, 2e type de tumeurs solides pancréatiques
Ces tumeurs développées aux dépens des îlots endocrines du pancréas sont beaucoup plus rares, représentant 1 à 2 % des tumeurs malignes du pancréas. Elles se répartissent en deux catégories : les tumeurs non fonctionnelles (n’assurant aucune sécrétion) et les fonctionnelles pouvant sécréter des peptides hormonaux (insuline, gastrine ou glucagon).
Quels signes cliniques ?
Les tumeurs non fonctionnelles se manifestent sous forme d’un syndrome tumoral souvent par compression des organes de voisinage ou par des symptômes aspécifiques (ictère, douleur, amaigrissement, diabète…). Dans plus d’un tiers des cas, ils sont détectés de façon fortuite à l’imagerie (incidentalomes), à l’occasion d’un bilan digestif, urologique, vasculaire ou gynécologique. Ils sont habituellement résécables au moment du diagnostic, facteur de meilleur pronostic.
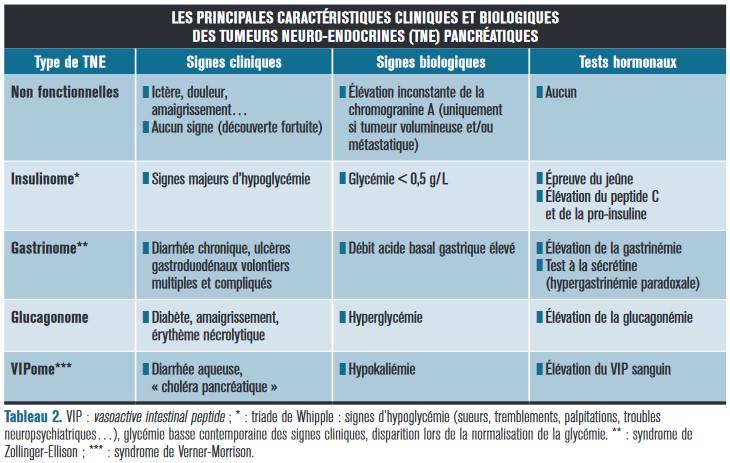
Les symptômes des tumeurs fonctionnelles dites sécrétantes varient en fonction de la sécrétion d’hormones ou peptides. Par ordre de fréquence, on peut distinguer l’insulinome, le gastrinome, le glucagonome et le VIPome.
Diagnostic et prise en charge
Elles sont classées en tumeurs de bas grade (de bon pronostic, sans métastases) ou de haut grade, dont le pronostic est beaucoup plus péjoratif. Les examens diagnostiques sont l’échographie, puis le scanner, l’IRM mais aussi l’imagerie isotopique à l’aide d’analogues stables de la somatostatine marqués à l’indium-111 ou au gallium-68.
Le traitement va de la simple surveillance pour les petites lésions de bas grade à la chirurgie curatrice. D’autres traitements peuvent être envisagés, visant à ralentir la croissance des tumeurs primaires et secondaires : analogues stables de la somatostatine, chimiothérapie, biothérapies, techniques de chimio-embolisation, radiothérapie interne vectorisée avec des analogues de la somatostatine marqués d’isotopes très énergétiques (lutécium).
Lésions kystiques pancréatiques
Il faut bien distinguer les pseudokystes (80 %) – lésions inflammatoires survenant après pancréatite aiguë et/ou pancréatite chronique – des tumeurs kystiques vraies (20 %). Ces dernières sont souvent de découverte fortuite, mais peuvent également occasionner des symptômes liés à la compression des organes de voisinage.
Il s’agit de tumeurs intracanalaires papillaires et mucineuses du pancréas qui peuvent toucher soit les canaux secondaires, soit le canal principal, soit les deux.
Leur pronostic est variable en fonction de la localisation.
La prise en charge de la plupart de ces lésions consiste en une surveillance, sauf s’il y a des signes de dégénérescence ou si elles atteignent le canal principal (chirurgie d’exérèse).
Le cystadénome mucineux est une tumeur pouvant également dégénérer. En fonction des symptômes et de sa taille, une chirurgie peut être proposée.
Enfin, les cystadénomes séreux ne dégénèrent jamais et peuvent parfois faire l’objet d’une simple surveillance.
D’après :
Buscail L. Item 308 – Tumeurs du pancréas.Rev Prat 2022 ;72(2) ;201-9.
Buscail L. Item 308 (focus) – Tumeurs du pancréas : un bilan diagnostique et thérapeutique hiérarchisé.Rev Prat 2022;72(2);210.
Cinzia Nobile, La Revue du Praticien