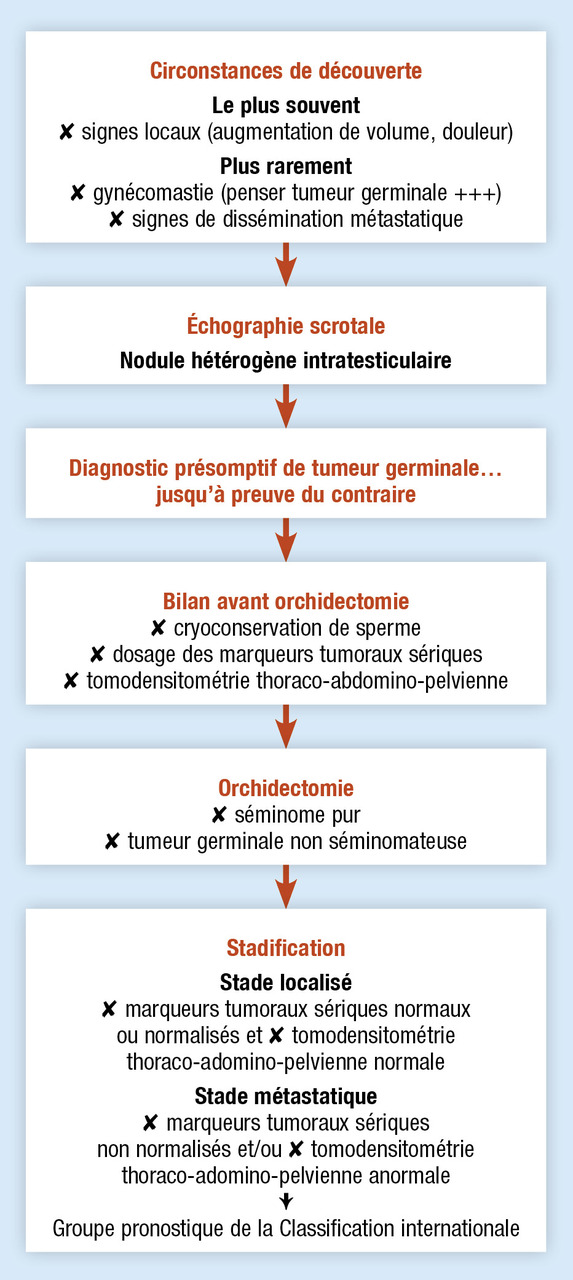
Éléments cliniques et de diagnostic d’une tumeur du testicule.
« Toute tumeur du testicule est un cancer jusqu’à preuve du contraire »… ce vieil adage transmis de génération en génération d’étudiants demeure d’actualité en 2022. La démarche diagnostique des tumeurs du testicule doit être parfaitement conduite (fig. 1) dans la mesure où la prise en charge thérapeutique qui en découle a pour objectif la guérison du patient et que tout écart risque de la compromettre !
Anatomopathologie (rang A)
La très grande majorité des tumeurs du testicule de l’adulte correspond à des tumeurs germinales (
Les tumeurs germinales malignes de l’adulte jeune dérivent des gonocytes primordiaux, précurseurs embryonnaires des gamètes de l’adulte. Du point de vue de la prise en charge thérapeutique, il est important de distinguer les séminomes purs, d’une part, et les tumeurs non séminomateuses, d’autre part. Une tumeur non séminomateuse peut contenir des cellules séminomateuses mais comporte obligatoirement une autre composante. Le terme de « néoplasie germinale intratubulaire indifférenciée » désigne la lésion précancéreuse commune aux tumeurs germinales malignes.
Les tumeurs spermatocytaires sont très rares et se développent à partir des spermatogonies. Elles sont considérées comme des tumeurs bénignes, sans potentiel métastatique.
Les tumeurs non germinales constituent un groupe de tumeurs très hétérogène, bénignes ou malignes, principale ment issues des tissus de soutien (stroma gonadique et cordons sexuels).
Tumeurs germinales malignes du testicule de l’adulte
Épidémiologie et facteurs de risque (rang B)
Elles représentent entre 1 et 1,5 % des cancers de l’homme. En constante augmentation au cours des dernières décennies, l’incidence française est d’environ 2 500 nouveaux cas par an, soit 5 pour 100 000 hommes. L’incidence est plus élevée dans les pays scandinaves, similaire en Amérique du Nord et nettement moindre en Afrique et en Asie. Les formes bilatérales représentent 1 à 2 % des cas. Il s’agit d’un cancer qui touche l’homme jeune, avec un pic de fréquence autour de la troisième décennie, et un second pic entre 40 et 50 ans pour les séminomes.
Les tumeurs germinales du testicule ont la particularité d’être associées à un très bon pronostic, avec une survie à cinq ans de plus de 95 % tous stades confondus, dès lors que la démarche diagnostique conduit à une prise en charge thérapeutique adaptée. Elles sont responsables de moins de 100 décès par an en France, ce qui correspond à un taux de mortalité de 0,2/100 000 hommes, en constante diminution.
Les facteurs de risque identifiés à ce jour sont les suivants :
- antécédents de cryptorchidie, le risque persistant après abaissement testiculaire ;
- antécédents familiaux du premier degré de cancer du testicule ;
- antécédent personnel de tumeur du testicule ou de néoplasie germinale intratubulaire controlatérale ;
- infertilité ;
- trisomie 21 ;
- consommation régulière et prolongée de cannabis pour les tumeurs non séminomateuses.
Modes de dissémination (rang A)
Leur connaissance permet de comprendre les différentes manifestations cliniques pouvant être rencontrées, ainsi que le bilan d’extension nécessaire. La voie lymphatique suit les pédicules vasculaires spermatiques, qui naissent directement de l’aorte lombaire et se jettent dans la veine cave inférieure à droite et la veine rénale à gauche, tandis que la voie hématogène est celle de la veine spermatique. Les premiers sites métastatiques atteints sont donc les ganglions rétropéritonéaux et les poumons.
Circonstances de découverte (rang A)
Classiquement, les tumeurs germinales du testicule sont diagnostiquées devant l’apparition de symptômes locaux : augmentation progressive du volume testiculaire, autopalpation d’une masse scrotale, douleurs. Elles peuvent se révéler également de manière plus aiguë, à l’occasion d’une orchite ou d’un traumatisme scrotal. Leur découverte fortuite lors d’une échographie réalisée dans le cadre d’un bilan (d’infertilité, par exemple) est aussi possible.
Plus rarement, le diagnostic est porté au cours du bilan d’une masse abdominale, d’une adénopathie de Troisier, d’une gynécomastie (en cas de sécrétion tumorale d’hormone chorionique gonadotrope), d’une altération de l’état général, ou encore d’une dyspnée dans les formes massivement métastatiques d’emblée.
Examen clinique (rang A)
La palpation scrotale doit être bilatérale et comparative. Elle met en évidence un nodule ou une masse développée aux dépens du testicule, de consistance dure et irrégulière, et indépendante de l’épididyme (avec persistancedu sillon épididymo-testiculaire, ou signe de Chevassu). L’examen clinique doit également comporter la palpation des aires ganglionnaires sus-claviculaires gauches et la palpation abdominale (à la recherche d’une hépatomégalie ou d’une masse abdominale), ainsi qu’un examen général (pleuropulmonaire…) à la recherche de signes d’une ou de plusieurs localisations métastatiques.
Échographie scrotale (rang A)
Elle doit être systématiquement réalisée et permet non seulement de confirmer l’origine testiculaire de la masse scrotale mais aussi d’explorer le testicule controlatéral. L’aspect échographique d’une tumeur germinale est volontiers celui d’un nodule hétérogène pouvant être hypervascularisé (
Diagnostics différentiels (rang B)
Le principal diagnostic différentiel est l’orchi-épididymite, qui se distingue par la présence de signes infectieux pouvant être marqués (fièvre, douleur), de troubles urinaires, d’un examen cytobactériologique des urines positif, et d’un signe de Chevassu négatif. En cas de doute, l’échographie testiculaire peut trancher en mettant en évidence un épaississement et un aspect hypervascularisé de l’épididyme. L’hydrocèle vaginale est facilement reconnaissable par son aspect régulier et de consistance hydrique. Les autres diagnostics différentiels peuvent facilement être éliminés cliniquement ou à l’échographie (kyste de l’épididyme, varicocèle, hernie inguino-scrotale…).
Marqueurs tumoraux sériques (rang A)
Les trois marqueurs d’intérêt sont l’alphafœtoprotéine (AFP), l’hormone chorionique gonadotrope (hCG) totale et la lactate déshydrogénase (LDH).
L’AFP n’est élevée qu’en cas de tumeur germinale non séminomateuse. Sa demi-vie est de cinq à six jours. Son élévation est également possible dans certaines pathologies hépatiques, bénignes ou malignes.
L’hCG totale peut être élevée en cas de tumeur germinale séminomateuse ou non séminomateuse. Sa demi-vie est de deux à trois jours.
La LDH n’a pas de spécificité d’organe ni d’histologie et reflète la masse tumorale.
Ces marqueurs ont un triple rôle diagnostique, pronostique et de suivi au cours de la prise en charge des tumeurs germinales du testicule. Avant l’orchidectomie, l’élévation de l’AFP et/ou de l’hCG confirme quasiment avant l’histologie le diagnostic de tumeur germinale. À tel point que leur élévation peut être suffisante pour engager un traitement avant l’orchidectomie si le tableau clinique le justifie (métastases menaçantes).
Au décours de l’orchidectomie, les marqueurs tumoraux sériques participent à la stadification de la maladie. Si la tomodensitométrie thoraco-abdomino-pelvienne est sans anomalies, la normalisation des marqueurs est nécessaire pour conclure au stade localisé de la maladie. Si la tomodensitométrie thoraco-abdomino-pelvienne montre des métastases, le niveau d’élévation des marqueurs permet d’adapter les traitements en fonction du pronostic de la maladie.
Bilan d’extension (rang B)
La tomodensitométrie thoraco-abdomino-pelvienne est l’examen d’imagerie de référence pour le bilan d’extension de la maladie. Les principales régions d’intérêt à la recherche d’une dissémination métastatique sont le rétropéritoine, le foie, le médiastin et les poumons. L’imagerie par tomographie d’émission de positons-fluorodésoxyglucose (TEP-FDG) n’a pas de place dans le bilan initial. L’imagerie cérébrale doit être réalisée en cas de signes de localisation neurologique ou de forme métastatique de mauvais pronostic. La scintigraphie osseuse n’est demandée qu’en cas de point d’appel clinique.
Orchidectomie (rang A)
Le diagnostic positif final d’une tumeur germinale du testicule repose sur l’analyse anatomopathologique de la pièce d’orchidectomie. Une tumeur testiculaire ne doit jamais être biopsiée : toute découverte d’une masse testiculaire est un cancer jusqu’à preuve anatomopathologique du contraire et doit conduire à la réalisation d’une exploration scrotale par voie inguinale. Celle-ci se fait sous anesthésie générale ou sous rachianesthésie, par voie inguinale, après clampage haut et premier du cordon spermatique à l’orifice inguinal profond (pour éviter toute dissémination hématogène lors de la mobilisation de la masse). La pièce opératoire comporte ainsi le testicule, ses annexes et le cordon spermatique jusqu’à l’orifice inguinal. Une prothèse testiculaire peut être mise en place dans le même temps ou à distance.
Un recueil de sperme pour cryoconservation doit être proposé au patient, au mieux avant l’orchidectomie, au sein d’un centre d’étude et de conservation des œufs et du sperme humains (CECOS). Il s’agit d’une mesure médico-légale puisque les traitements (radiothérapie et chimiothérapie) peuvent être responsables de troubles de la fertilité.
POINTS FORTS À RETENIR
Les tumeurs germinales du testicule représentent la première cause de tumeur maligne solide de l’homme jeune.
L’échographie scrotale est l’examen de référence de première intention pour l’exploration testiculaire.
Le diagnostic positif repose sur l’analyse anatomopathologique de la pièce d’orchidectomie.
Les marqueurs tumoraux sériques (AFP, hCG, LDH) ont un rôle dans le diagnostic, le bilan d’extension, le pronostic et le suivi de la maladie.
La tomodensitométrie thoraco-abdomino-pelvienne demeure l’examen d’imagerie de référence pour le bilan d’extension.
Une conservation du sperme doit être obligatoirement proposée, au mieux avant tout acte thérapeutique.
Le pronostic est excellent (taux de guérison de plus de 95 %) sous réserve d’une prise en charge diagnostique et thérapeutique adaptée.
Le testicule controlatéral doit être évalué et surveillé.
Comité de cancérologie de l’Association française d’urologie (CCAFU). Recommandations en onco-urologie 2020. Tumeurs germinales du testicule. www.urofrance.org
Haute Autorité de santé. ALD n° 30. Guide patient. Cancer du testicule, 2011.

 Encadrés
Encadrés