La chirurgie bariatrique (CB) constitue aujourd’hui le traitement le plus efficace en termes de perte pondérale durable et de réduction de la morbi-mortalité associée à l’obésité (diabète de type 2, maladies cardiovasculaires, cancers, notamment).1, 2 Au-delà de la perte pondérale, ses bénéfices métaboliques s’expliquent également par les modifications profondes de l’anatomie et de la physiologie digestives qu’elle entraîne. Néanmoins, ces modifications favorisent également des carences en oligo-éléments et vitamines qui, bien qu’évitables par une surveillance et une supplémentation à vie, peuvent conduire à des complications sévères et irréversibles.
À l’inverse des complications chirurgicales dont la présentation clinique peut être bruyante (fistule, hémorragie, hernie interne), le diagnostic des complications nutritionnelles et métaboliques est difficile, retardé du fait de la présentation insidieuse de la plupart des syndromes carentiels, de la non-spécificité des facteurs favorisants (troubles digestifs, mauvaise observance, troubles du comportement alimentaire) et de la perte de poids qui, recherchée dans ce contexte, ne constitue plus un signe d’alarme pour le patient et le clinicien.3 Le nombre de personnes ayant subi une opération de chirurgie bariatrique allant croissant, tout médecin généraliste ou spécialiste sera amené à prendre en charge un patient opéré et devrait connaître les principes de la surveillance. Une bonne connaissance de l’anatomie post-chirurgicale de son patient et des complications potentielles est nécessaire à la prévention de ces dernières, à leur diagnostic et à leur traitement en temps opportun. Il est donc essentiel de maîtriser les principes cliniques de la prévention et du traitement des complications fonctionnelles, métaboliques et nutritionnelles de la chirurgie bariatrique.
À l’inverse des complications chirurgicales dont la présentation clinique peut être bruyante (fistule, hémorragie, hernie interne), le diagnostic des complications nutritionnelles et métaboliques est difficile, retardé du fait de la présentation insidieuse de la plupart des syndromes carentiels, de la non-spécificité des facteurs favorisants (troubles digestifs, mauvaise observance, troubles du comportement alimentaire) et de la perte de poids qui, recherchée dans ce contexte, ne constitue plus un signe d’alarme pour le patient et le clinicien.3 Le nombre de personnes ayant subi une opération de chirurgie bariatrique allant croissant, tout médecin généraliste ou spécialiste sera amené à prendre en charge un patient opéré et devrait connaître les principes de la surveillance. Une bonne connaissance de l’anatomie post-chirurgicale de son patient et des complications potentielles est nécessaire à la prévention de ces dernières, à leur diagnostic et à leur traitement en temps opportun. Il est donc essentiel de maîtriser les principes cliniques de la prévention et du traitement des complications fonctionnelles, métaboliques et nutritionnelles de la chirurgie bariatrique.
Outre les bénéfices, les modifications anatomiques peuvent induire des complications
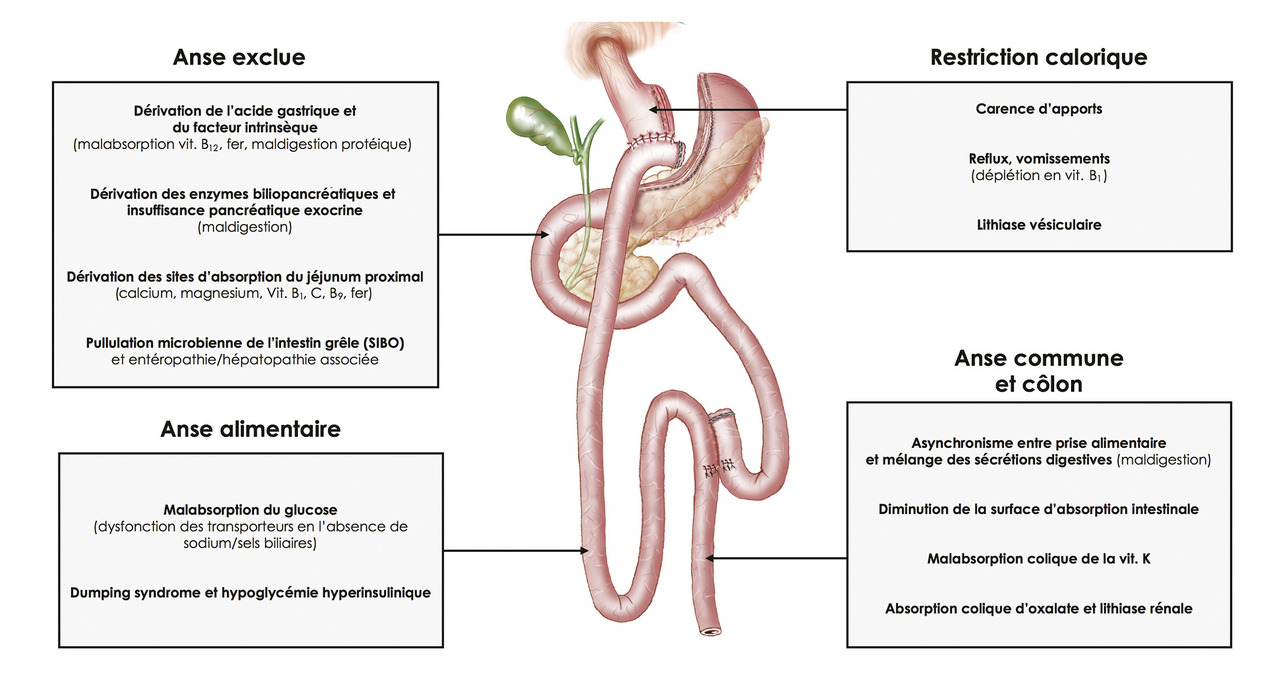
La chirurgie restrictive, telle que l’anneau gastrique (AG) et la sleeve gastrectomie (SG), limite l’absorption alimentaire en diminuant le volume gastrique. Les interventions mixtes, telles que les bypass (Roux-en-Y gastric bypass [RYGB], bypass en oméga ou one-anastomosis gastric bypass [OAGB], bilio-pancreatic diversion with duodenal switch [BPD-DS]), comportent une part de restriction et une part de malabsorption, liée à la dérivation (court-circuit) de segments intestinaux et des sécrétions digestives (maldigestion) et à la diminution de la surface d’absorption dans l’anse commune.3 Cependant, la restriction alimentaire et la perte de poids durable entraînées par les courts-circuits gastro-intestinaux s’expliquent surtout par des mécanismes neuro-hormonaux complexes induits par les modifications anatomiques du système digestif, qui renforcent la satiété et les bénéfices métaboliques.1, 3 Ces modifications anatomiques et physiologiques sous-tendent donc non seulement les bénéfices mais aussi les complications, métaboliques et nutritionnelles (fig. 1 ).
La chirurgie bariatrique induit généralement une perte de poids importante et rapide, atteignant un nadir douze à dix-huit mois après (tableau 1 ).1 Ensuite, une reprise de 5 à 10 % de poids est fréquente, favorisée par des adaptations hormonales et métaboliques, des erreurs diététiques, l’arrêt de l’activité physique ou certains médicaments (corticoïdes, psychotropes, notamment). À l’inverse, une perte de poids excessive qui s’accentue après cette période est inhabituelle ; elle doit faire rechercher une complication chirurgicale et/ou nutritionnelle.
La chirurgie bariatrique induit généralement une perte de poids importante et rapide, atteignant un nadir douze à dix-huit mois après (
Quelles carences et pour quelles raisons ?
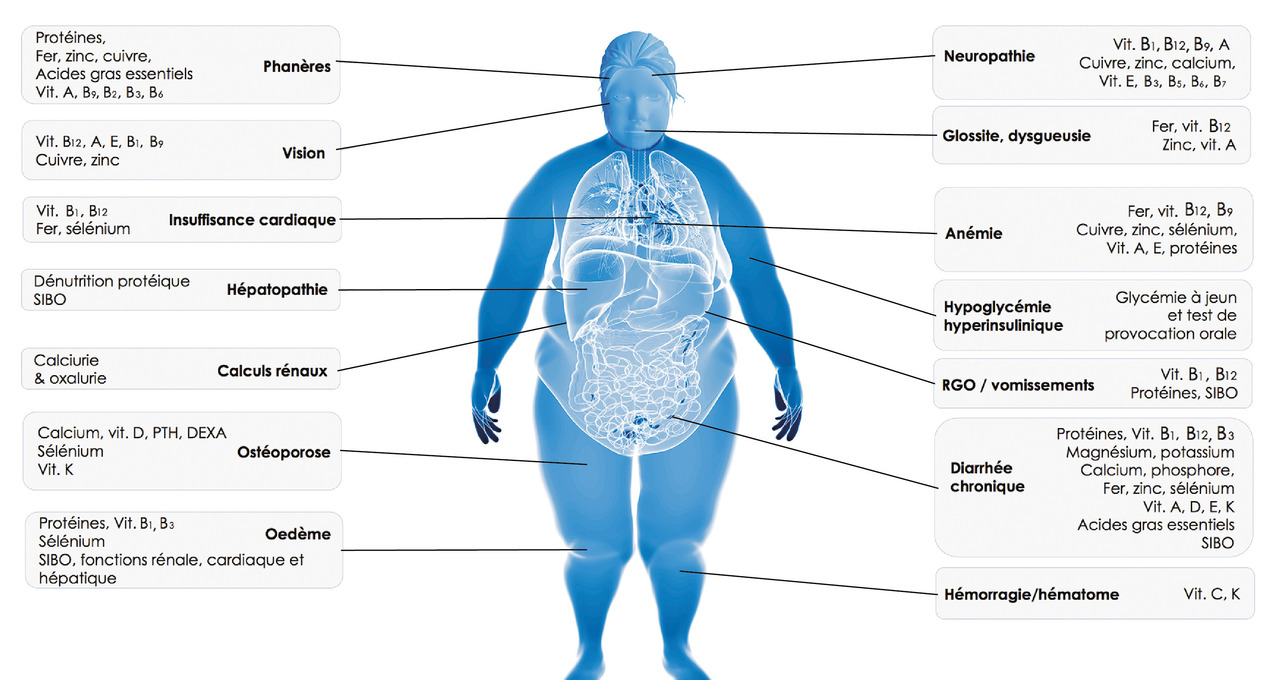
Du fait de paramètres intrinsèques (séquestration de vitamines liposolubles dans le tissu adipeux, augmentation du métabolisme oxydatif, hypersécrétion d’hepcidine, pullulation microbienne du grêle) et extrinsèques (troubles du comportement alimentaire, erreurs diététiques), l’obésité prédispose à une fréquence élevée de carences, qui préexistent à la chirurgie.4 Après la chirurgie bariatrique, ces carences peuvent s’aggraver ou apparaître en raison des changements physiologiques dus aux montages malabsorptifs (les carences sont à peu près proportionnelles à la longueur des anses intestinales exclues, maximales pour la dérivation biliopancréatique avec switch duodénal), mais sont également possibles en l’absence de dérivation du fait d’une réduction importante de l’apport calorique, d’une aversion pour certains aliments ou groupes d’aliments (viande, poisson, produits laitiers), de vomissements prolongés, ou du non-respect des conseils alimentaires et des prescriptions de micronutriments. En effet, bien que l’observance des supplémentations en vitamines soit acceptable durant six mois, elle chute à 50 % chez les adultes et 27 % chez les adolescents à plus long terme.3 En France, les déficits les plus fréquents après chirurgie bariatrique sont les carences en fer, vitamines B12 et D.1, 3-6 Les carences en zinc sont fréquentes, mais leur signification clinique est incertaine, alors que les carences en vitamine B1, moins fréquentes, ont des conséquences neurologiques potentiellement graves (tableau 2 ). Après les procédures malabsorptives, d’autres carences plus rares peuvent être observées, qu’il faut rechercher en fonction de la présentation clinique (fig. 2 ).
Les présentations cliniques orientent les recherches
Les carences nutritionnelles se manifestent par des symptômes non spécifiques tels que l’asthénie, des anomalies des phanères, des crampes ou des paresthésies. D’une façon générale, tout symptôme inexpliqué (en particulier neurologique), ou signe digestif chronique (vomissement, diarrhée), ou une perte de poids excessive qui persiste ou réapparaît au-delà du nadir pondéral après chirurgie bariatrique doit alerter sur un risque nutritionnel, ce d’autant qu’il existe un trouble du comportement alimentaire et/ou une mauvaise observance des suppléments nutritionnels.1, 3 Les présentations cliniques orientent vers les causes nutritionnelles à évoquer (fig. 2 ).
Certains signes doivent alerter
Après la chirurgie, des régurgitations/vomissements occasionnels peuvent survenir chez les patients qui ne respectent pas les conseils diététiques : petits repas fractionnés, longuement mâchés, pris lentement, boissons à distance des repas (à plus de 30 minutes), ni gazeuses ni sucrées.1, 7 Cependant, des vomissements récurrents ou persistants sont un facteur de risque majeur de carence aiguë en vitamine B1. Or toute suspicion impose une supplémentation. Il faut aussi retenir que toute perfusion de sérum glucosé doit être associée à un apport préalable et/ou simultané de vitamine B1. Ces vomissements doivent faire rechercher une cause spécifique comme un glissement de l’anneau ou un trouble moteur œsophagien après pose d’anneau gastrique, un reflux gastro-œsophagien ou une sténose médiogastrique après sleeve gastrectomie, un ulcère anastomotique (favorisé par le tabagisme actif, la prise d’anti-inflammatoires non stéroïdiens sans couverture systématique par inhibiteurs de pompe à protons) et/ou une sténose anastomotique, ou enfin une hernie interne dans le cas d’un court-circuit gastro-intestinal.1, 8 Poser le diagnostic de ces complications nécessite des investigations systématiques telles que des opacifications digestives (transit œso-gastro-duodénal ou jéjunal), un scanner abdomino-pelvien opacifié et injecté et une endoscopie digestive haute.
Une diarrhée chronique après chirurgie bariatrique est inhabituelle et doit faire évoquer un syndrome de malabsorption.1, 3, 4 La malabsorption est alors favorisée par :
– une maldigestion (induite par l’asynchronisme entre la prise alimentaire et le mélange des sécrétions digestives biliopancréatiques) ;
– une anse intestinale commune raccourcie (perte excessive de la surface d’absorption similaire à celle du syndrome du grêle court s’il mesure moins de 150 cm) ;
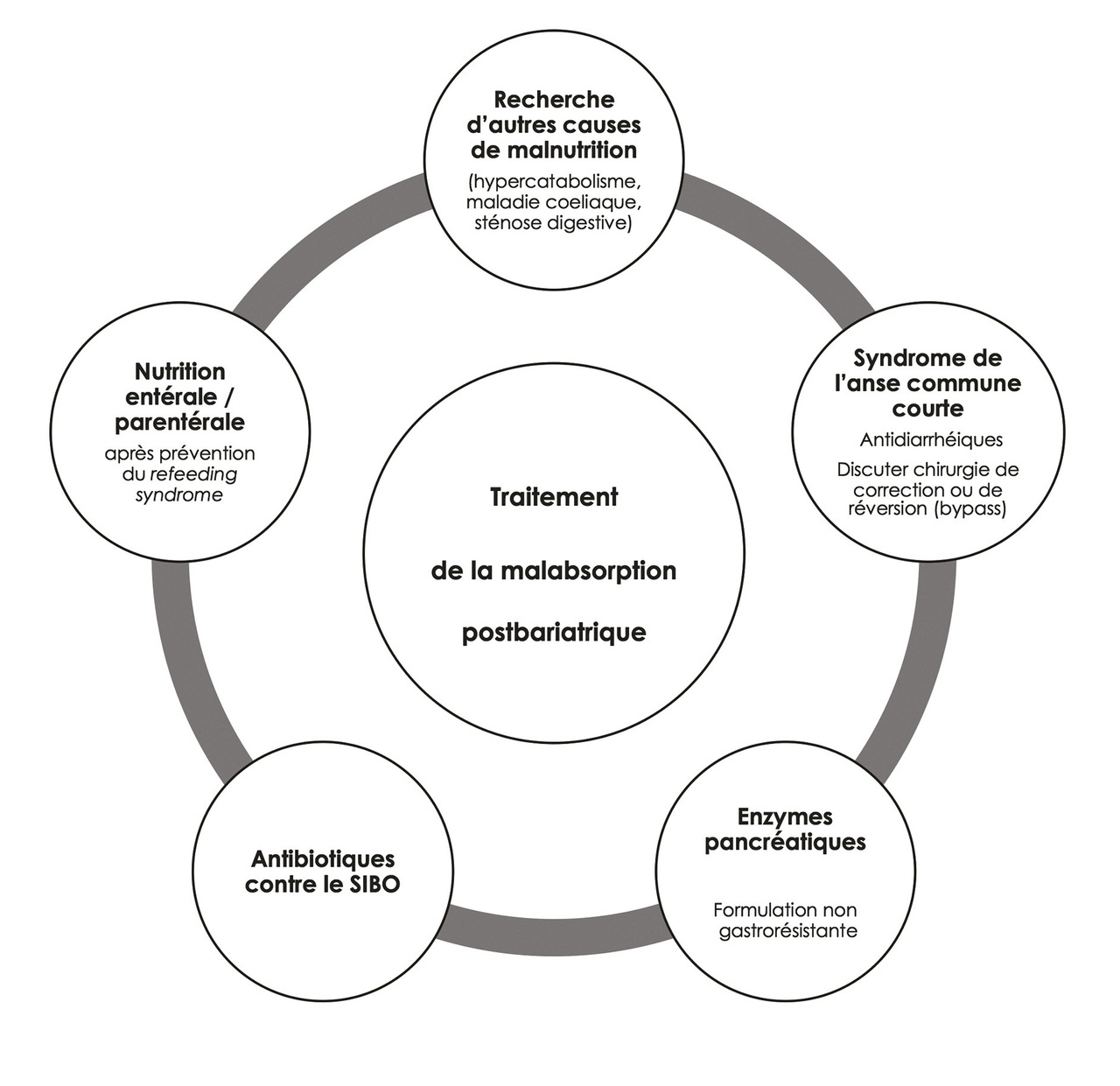
– et une prolifération bactérienne dans l’anse d’intestin grêle exclue ou SIBO (small intestinal bacterial overgrowth). La SIBO aggrave la malabsorption en induisant une atrophie villositaire, une entéropathie exsudative et une déconjugaison bactérienne des acides biliaires.3 La dénutrition protéique et la SIBO peuvent aussi induire une hépatopathie (rôle pro-inflammatoire et fibrosant des endotoxines et de la flore anaérobie, perturbation du métabolisme des acides biliaires). En raison de changements anatomiques dus à la chirurgie, la SIBO peut être difficile à prouver et un traitement antibiotique empirique d’épreuve peut être proposé.3 Les autres causes de diarrhée après chirurgie bariatrique sont l’infection à Clostridium difficile, les effets secondaires des médicaments, la diarrhée cholérétique (soulagée par la cholestyramine), l’exacerbation d’une neuropathie entérique diabétique ou l’apparition d’une maladie cœliaque/inflammatoire de l’intestin. En pratique, toute diarrhée chronique associée à un syndrome de malabsorption ou à des anomalies du bilan hépatique doit être évaluée par le centre expert référent. Après avoir traité d’éventuels facteurs favorisants (sténose digestive, complication infectieuse), une renutrition orale ou entérale et un traitement de la diarrhée par malabsorption résolvent généralement la malnutrition et l’hépatopathie (fig. 3 ). Une chirurgie correctrice est requise dans 30 à 80 % des cas extrêmes qui nécessitent une nutrition parentérale, avec une mortalité d’environ 10 %.3, 9
Une diarrhée chronique après chirurgie bariatrique est inhabituelle et doit faire évoquer un syndrome de malabsorption.1, 3, 4 La malabsorption est alors favorisée par :
– une maldigestion (induite par l’asynchronisme entre la prise alimentaire et le mélange des sécrétions digestives biliopancréatiques) ;
– une anse intestinale commune raccourcie (perte excessive de la surface d’absorption similaire à celle du syndrome du grêle court s’il mesure moins de 150 cm) ;
– et une prolifération bactérienne dans l’anse d’intestin grêle exclue ou SIBO (small intestinal bacterial overgrowth). La SIBO aggrave la malabsorption en induisant une atrophie villositaire, une entéropathie exsudative et une déconjugaison bactérienne des acides biliaires.3 La dénutrition protéique et la SIBO peuvent aussi induire une hépatopathie (rôle pro-inflammatoire et fibrosant des endotoxines et de la flore anaérobie, perturbation du métabolisme des acides biliaires). En raison de changements anatomiques dus à la chirurgie, la SIBO peut être difficile à prouver et un traitement antibiotique empirique d’épreuve peut être proposé.3 Les autres causes de diarrhée après chirurgie bariatrique sont l’infection à Clostridium difficile, les effets secondaires des médicaments, la diarrhée cholérétique (soulagée par la cholestyramine), l’exacerbation d’une neuropathie entérique diabétique ou l’apparition d’une maladie cœliaque/inflammatoire de l’intestin. En pratique, toute diarrhée chronique associée à un syndrome de malabsorption ou à des anomalies du bilan hépatique doit être évaluée par le centre expert référent. Après avoir traité d’éventuels facteurs favorisants (sténose digestive, complication infectieuse), une renutrition orale ou entérale et un traitement de la diarrhée par malabsorption résolvent généralement la malnutrition et l’hépatopathie (
Différents syndromes carentiels
Les carences exposent à différents types d’anémie et de complications neurologiques, à une perte osseuse ou encore à une lithiase.
tableaux 1 et 2 ). Grâce à des stocks hépatiques importants, la carence en vitamine B12 est généralement plus tardive (2-3 ans). Son dépistage peut être amélioré en mesurant l’acide méthylmalonique sérique, marqueur plus sensible et plus précoce. En effet, sa voie métabolique dépend de la vitamine B12 comme cofacteur, il s’accumule donc en cas de carence.3, 4, 7
fig. 2 ).3, 4, 7, 10 Les complications les plus courantes sont les neuropathies périphériques, tandis que l’encéphalopathie aiguë (Wernicke) et chronique (Korsakoff), la myélopathie et la neuropathie optique sont les plus graves, potentiellement mortelles ou invalidantes. Les stocks corporels de vitamine B1 étant faibles, une encéphalopathie peut survenir après seulement quelques jours/semaines de nausées/vomissements récurrents. La présentation clinique et les résultats de l’imagerie par résonance magnétique (IRM) étant souvent atypiques, toute suspicion impose un traitement immédiat (tableau 2 ) et toute perfusion de glucose doit être supplémentée en vitamine B1, du fait du risque d’aggravation du tableau par l’apport de glucose.
– une supplémentation en calcium et vitamine D (tableaux 1 et 2 ), guidée par une évaluation régulière de leur métabolisme et de la densité minérale osseuse ;
– la promotion de l’activité physique ;
– et un traitement par biphosphonates pour patients à haut risque.11
Le dumping syndrome tardif (renommé hypoglycémie post-prandiale hyperinsulinémique), complication potentiellement grave, survient un à trois ans après la chirurgie et correspond à une hypoglycémie post-prandiale tardive (une à trois heures après le repas) provoquée par une exacerbation des pics post-prandiaux de glucose, de GLP-1 et d’insuline. Les hypoglycémies sévères (confusion, perte de conscience, convulsions) sont rares (0,2 à 1 %) mais peuvent être très invalidantes, voire mortelles. Après confirmation par un test de provocation orale et avoir éliminé un insulinome, la prise en charge en centre expert repose sur les mesures diététiques (éviction des sucres rapides), l’éducation du patient aux signes d’hypoglycémie, voire un traitement médicamenteux diminuant les pics de glucose (acarbose) ou d’insuline (les médicaments suivants ont été testés dans quelques séries de patients : diazoxide, nifédipine, analogues de la somatostatine, analogues GLP-1) ou le démontage chirurgical du bypass.3, 12
La chirurgie bariatrique et la perte de poids sont des facteurs de risque bien établis de calculs biliaires, avec un risque de cholécystectomie de 7-10 % après trois ans en moyenne.14 Ce risque justifie une prescription prophylactique systématique d’acide ursodésoxycholique par voie orale pendant les six mois qui suivent l’intervention. La cholangiopancréatographie rétrograde endoscopique (CPRE) n’étant plus réalisable après court-circuit gastro-intestinal, une cholécystectomie est discutée avant la chirurgie bariatrique chez les patients asymptomatiques en présence de calculs biliaires connus.1, 3, 5
L’anémie est fréquente
L’anémie résulte de carences en fer et en vitamine B12 secondaires à l’hypochlorhydrie et à l’exclusion (dérivation) de leurs sites d’absorption duodénaux. La supplémentation en fer est optimisée par la vitamine C et par une prise décalée par rapport à celle des suppléments de calcium ou de zinc (Un large spectre de troubles neurologiques
Différents troubles neurologiques ont été décrits chez 1 à 16 % des patients, parfois de nombreuses années après tout type de chirurgie bariatrique.10 Les personnes opérées doivent donc être éduquées à en reconnaître les premiers signes, tels que troubles de la mémoire, de la marche, une faiblesse ou une confusion. Les carences en vitamines B1, B12, B9, A et en cuivre sont les plus fréquemment en cause (tableau 2,Ostéoporose et risque fracturaire
La chirurgie bariatrique provoque une perte osseuse et une altération de la micro-architecture de l’os multifactorielles : diminution de la charge pondérale, de l’absorption de vitamine D et de calcium, hyperparathyroïdie, malnutrition protéique. Ces modifications entraînent un surrisque fracturaire qui débute deux à cinq ans après la chirurgie.11 La prise en charge comprend :– une supplémentation en calcium et vitamine D (
– la promotion de l’activité physique ;
– et un traitement par biphosphonates pour patients à haut risque.11
Dumping syndrome précoce et hypoglycémie postprandiale hyperinsulinique
Le dumping syndrome correspond à des symptômes postprandiaux liés à une vidange (dumping) gastrique trop rapide ou prématurée dans l’intestin grêle.12 Le dumping syndrome précoce, complication fonctionnelle courante et bénigne (10-75 %) du bypass gastrique et de la sleeve gastrectomie, survient tôt après la chirurgie (1re année) et tôt après le repas (de quelques minutes à une heure). Il associe des symptômes gastro-intestinaux (nausée, ballonnement, diarrhée) et vasomoteurs (fatigue, besoin de s’allonger, tachycardie, bouffées de chaleur) liés à l’arrivée rapide de nutriments mal digérés hyperosmolaires dans l’intestin grêle. La glycémie est normale ou augmentée. Ce syndrome peut régresser avec l’éviction des aliments favorisants.12Le dumping syndrome tardif (renommé hypoglycémie post-prandiale hyperinsulinémique), complication potentiellement grave, survient un à trois ans après la chirurgie et correspond à une hypoglycémie post-prandiale tardive (une à trois heures après le repas) provoquée par une exacerbation des pics post-prandiaux de glucose, de GLP-1 et d’insuline. Les hypoglycémies sévères (confusion, perte de conscience, convulsions) sont rares (0,2 à 1 %) mais peuvent être très invalidantes, voire mortelles. Après confirmation par un test de provocation orale et avoir éliminé un insulinome, la prise en charge en centre expert repose sur les mesures diététiques (éviction des sucres rapides), l’éducation du patient aux signes d’hypoglycémie, voire un traitement médicamenteux diminuant les pics de glucose (acarbose) ou d’insuline (les médicaments suivants ont été testés dans quelques séries de patients : diazoxide, nifédipine, analogues de la somatostatine, analogues GLP-1) ou le démontage chirurgical du bypass.3, 12
Calculs rénaux et biliaires
Une augmentation du risque de calculs rénaux d’oxalate de calcium a été rapportée un à trois ans après la chirurgie.13 Dans des conditions physiologiques, l’oxalate alimentaire forme des sels insolubles avec le calcium alimentaire et est mal absorbé. En cas de malabsorption des graisses, le calcium est saponifié dans les graisses, et l’oxalate solitaire est absorbé dans le côlon, puis éliminé par le rein, où il cristallise avec le calcium dans la lumière tubulaire. Le traitement repose sur une prévention de la déshydratation, un régime alimentaire pauvre en oxalate, une supplémentation calcique, et le citrate de potassium (le citrate entre en compétition avec l’oxalate urinaire pour se lier au calcium).1, 3, 5, 13La chirurgie bariatrique et la perte de poids sont des facteurs de risque bien établis de calculs biliaires, avec un risque de cholécystectomie de 7-10 % après trois ans en moyenne.14 Ce risque justifie une prescription prophylactique systématique d’acide ursodésoxycholique par voie orale pendant les six mois qui suivent l’intervention. La cholangiopancréatographie rétrograde endoscopique (CPRE) n’étant plus réalisable après court-circuit gastro-intestinal, une cholécystectomie est discutée avant la chirurgie bariatrique chez les patients asymptomatiques en présence de calculs biliaires connus.1, 3, 5
Supplémentation systématique et surveillance à vie
Les complications nutritionnelles de la chirurgie bariatrique sont facilement évitables par un suivi strict à vie, recommandé pour tous les patients par les sociétés savantes américaines1, 12, européennes et françaises5, 7, 15 (tableaux 1 et 2 ). Il doit inclure :
– une surveillance biologique des vitamines et oligo-éléments (tous les trois à six mois en période de perte de poids, au moins annuelle ensuite) ;
– et une supplémentation systématique en micronutriments : multivitamines, calcium-vitamine D, fer et vitamine B12 (également vitamine B1 en cas de vomissements et vitamine B9 en cas de grossesse), avec un apport protéique suffisant.1, 4, 5, 7, 15
De plus, un dépistage spécifique des carences en micronutriments est nécessaire devant des signes cliniques d’alerte (signes digestifs, perte de poids excessive), un syndrome carentiel (fig. 2 ) ou dans les situations à risque accru de malnutrition (troubles psychologiques, du comportement alimentaire, abus d’alcool, adolescence et grossesse). Cependant, ces recommandations sont mal suivies en pratique, tant par les patients que par leurs médecins. Les propositions pour améliorer le suivi incluent la réduction du nombre de comprimés et de leur coût, ainsi que l’amélioration de l’éducation du patient et de la communauté médicale aux complications de la chirurgie bariatrique. Compte tenu des risques encourus, il faut rappeler l’importance de la phase de préparation préopératoire et de l’éducation thérapeutique.
Avec l’augmentation du nombre de personnes opérées, le nombre de patients qui développent des complications nutritionnelles potentiellement graves à long terme augmente. Le suivi au long cours et l’adhésion du patient sont essentiels dans cette situation clinique paradoxale où la perte de poids tant attendue peut aussi s’associer à des carences potentiellement morbides. En tant que médecins, il est de notre responsabilité de nous familiariser avec ces interventions et leurs éventuelles conséquences, et de développer des stratégies pour améliorer l’adhésion à vie des patients aux mesures diététiques, aux prescriptions de suppléments et au suivi.
– une surveillance biologique des vitamines et oligo-éléments (tous les trois à six mois en période de perte de poids, au moins annuelle ensuite) ;
– et une supplémentation systématique en micronutriments : multivitamines, calcium-vitamine D, fer et vitamine B12 (également vitamine B1 en cas de vomissements et vitamine B9 en cas de grossesse), avec un apport protéique suffisant.1, 4, 5, 7, 15
De plus, un dépistage spécifique des carences en micronutriments est nécessaire devant des signes cliniques d’alerte (signes digestifs, perte de poids excessive), un syndrome carentiel (
Avec l’augmentation du nombre de personnes opérées, le nombre de patients qui développent des complications nutritionnelles potentiellement graves à long terme augmente. Le suivi au long cours et l’adhésion du patient sont essentiels dans cette situation clinique paradoxale où la perte de poids tant attendue peut aussi s’associer à des carences potentiellement morbides. En tant que médecins, il est de notre responsabilité de nous familiariser avec ces interventions et leurs éventuelles conséquences, et de développer des stratégies pour améliorer l’adhésion à vie des patients aux mesures diététiques, aux prescriptions de suppléments et au suivi.
Références
1. Mechanick JI, Apovian C, Brethauer S, Garvey WT, Joffe AM, Kim J, et al. Clinical Practice Guidelines for the Perioperative Nutrition, Metabolic, and Nonsurgical Support of Patients Undergoing Bariatric Procedures - 2019 Update: cosponsored by American Association of Clinical Endocrinologists/American College of Endocrinology, Obesity Society, American Society for Metabolic & Bariatric Surgery, Obesity Medicine Association, and American Society of Anesthesiologists - Executive Summary. Endocr Pract 2019;25:1346-59.
2. Thereaux J, Lesuffleur T, Czernichow S, Basdevant A, Msika S, Nocca D, et al. Long-term adverse events after sleeve gastrectomy or gastric bypass: a 7-year nationwide, observational, population-based, cohort study. Lancet Diabetes Endocrinol 2019;7:786-95.
3. Nuzzo A, Czernichow S, Hertig A, Ledoux S, Poghosyan T, Quilliot D, et al. Prevention and treatment of nutritional complications after bariatric surgery. Lancet Gastroenterol Hepatol 2021;6:238-51.
4. Parrott J, Frank L, Rabena R, Craggs-Dino L, Isom KA, Greiman L. American Society for Metabolic and Bariatric Surgery Integrated Health Nutritional Guidelines for the Surgical Weight Loss Patient 2016 Update: Micronutrients. Surg Obes Relat Dis 2017;13:727-41.
5. Fried M, Yumuk V, Oppert JM, Scopinaro N, Torres AJ, Weiner R, et al. Interdisciplinary European Guidelines on metabolic and bariatric surgery. Obes Facts 2013;6:449-68.
6. Ledoux S, Calabrese D, Bogard C, Dupré T, Castel B, Msika S, et al. Long-term evolution of nutritional deficiencies after gastric bypass: an assessment according to compliance to medical care. Ann Surg 2014;259:1104-10.
7. Quilliot D, Coupaye M, Ciangura C, Czernichow S, Sallé A, Gaborit B, et al. Recommendations for nutritional care after bariatric surgery: Recommendations for best practice and SOFFCO-MM/AFERO/SFNCM/expert consensus. J Visc Surg 2021;158:51-61.
8. Angrisani L, Santonicola A, Iovino P, Vitiello A, Higa K, Himpens J, et al. IFSO Worldwide Survey 2016: Primary, Endoluminal, and Revisional Procedures. Obes Surg 2018;28:3783-94.
9. Van Gossum A, Pironi L, Chambrier C, Dreesen M, Brandt CF, Santarpia L, et al. Home parenteral nutrition (HPN) in patients with post-bariatric surgery complications. Clin Nutr 2017;36:1345-8.
10. Landais A. Neurological complications of bariatric surgery. Obes Surg 2014;24:1800-7.
11. Zhang Q, Chen Y, Li J, Chen D, Cheng Z, Xu S, et al. A meta-analysis of the effects of bariatric surgery on fracture risk. Obes Rev 2018;19:728-36.
12. Eisenberg D, Azagury DE, Ghiassi S, Grover BT, Kim JJ. ASMBS Position statement on postprandial hyperinsulinemic hypoglycemia after bariatric surgery. Surg Obes Relat Dis 2017;13:371-8.
13. Lieske JC, Mehta RA, Milliner DS, Rule AD, Bergstralh EJ, Sarr MG. Kidney stones are common after bariatric surgery. Kidney Int 2015;87:839-45.
14. Coupaye M, Castel B, Sami O, Tuyeras G, Msika S, Ledoux S. Comparison of the incidence of cholelithiasis after sleeve gastrectomy and Roux-en-Y gastric bypass in obese patients: a prospective study. Surg Obes Relat Dis 2015;11:779-84.
15. Busetto L, Dicker D, Azran C, Batterham RL, Farpour-Lambert N, Fried M, et al. Obesity management task force of the European Association for the Study of Obesity released «Practical recommendations for the post-bariatric surgery medical management». Obes Surg 2018;28:2117-21.
2. Thereaux J, Lesuffleur T, Czernichow S, Basdevant A, Msika S, Nocca D, et al. Long-term adverse events after sleeve gastrectomy or gastric bypass: a 7-year nationwide, observational, population-based, cohort study. Lancet Diabetes Endocrinol 2019;7:786-95.
3. Nuzzo A, Czernichow S, Hertig A, Ledoux S, Poghosyan T, Quilliot D, et al. Prevention and treatment of nutritional complications after bariatric surgery. Lancet Gastroenterol Hepatol 2021;6:238-51.
4. Parrott J, Frank L, Rabena R, Craggs-Dino L, Isom KA, Greiman L. American Society for Metabolic and Bariatric Surgery Integrated Health Nutritional Guidelines for the Surgical Weight Loss Patient 2016 Update: Micronutrients. Surg Obes Relat Dis 2017;13:727-41.
5. Fried M, Yumuk V, Oppert JM, Scopinaro N, Torres AJ, Weiner R, et al. Interdisciplinary European Guidelines on metabolic and bariatric surgery. Obes Facts 2013;6:449-68.
6. Ledoux S, Calabrese D, Bogard C, Dupré T, Castel B, Msika S, et al. Long-term evolution of nutritional deficiencies after gastric bypass: an assessment according to compliance to medical care. Ann Surg 2014;259:1104-10.
7. Quilliot D, Coupaye M, Ciangura C, Czernichow S, Sallé A, Gaborit B, et al. Recommendations for nutritional care after bariatric surgery: Recommendations for best practice and SOFFCO-MM/AFERO/SFNCM/expert consensus. J Visc Surg 2021;158:51-61.
8. Angrisani L, Santonicola A, Iovino P, Vitiello A, Higa K, Himpens J, et al. IFSO Worldwide Survey 2016: Primary, Endoluminal, and Revisional Procedures. Obes Surg 2018;28:3783-94.
9. Van Gossum A, Pironi L, Chambrier C, Dreesen M, Brandt CF, Santarpia L, et al. Home parenteral nutrition (HPN) in patients with post-bariatric surgery complications. Clin Nutr 2017;36:1345-8.
10. Landais A. Neurological complications of bariatric surgery. Obes Surg 2014;24:1800-7.
11. Zhang Q, Chen Y, Li J, Chen D, Cheng Z, Xu S, et al. A meta-analysis of the effects of bariatric surgery on fracture risk. Obes Rev 2018;19:728-36.
12. Eisenberg D, Azagury DE, Ghiassi S, Grover BT, Kim JJ. ASMBS Position statement on postprandial hyperinsulinemic hypoglycemia after bariatric surgery. Surg Obes Relat Dis 2017;13:371-8.
13. Lieske JC, Mehta RA, Milliner DS, Rule AD, Bergstralh EJ, Sarr MG. Kidney stones are common after bariatric surgery. Kidney Int 2015;87:839-45.
14. Coupaye M, Castel B, Sami O, Tuyeras G, Msika S, Ledoux S. Comparison of the incidence of cholelithiasis after sleeve gastrectomy and Roux-en-Y gastric bypass in obese patients: a prospective study. Surg Obes Relat Dis 2015;11:779-84.
15. Busetto L, Dicker D, Azran C, Batterham RL, Farpour-Lambert N, Fried M, et al. Obesity management task force of the European Association for the Study of Obesity released «Practical recommendations for the post-bariatric surgery medical management». Obes Surg 2018;28:2117-21.