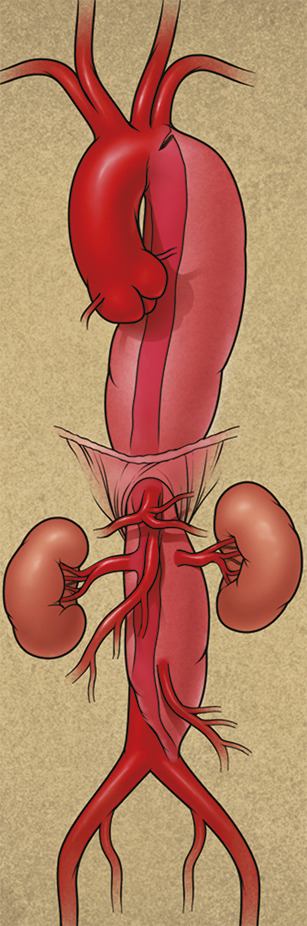
Un patient qui a survécu à la phase aiguë de sa dissection aortique doit être pris en charge au long cours, comme pour une pathologie chronique de l’aorte. En effet, la dissection aortique, qui s’étend fréquemment (une fois l’aorte ascendante remplacée ou non) de la crosse aortique aux artères iliaques, voire fémorales, comporte toujours un risque d’évolution anévrismale du faux chenal et donc de rupture secondaire ; elle doit être surveillée.
Traitement médical nécessaire mais pas suffisant
Le traitement médical considéré comme optimal repose, bien sûr, sur le contrôle strict de la pression artérielle avec un objectif < 120/80 mmHg, mais il ne garantit pas l’absence d’évolution anévrismale de l’aorte. Les données de l’International Registry of Acute Aortic Dissection (IRAD) confirment que deux tiers des patients connaîtront une évolution anévrismale de leur aorte thoraco-abdominale (descendante et juxta-diaphragmatique), malgré un traitement médical bien conduit1, imposant une intervention chirurgicale secondaire dans 60 % des cas à six ans.2 La plupart des études de suivi après dissection aortique font ainsi état d’une mortalité de 25 % à trois ans3, et d’une médiane de survie de l’ordre de 50 % à cinq ou six ans. Ces chiffres alarmants justifient pleinement une surveillance médicale et radiologique régulière à trois, six, douze mois, puis annuelle.
Chirurgie préventive à haut risque
En cas d’évolution anévrismale d’un diamètre > 55 mm, le risque de rupture secondaire dépasse 20 % par an et augmente de façon exponentielle avec le diamètre aortique (fig. 1 ).4
Une intervention préventive peut alors être proposée, afin d’éviter cette rupture secondaire de l’aorte. Mais les zones de l’aorte disséquée évoluant le plus souvent vers une dégénérescence anévrismale, soit la crosse aortique et l’aorte thoracique descendante, jusqu’à l’aorte viscérale, sont aussi celles dont le remplacement est le plus complexe. Le remplacement de la crosse aortique expose à des risques élevés d’accident vasculaire peropératoire (10-20 %), celui de l’aorte thoracique descendante au risque de paraplégie par ischémie médullaire (5-10 %), et celui de l’aorte viscérale aux risques d’ischémie digestive et d’insuffisance rénale terminale suivie d’hémodialyse au long cours.5 Bien qu’elles soient réalisées dans les centres d’expertise, ces procédures itératives engendrent une mortalité qui reste relativement élevée, de l’ordre de 10 à 20 %, qu’il s’agisse de chirurgies ouvertes par thoracotomie ou de traitements endovasculaires complexes, au moyen d’endoprothèses fenêtrées ou branchées.6 Ces dernières techniques, innovantes, font l’objet d’une surveillance particulière, compte tenu du risque élevé de défaut d’étanchéité (ou endofuites).7
Il apparaît donc qu’une majorité des patients suivis pour une dissection aortique sont condamnés, malgré un traitement médical optimal, à subir des réinterventions aortiques complexes dans les cinq ans qui suivent le diagnostic initial, afin de les protéger d’une rupture aortique secondaire fatale. Ce risque évolutif, associé à un traitement médical contraignant, induit de grands bouleversements dans la vie des patients, entraînant souvent un reclassement professionnel, et un stress post-traumatique nécessitant une réadaptation à l’effort et un accompagnement médico-psychologique.8
Une intervention préventive peut alors être proposée, afin d’éviter cette rupture secondaire de l’aorte. Mais les zones de l’aorte disséquée évoluant le plus souvent vers une dégénérescence anévrismale, soit la crosse aortique et l’aorte thoracique descendante, jusqu’à l’aorte viscérale, sont aussi celles dont le remplacement est le plus complexe. Le remplacement de la crosse aortique expose à des risques élevés d’accident vasculaire peropératoire (10-20 %), celui de l’aorte thoracique descendante au risque de paraplégie par ischémie médullaire (5-10 %), et celui de l’aorte viscérale aux risques d’ischémie digestive et d’insuffisance rénale terminale suivie d’hémodialyse au long cours.5 Bien qu’elles soient réalisées dans les centres d’expertise, ces procédures itératives engendrent une mortalité qui reste relativement élevée, de l’ordre de 10 à 20 %, qu’il s’agisse de chirurgies ouvertes par thoracotomie ou de traitements endovasculaires complexes, au moyen d’endoprothèses fenêtrées ou branchées.6 Ces dernières techniques, innovantes, font l’objet d’une surveillance particulière, compte tenu du risque élevé de défaut d’étanchéité (ou endofuites).7
Il apparaît donc qu’une majorité des patients suivis pour une dissection aortique sont condamnés, malgré un traitement médical optimal, à subir des réinterventions aortiques complexes dans les cinq ans qui suivent le diagnostic initial, afin de les protéger d’une rupture aortique secondaire fatale. Ce risque évolutif, associé à un traitement médical contraignant, induit de grands bouleversements dans la vie des patients, entraînant souvent un reclassement professionnel, et un stress post-traumatique nécessitant une réadaptation à l’effort et un accompagnement médico-psychologique.8
Prise en charge précoce des patients à risque élevé
La recherche de facteurs prédictifs d’évolution anévrismale, dès la phase aiguë, a permis d’identifier une population de patients à risque : sexe masculin, âge < 60 ans, diamètre maximal aortique > 40 mm, porte d’entrée large > 10 mm, maladie génétique associée.9, 10
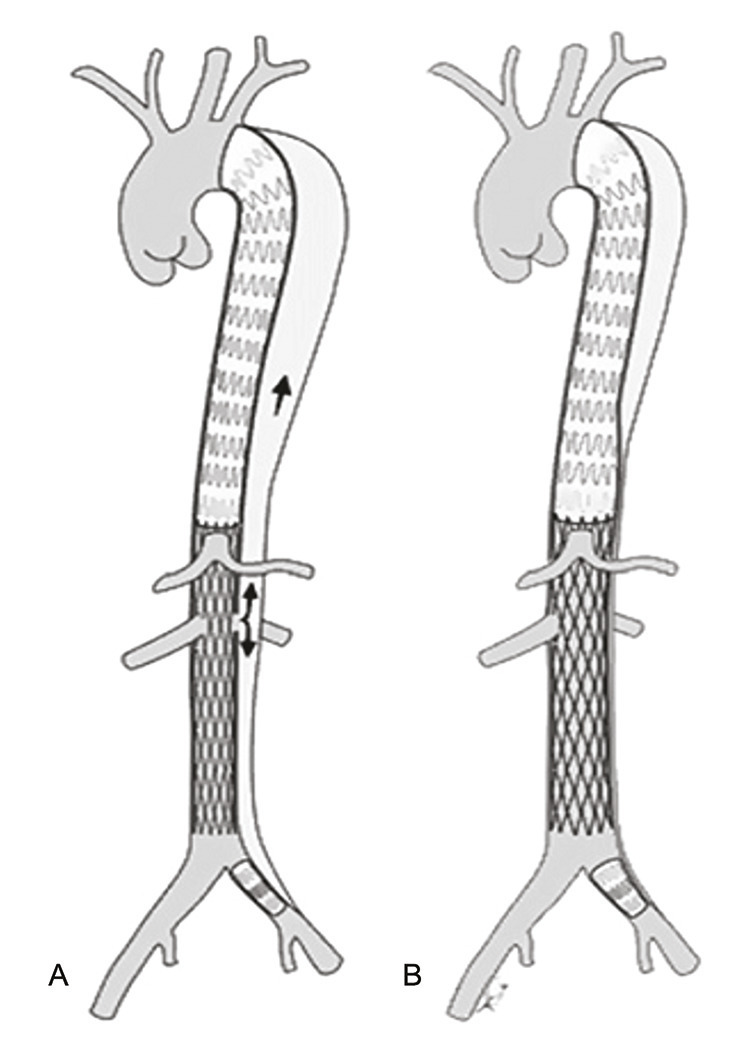
Il paraît donc licite de proposer à ce sous-groupe de patients à risque élevé d’évolution anévrismale une prise en charge endovasculaire plus agressive dès la phase initiale de la maladie. En effet, des techniques endovasculaires, en cours d’évaluation, combinant fermeture de la porte d’entrée principale au moyen d’une endoprothèse couverte et fenestration distale de l’aorte viscérale avec réaccolement du flap de dissection par un stent non couvert auto-expansible (technique STABILISE), permettent d’obtenir une cicatrisation (ou remodelage) précoce de la dissection aortique (fig. 2 ), avant que le faux chenal ne soit trop dilaté.11 Cette intervention endovasculaire, réalisée par voie fémorale percutanée dès la phase initiale de la dissection, offre une option peu invasive de traitement préventif du risque de dégénérescence anévrismale.12 La cicatrisation complète de l’aorte thoracique descendante et viscérale, jusqu’au niveau de l’aorte sous-rénale, ainsi obtenue par voie endovasculaire avec des taux de complications périopératoires faibles, constitue un réel espoir de contrecarrer l’évolution chronique des dissections aortiques, et de permettre aux patients la reprise de leurs activités de façon beaucoup plus sereine sur le long terme.
Il paraît donc licite de proposer à ce sous-groupe de patients à risque élevé d’évolution anévrismale une prise en charge endovasculaire plus agressive dès la phase initiale de la maladie. En effet, des techniques endovasculaires, en cours d’évaluation, combinant fermeture de la porte d’entrée principale au moyen d’une endoprothèse couverte et fenestration distale de l’aorte viscérale avec réaccolement du flap de dissection par un stent non couvert auto-expansible (technique STABILISE), permettent d’obtenir une cicatrisation (ou remodelage) précoce de la dissection aortique (
La voie endovasculaire en prévention
Une meilleure connaissance de l’évolution de la dissection aortique et du risque de dégénérescence anévrismale permet de focaliser la surveillance sur les patients les plus à risque, et de leur proposer, le cas échéant, un traitement préventif adapté, possiblement par voie endovasculaire.
Références
1. Fattori R, Montgomery D, Lovato L, Kische S, Di Eusanio M, Ince H, et al. Survival after endovascular therapy in patients with type B aortic dissection: a report from the International Registry of Acute Aortic Dissection (IRAD). JACC Cardiovasc Interv 2013;6(8):876-82.
2. Durham CA, Cambria RP, Wang LJ, Ergul EA, Aranson NJ, Patel VI, et al. The natural history of medically managed acute type B aortic dissection. J Vasc Surg 2015;61(5):1192-8.
3. Tsai TT, Fattori R, Trimarchi S, Isselbacher E, Myrmel T, Evangelista A, et al; International Registry of Acute Aortic Dissection. Long-term survival in patients presenting with type B acute aortic dissection: insights from the International Registry of Acute Aortic Dissection. Circulation 2006;114(21):2226-31.
4. Oda T, Minatoya K, Sasaki H, Tanaka H, Seike Y, Itonaga T, et al. Surgical indication for chronic aortic dissection in descending thoracic and thoracoabdominal aorta. Circ Cardiovasc Interv 2017;10(2):e004292.
5. Alfonsi J, Murana G, Smeenk HG, Kelder H, Schepens M, Sonker U, et al. Open surgical repair of post-dissection thoraco-abdominal aortic aneurysms: early and late outcomes of a single-centre study involving over 200 patients. Eur J Cardiothorac Surg 2018;54(2):382-8.
6. Spear R, Hertault A, Van Calster K, Settembre N, Delloye M, Azzaoui R, et al. Complex endovascular repair of postdissection arch and thoracoabdominal aneurysms. J Vasc Surg 2018;67(3):685-93.
7. Czerny M, Schmidli J, Adler S, van den Berg JC, Bertoglio L, Carrel T, et al. Editor’s choice - Current options and recommendations for the treatment of thoracic aortic pathologies involving the aortic arch: an expert consensus document of the European Association for Cardio-Thoracic Surgery (EACTS) & the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg 2019;57(2):165-98.
8. Pasadyn SR, Roselli EE, Artis AS, Pasadyn CL, Phelan D, Hurley K, et al. From tear to fear: Posttraumatic stress disorder in patients with acute type A aortic dissection. J Am Heart Assoc 2020;9(9):e015060.
9. Trimarchi S, Jonker FH, van Bogerijen GH, Tolenaar JL, Moll FL, Czerny M, et al. Predicting aortic enlargement in type B aortic dissection. Ann Cardiothorac Surg 2014;3(3):285-91.
10. van Bogerijen GH, Tolenaar JL, Rampoldi V, Moll FL, van Herwaarden JA, Jonker FH, et al. Predictors of aortic growth in uncomplicated type B aortic dissection. J Vasc Surg 2014;59(4):1134-43.
11. Hofferberth SC, Nixon IK, Boston RC, McLachlan CS, Mossop PJ. Stent-assisted balloon-induced intimal disruption and relamination in aortic dissection repair: the STABILISE concept. J Thorac Cardiovasc Surg 2014;147(4):1240-5.
12. Faure EM, El Batti S, Abou Rjeili M, Julia P, Alsac JM. Mid-term outcomes of stent assisted balloon induced intimal disruption and relamination in aortic dissection repair (STABILISE) in acute type B aortic dissection. Eur J Vasc Endovasc Surg 2018;56(2):209-15.
2. Durham CA, Cambria RP, Wang LJ, Ergul EA, Aranson NJ, Patel VI, et al. The natural history of medically managed acute type B aortic dissection. J Vasc Surg 2015;61(5):1192-8.
3. Tsai TT, Fattori R, Trimarchi S, Isselbacher E, Myrmel T, Evangelista A, et al; International Registry of Acute Aortic Dissection. Long-term survival in patients presenting with type B acute aortic dissection: insights from the International Registry of Acute Aortic Dissection. Circulation 2006;114(21):2226-31.
4. Oda T, Minatoya K, Sasaki H, Tanaka H, Seike Y, Itonaga T, et al. Surgical indication for chronic aortic dissection in descending thoracic and thoracoabdominal aorta. Circ Cardiovasc Interv 2017;10(2):e004292.
5. Alfonsi J, Murana G, Smeenk HG, Kelder H, Schepens M, Sonker U, et al. Open surgical repair of post-dissection thoraco-abdominal aortic aneurysms: early and late outcomes of a single-centre study involving over 200 patients. Eur J Cardiothorac Surg 2018;54(2):382-8.
6. Spear R, Hertault A, Van Calster K, Settembre N, Delloye M, Azzaoui R, et al. Complex endovascular repair of postdissection arch and thoracoabdominal aneurysms. J Vasc Surg 2018;67(3):685-93.
7. Czerny M, Schmidli J, Adler S, van den Berg JC, Bertoglio L, Carrel T, et al. Editor’s choice - Current options and recommendations for the treatment of thoracic aortic pathologies involving the aortic arch: an expert consensus document of the European Association for Cardio-Thoracic Surgery (EACTS) & the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg 2019;57(2):165-98.
8. Pasadyn SR, Roselli EE, Artis AS, Pasadyn CL, Phelan D, Hurley K, et al. From tear to fear: Posttraumatic stress disorder in patients with acute type A aortic dissection. J Am Heart Assoc 2020;9(9):e015060.
9. Trimarchi S, Jonker FH, van Bogerijen GH, Tolenaar JL, Moll FL, Czerny M, et al. Predicting aortic enlargement in type B aortic dissection. Ann Cardiothorac Surg 2014;3(3):285-91.
10. van Bogerijen GH, Tolenaar JL, Rampoldi V, Moll FL, van Herwaarden JA, Jonker FH, et al. Predictors of aortic growth in uncomplicated type B aortic dissection. J Vasc Surg 2014;59(4):1134-43.
11. Hofferberth SC, Nixon IK, Boston RC, McLachlan CS, Mossop PJ. Stent-assisted balloon-induced intimal disruption and relamination in aortic dissection repair: the STABILISE concept. J Thorac Cardiovasc Surg 2014;147(4):1240-5.
12. Faure EM, El Batti S, Abou Rjeili M, Julia P, Alsac JM. Mid-term outcomes of stent assisted balloon induced intimal disruption and relamination in aortic dissection repair (STABILISE) in acute type B aortic dissection. Eur J Vasc Endovasc Surg 2018;56(2):209-15.