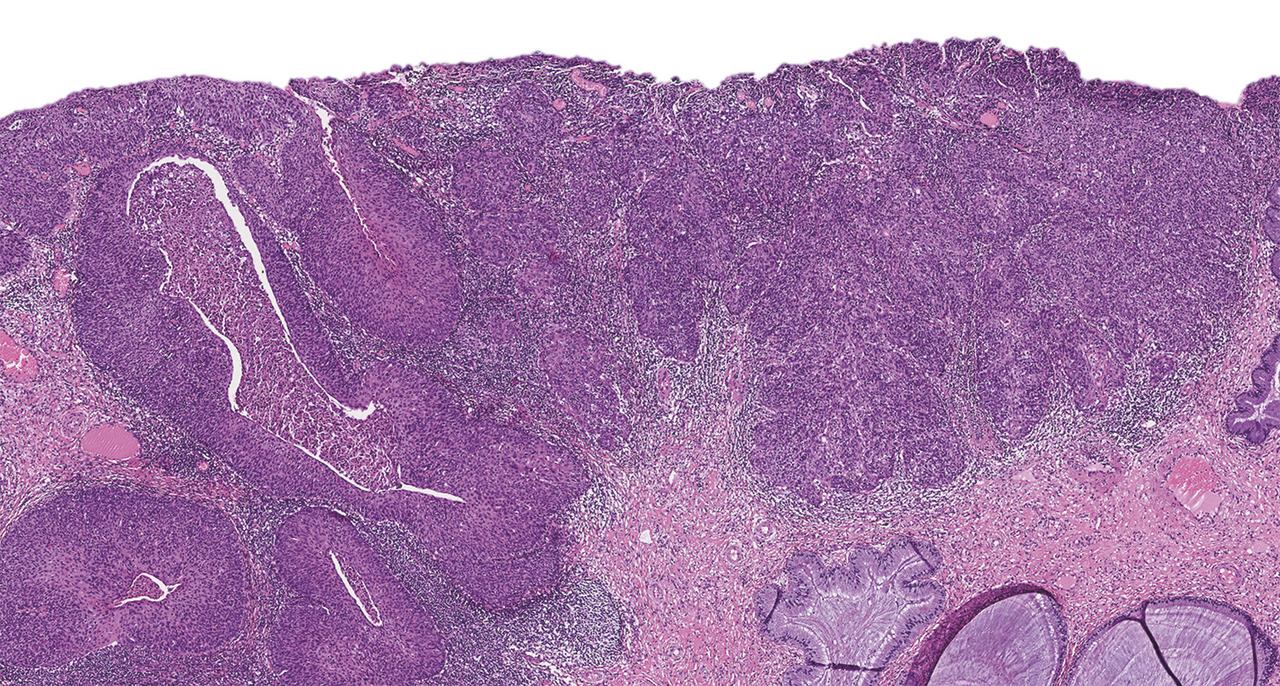
Le cancer du col utérin peut être évité. En effet, d’une part il s’agit d’un cancer viro-induit pour lequel il existe des vaccins prophylactiques efficaces, et d’autre part ce cancer est marqué par l’existence de lésions précancéreuses pendant une longue durée dont le dépistage permet un traitement peu morbide qui évite l’évolution vers le cancer.
En Australie et en Nouvelle-Zélande près de 80 % des jeunes filles sont vaccinées contre les papillomavirus humains depuis 2007-2008. Forts de cette excellente couverture, ces pays ont allégé les procédures de dépistage. Une modélisation leur permet même d’envisager grâce à l’efficacité du nouveau vaccin nonavalent, la disparition quasi complète du cancer du col de l’utérus à l’horizon 2034.1 Dans ces pays, l’organisation à la fois du dépistage et de la vaccination met totalement à profit la complémentarité entre les deux stratégies de prévention.
En France, la couverture vaccinale est très faible. Les données calculées sur « l’échantillon généraliste des bénéficiaires » et mises à jour au 31 décembre 2018 par Santé publique France révèlent une couverture vaccinale de 23,7 % des jeunes filles de 16 ans ayant reçu un schéma complet. Il existe de surcroît une hétérogénéité entre les différentes régions avec des taux nettement plus faibles dans le sud de la France. Notons par ailleurs qu’actuellement même les femmes vaccinées devront être dépistées en raison des cancers induits par les types non couverts par les vaccins actuels (environ 10 à 30 % des cancers du col selon le vaccin utilisé) ou les cancers dus aux infections virales survenues avant la vaccination.
En Australie et en Nouvelle-Zélande près de 80 % des jeunes filles sont vaccinées contre les papillomavirus humains depuis 2007-2008. Forts de cette excellente couverture, ces pays ont allégé les procédures de dépistage. Une modélisation leur permet même d’envisager grâce à l’efficacité du nouveau vaccin nonavalent, la disparition quasi complète du cancer du col de l’utérus à l’horizon 2034.1 Dans ces pays, l’organisation à la fois du dépistage et de la vaccination met totalement à profit la complémentarité entre les deux stratégies de prévention.
En France, la couverture vaccinale est très faible. Les données calculées sur « l’échantillon généraliste des bénéficiaires » et mises à jour au 31 décembre 2018 par Santé publique France révèlent une couverture vaccinale de 23,7 % des jeunes filles de 16 ans ayant reçu un schéma complet. Il existe de surcroît une hétérogénéité entre les différentes régions avec des taux nettement plus faibles dans le sud de la France. Notons par ailleurs qu’actuellement même les femmes vaccinées devront être dépistées en raison des cancers induits par les types non couverts par les vaccins actuels (environ 10 à 30 % des cancers du col selon le vaccin utilisé) ou les cancers dus aux infections virales survenues avant la vaccination.
Quels arguments pour la poursuite du dépistage ?
Les données épidémiologiques françaises fournissent le principal argument pour la poursuite du dépistage. Actuellement on estime le nombre de nouveaux cas de cancers invasifs du col de l’utérus à 3 000 et celui des décès à 1 000. Il s’agit de la deuxième cause de mortalité par cancer chez les femmes de moins de 45 ans.2 La diminution régulière de l’incidence et de la mortalité du cancer du col ralentit depuis quelques années en France. Ce ralentissement est observé depuis 2005 avec une diminution sur la période récente 2010-2018 qui n’est plus que de -0,7 % par an, voire encore moins chez les femmes de moins de 50 ans.
Parallèlement on constate en France, comme dans de nombreux autres pays, une augmentation de l’incidence des lésions précancéreuses.3 L’exposition des femmes à un risque accru d’infections liées aux papillomavirus du fait de l’évolution des comportements sexuels pourrait en être la cause.
Parallèlement on constate en France, comme dans de nombreux autres pays, une augmentation de l’incidence des lésions précancéreuses.3 L’exposition des femmes à un risque accru d’infections liées aux papillomavirus du fait de l’évolution des comportements sexuels pourrait en être la cause.
Selon quelles modalités ce dépistage doit-il continuer ?
L’outil de dépistage doit obéir à un certain nombre d’impératifs : innocuité totale, réalisation simple et reproductible, faible coût et fiabilité en termes de sensibilité, de spécificité et de valeurs prédictives. La sensibilité d’un test est fondamentale en cancérologie afin de limiter les faux négatifs du test potentiellement graves pour un individu, mais à l’inverse la spécificité est requise pour un dépistage de masse afin d’éviter les explorations diagnostiques dispendieuses et anxiogènes, voire les sur-traitements en cas de test faussement positif.
Généraliser le dépistage organisé
L’absence de dépistage constitue le facteur de risque majeur de cancer du col de l’utérus dans l’ensemble des pays développés. L’absence ou l’insuffisance de dépistage est le plus souvent observée chez les femmes de plus de 50 ans ou issues de milieux socio-économiques défavorisés.4 Les experts de l’Organisation mondiale de la santé et du Centre international de recherche sur le cancer s’accordent pour dire que le meilleur remède est l’organisation avec un système d’invitation des femmes. L’arrêté du 4 mai 2018 prévoit la généralisation à l’échelle nationale du dépistage organisé du cancer du col de l'utérus en France. Sa mise en œuvre est fondée sur un système d’invitations et de relances des femmes n’ayant pas participé spontanément au dépistage dans les trois dernières années, un suivi de l’ensemble des femmes dont le test de dépistage est positif (qu’elles aient participé spontanément ou qu’elles aient été invitées par courrier à participer au dépistage). L’analyse du frottis est prise en charge à 100 %, c’est-à-dire gratuite, pour les femmes invitées. La généralisation du dépistage organisé à l’échelle nationale a pour objectif d’atteindre un taux de couverture dans la population cible de 80 %, tout en facilitant l’accès au dépistage des populations vulnérables ou les plus éloignées du système de santé. Notons que cet objectif a été atteint dans une campagne pilote menée en Alsace5 qui réduit le nombre de cancers diagnostiqués et de décès liés à ces cancers de 16,1 % et 19,5 % respectivement par rapport au dépistage individuel avec un coût annuel de 1,05 € par femme à dépister soit 22 700 € par année de vie sauvée.3, 6
Frottis ou test HPV ?
Actuellement le dépistage repose sur la réalisation périodique du frottis cervical. Les recommandations françaises confirmées en 2010 par la Haute Autorité de santé (HAS) préconisent un dépistage par frottis cervical chez toutes les femmes ayant eu des rapports sexuels, à partir de 25 ans et jusqu’à 65 ans.7
Certains réclament dès ce stade le remplacement du frottis par la recherche du génome des papillomavirus oncogènes (test HPV) dont la sensibilité pour le dépistage primaire des lésions précancéreuses et cancéreuses du col de l’utérus est significativement supérieure, bien que la spécificité soit significativement plus faible. Le test HPV tous les 5 ans est, selon la modélisation mathématique menée sous l’égide de l’Institut national du cancer,8 la méthode de dépistage ayant le meilleur rapport coût-efficacité. À la demande de la Direction générale de la santé, la HAS a inscrit à son programme de travail une évaluation de la place de la recherche des papillomavirus en dépistage primaire des lésions précancéreuses et cancéreuses du col de l’utérus et du double marquage immuno-histochimique (p16/Ki67). De nouveaux algorithmes de prises en charge des femmes positives au test HPV devraient y être définis. Leur mise en œuvre aura pour objectif de contribuer à la réduction des sur-diagnostics et des surtraitements liés à la moins bonne spécificité de ce test de dépistage. Dans le cadre de l’organisation qui se met parallèlement en place, les centres régionaux du dépistage organisé du cancer du col de l’utérus devront être en capacité d’aider les professionnels de santé à promouvoir cette mise en œuvre conformément aux recommandations. Compte tenu de la spécificité plus faible du test HPV par rapport au frottis, nous sommes persuadés que la mise en place d’une organisation efficace reste un préalable indispensable. À ce jour, dans tous les pays à forte couverture vaccinale (Pays-Bas, Australie, Nouvelle Zélande…), le test HPV a été introduit dans un contexte d’organisation du dépistage déjà ancienne et pleinement effective.
Certains réclament dès ce stade le remplacement du frottis par la recherche du génome des papillomavirus oncogènes (test HPV) dont la sensibilité pour le dépistage primaire des lésions précancéreuses et cancéreuses du col de l’utérus est significativement supérieure, bien que la spécificité soit significativement plus faible. Le test HPV tous les 5 ans est, selon la modélisation mathématique menée sous l’égide de l’Institut national du cancer,8 la méthode de dépistage ayant le meilleur rapport coût-efficacité. À la demande de la Direction générale de la santé, la HAS a inscrit à son programme de travail une évaluation de la place de la recherche des papillomavirus en dépistage primaire des lésions précancéreuses et cancéreuses du col de l’utérus et du double marquage immuno-histochimique (p16/Ki67). De nouveaux algorithmes de prises en charge des femmes positives au test HPV devraient y être définis. Leur mise en œuvre aura pour objectif de contribuer à la réduction des sur-diagnostics et des surtraitements liés à la moins bonne spécificité de ce test de dépistage. Dans le cadre de l’organisation qui se met parallèlement en place, les centres régionaux du dépistage organisé du cancer du col de l’utérus devront être en capacité d’aider les professionnels de santé à promouvoir cette mise en œuvre conformément aux recommandations. Compte tenu de la spécificité plus faible du test HPV par rapport au frottis, nous sommes persuadés que la mise en place d’une organisation efficace reste un préalable indispensable. À ce jour, dans tous les pays à forte couverture vaccinale (Pays-Bas, Australie, Nouvelle Zélande…), le test HPV a été introduit dans un contexte d’organisation du dépistage déjà ancienne et pleinement effective.
Ne pas baisser la garde
Le dépistage organisé, qui assure à la fois une sécurité augmentée une meilleure équité pour les patientes et une baisse des coûts pour la société, est une aide précieuse pour les professionnels de santé dans la prise en charge recommandée des anomalies. Cette organisation est un préalable à un éventuel dépistage par le test HPV qui requiert des procédures de triage indispensables. En France, la couverture vaccinale est dramatiquement faible et ne permet à ce stade ni de modifier la stratégie de dépistage ni d’espérer la disparition du cancer du col de l’utérus. Le dépistage doit continuer !
Références
1. Hall MT, Simms KT, Lew JB, et al. The projected timeframe until cervical cancer elimination in Australia: a modelling study. Lancet Public Health 2019;4:e19-e27.
2. Institut national du cancer. Épidémiologie du cancer du col de l'utérus en France métropolitaine. Données essentielles, INCa septembre 2012. www.e-cancer.fr
3. Woronoff AS, Trétarre B, Champenois V, Duport N, Bara S, Lapôtre-Ledoux B. Surveillance des lésions précancéreuses et cancéreuses du col de l’utérus par les registres des cancers du réseau Francim. Bull Epidemiol Hebd 2014;13-14-15:234-40.
4. Duport N, Serra D, Goulard H, Bloch J. Quels facteurs influencent la pratique du dépistage des cancers féminins en France ? Rev Epidemiol Sante Publique 2008;56: 303-13.
5. Baldauf JJ, Fender M, Bergeron C, et al. Cervical morbidity in Alsace, France: results from a regional organized cervical cancer screening program. Eur J Cancer Prev 2019;28:33-9.
6. Levy-Bruhl D, Kudjawu Y, Dervaux B, Lehne X. Modélisation médico-économique de l’impact de l’organisation du dépistage du cancer du col utérin et de l’introduction de la vaccination contre les HPV dans le calendrier vaccinal (synthèse). Rapport Institut de veille sanitaire, mars 2007.
7. Haute Autorité de santé. Recommandations en santé publique : état des lieux et recommandations pour le dépistage du cancer du col de l’utérus en France. Paris : HAS, 2010:1-256.
8. Barré S, Massetti M, Leleu H, De Bels F. Organised screening for cervical cancer in France: a cost-effectiveness assessment. BMJ Open 2017;7:e014626.
2. Institut national du cancer. Épidémiologie du cancer du col de l'utérus en France métropolitaine. Données essentielles, INCa septembre 2012. www.e-cancer.fr
3. Woronoff AS, Trétarre B, Champenois V, Duport N, Bara S, Lapôtre-Ledoux B. Surveillance des lésions précancéreuses et cancéreuses du col de l’utérus par les registres des cancers du réseau Francim. Bull Epidemiol Hebd 2014;13-14-15:234-40.
4. Duport N, Serra D, Goulard H, Bloch J. Quels facteurs influencent la pratique du dépistage des cancers féminins en France ? Rev Epidemiol Sante Publique 2008;56: 303-13.
5. Baldauf JJ, Fender M, Bergeron C, et al. Cervical morbidity in Alsace, France: results from a regional organized cervical cancer screening program. Eur J Cancer Prev 2019;28:33-9.
6. Levy-Bruhl D, Kudjawu Y, Dervaux B, Lehne X. Modélisation médico-économique de l’impact de l’organisation du dépistage du cancer du col utérin et de l’introduction de la vaccination contre les HPV dans le calendrier vaccinal (synthèse). Rapport Institut de veille sanitaire, mars 2007.
7. Haute Autorité de santé. Recommandations en santé publique : état des lieux et recommandations pour le dépistage du cancer du col de l’utérus en France. Paris : HAS, 2010:1-256.
8. Barré S, Massetti M, Leleu H, De Bels F. Organised screening for cervical cancer in France: a cost-effectiveness assessment. BMJ Open 2017;7:e014626.