Le système de santé français fait actuellement l’objet d’une modification en profondeur vers la prise en charge des maladies chroniques. Auparavant, l’objectif était de traiter une pathologie aiguë et de la guérir définitivement. Aujourd’hui, il faut suivre les patients pendant de longues années, avec un fardeau de complications qui s’alourdit. La maladie rénale chronique (MRC) peut servir de modèle d’évolution de l’organisation des soins.1 Elle se caractérise par sa durée – parfois plus de vingt ans –, sa simplicité aux stades initiaux, puis sa complexité aux stades avancés. Agir tôt sur la MRC, c’est garantir une meilleure survie mais aussi améliorer l’espérance de vie en bonne santé. En effet, ayons en tête que la survie en dialyse est comparable à celle du cancer du côlon métastatique, que l’espérance de vie d’une femme de 65 ans au stade 5 de la MRC est de six ans versus vingt-deux ans dans la population générale, avec « les dernières années en dialyse » caractérisées par une détérioration profonde de la qualité de vie.2
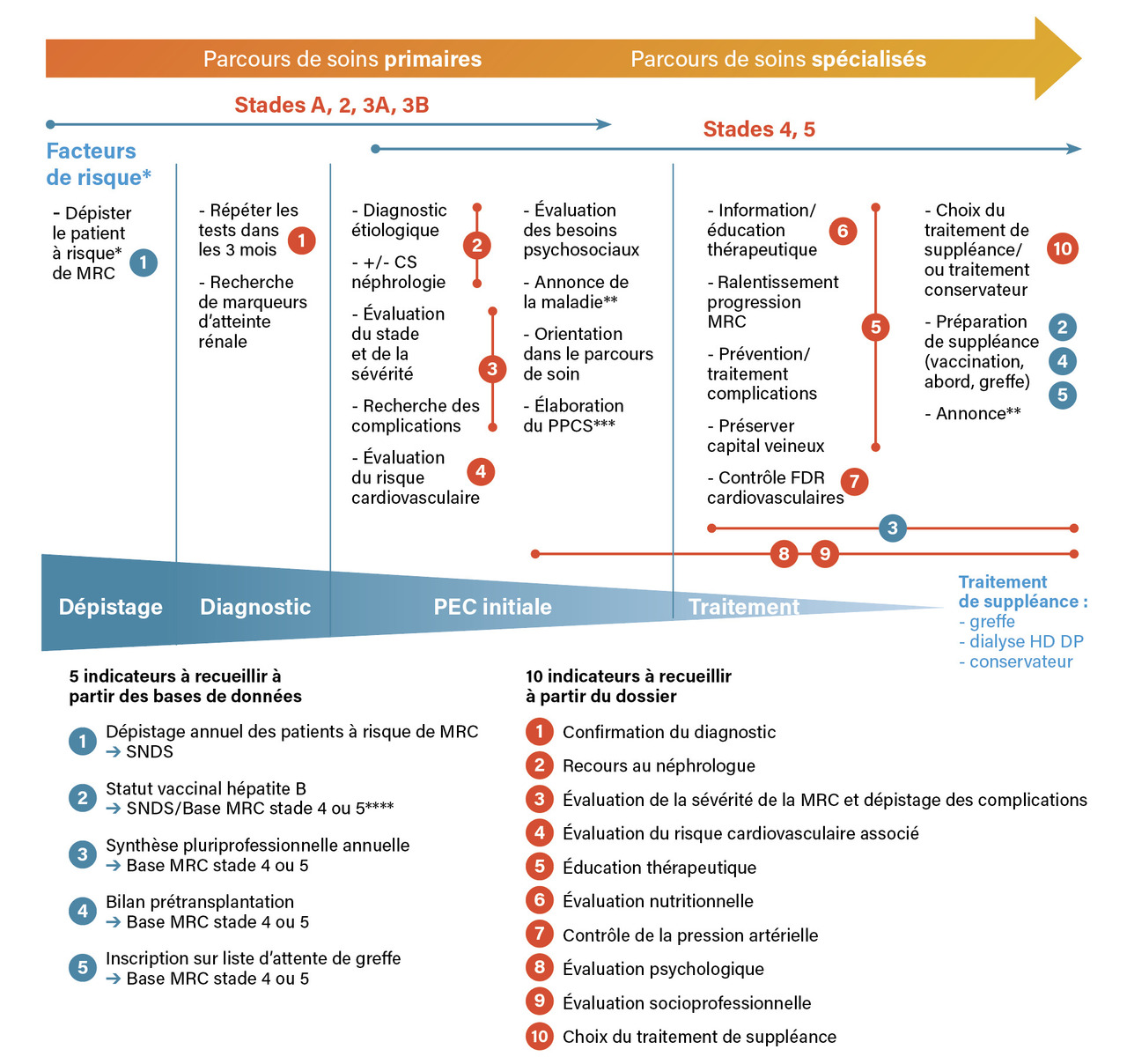
Pour être efficace, il faut passer d’une organisation avec des temps d’intervention très courts (consultation), sans suivi intercurrent, à un parcours de soins balisé et coordonné dans la durée, mobilisant les ressources motivationnelles des patients. La figure est issue des recommandations de la Haute Autorité de santé (HAS) 2021.3 Le parcours de soins primaires de la MRC aux stades 1, 2 et 3A ou pour les formes stables se déroule en médecine de ville. Il est coordonné par le médecin généraliste. Il comporte le temps du dépistage. Pour agir tôt, il faut y penser systématiquement. On peut s’appuyer sur des algorithmes d’aide à la prescription. Une façon positive de réaliser annuellement le dépistage des populations à risque consiste à mobiliser l’attention du patient. Par exemple, chez un diabétique, pourquoi ne pas lui dire « Vous prendrez soin de vos yeux et… de vos reins » ? Une fois par an, la recherche d’une rétinopathie diabétique et… le contrôle du débit de filtration glomérulaire estimé (DFGe) et du ratio albuminurie/créatininurie (RAC). Compte tenu de la pénurie en médecine de ville, il faut organiser des alternatives : conseils du pharmacien ou du biologiste, consultation avec une infirmière en pratique avancée (IPA), mobilisation des centres de médecine préventive, invitation par l’Assurance maladie à réaliser le dépistage annuel, comme pour le cancer du côlon…4,5 Sur un territoire donné, l’approche populationnelle6 coordonne le parcours MRC des nombreux patients qui sont « sous nos yeux », entre l’appareil administratif (mairie…), les maisons de santé pluriprofessionnelles (MSP), les communautés professionnelles territoriales de santé (CPTS), les structures de néphrologie… Pour garantir son efficacité, le parcours de soins doit être connu de tous les acteurs, et pourquoi pas matérialisé par une charte ?
Une fois la MRC dépistée, il faut aller jusqu’au diagnostic. En effet, cette étape ne doit pas être shuntée ; car il existe des avancées significatives des traitements étiologiques offrant le contrôle complet de certaines pathologies. Toutefois, si, comme cela est généralement le cas, la MRC évolue dans un contexte de diabète, de maladie cardiovasculaire hypertensive ou d’obésité, tout se joue au stade 3 de la MRC. La médecine de ville doit se donner les moyens d’appliquer les recommandations (figure) : annonce de la maladie, recherche des complications, évaluation du risque cardiovasculaire, évaluation des besoins psychosociaux. Après cela, il faut positionner le patient dans son parcours de soins en établissant un plan personnalisé de coordination en santé, centré sur les acteurs de santé du lieu de vie du patient. Il doit bénéficier d’un programme éducatif performant de protection cardiovasculaire et rénale dont la véracité et l’authenticité sont garanties. Attention à la désinformation sur les réseaux sociaux !7
L’action en médecine de ville est cruciale pour gagner en espérance de vie en bonne santé. En effet, les actions de prévention secondaire doivent permettre d’éviter la progression de la MRC vers les stades 4 et 5. La mise en place de mesures de néphroprotection est déterminante tant du point de vue de l’hygiène de vie que de la prescription des nouvelles molécules. La prise en charge du patient est d’autant plus commode qu’il y a une concordance des objectifs entre la médecine de ville, la cardiologie, la diabétologie et la néphrologie. L’orientation du patient dans le parcours de soins de la MRC est fonction de l’étiologie, du stade et de son pronostic ainsi que de l’âge et de la présence de complications. L’indicateur central dans la prise en charge du patient est la pente de décroissance du DFG.1 Il faut la partager avec le patient et tous les acteurs du parcours. Il faut donc exiger de son biologiste référent une figure dans les résultats biologiques matérialisant cette pente comme celle de l’HbA1c.
Aux stades 4 et 5 ou dans le cas d’une progression de la MRC avec perte de DFG de plus de 3 mL/min/1,73 m2 par an induisant un risque d’évolution vers l’insuffisance rénale chronique terminale (IRCT), la prise en charge se complexifie. Elle est spécialisée, coordonnée par le néphrologue et fait l’objet d’une facturation forfaitaire à l’Assurance maladie dite « forfait MRC ».8 En plus de la consultation de néphrologie, celui-ci comporte l’intervention d’un(e) infirmier(ère) de parcours et une prise en charge diététique. Aujourd’hui remboursée, la télésurveillance trouve toute sa justification. La place de l’éducation thérapeutique ciblée MRC se renforce.
Dans les objectifs du forfait, la néphroprotection reste prioritaire ; car les relevés d’activité conduisent au constat qu’une majorité de patients au stade 4 ne progressent pas, ce qui est la preuve de l’efficacité des actions mises en place. Cependant, lorsque l’évolution vers l’IRCT est anticipée dans les deux ans, la prise en charge engage le patient dans une démarche de décision partagée du choix de traitement de suppléance (greffe ou dialyse) ou du traitement conservateur (figure) ;9 puis, selon le choix retenu, la préparation débute. À partir du seuil de DFG de 20 mL/min/1,73 m2, en l’absence de contre-indication, il faut présenter prioritairement la greffe, puis la dialyse. En effet, les recommandations de la HAS d’accès à la liste d’attente de transplantation rénale fixent comme indicateur de qualité une inscription avant le démarrage de la dialyse. La dialyse autonome ou à domicile (dialyse péritonéale) doit être priorisée ; car elle garantit une meilleure qualité de vie. Il faut souligner que le démarrage de la dialyse est fondé sur les symptômes témoignant de la mauvaise tolérance de la MRC. Dire au patient que « le meilleur indicateur pour le moment où il faut débuter la dialyse, c’est lui » et non sur des valeurs numériques de DFG, de potassium, de phosphates…
Depuis une publication de la Société francophone de néphrologie, dialyse et transplantation (SFNDT) en 2022,10 le traitement conservateur, encore appelé « prise en charge de la MRC au stade 5 sans dialyse envisagée », est une option thérapeutique au même titre que la greffe ou la dialyse. Elle doit être proposée à tous les patients, notamment ceux âgés de plus de 75 ans : « La dialyse, ce n’est pas automatique ! » Il s’agit d’une prise en charge active qui maintient le plus longtemps possible toutes les actions thérapeutiques sans recourir à la dialyse dont les bénéfices sont inférieurs au fardeau qu’elle induit sur la qualité de vie. Comme aux stades initiaux de la MRC, la réussite du programme « forfait MRC » nécessite une organisation efficace sur le lieu de vie du patient. Le partenariat ville-hôpital est indispensable, en particulier avec les infirmiers(ères), le médecin généraliste, l’hospitalisation à domicile…8,11
Finalement, mettre sur pied une architecture du parcours MRC sur un territoire assure des résultats positifs, pour le patient comme pour la santé publique. La HAS propose une dizaine d’indicateurs (figure) dont l’appropriation collective aide sur le chemin de la réussite collective.
Cet article fait partie d'un supplément ayant bénéficié du soutien strictement institutionnel du laboratoire AstraZeneca , sans intervention de leur part dans l’élaboration du sommaire, le choix des auteurs et la rédaction des articles.
2. Cremades A, Moranne O, Couchoud C. Trajectoires des patients en suppléance. Nephrol Ther 2022;18(S2):21-4.
3. HAS. Parcours du patient adulte présentant une maladie rénale chronique. Définition des indicateurs de qualité du parcours de soins. Septembre 2021. https://www.has-sante.fr/jcms/p_3288950/fr/guide-du-parcours-de-soins-maladie-renale-chronique-de-l-adulte-mrc
4. Belaiche S, Mercier E, Cuny D, Kambia N, Wierre P, Bertoux E, et al. Implication du pharmacien d’officine dans le parcours de soins de la maladie rénale chronique. Nephrol Ther 2017;13:87-92.
5. Pagidipati NJ, Nelson AJ, Kaltenbach LA, Leyva M, McGuire DK, Pop-Busui R, et al. Coordinated care to optimize cardiovascular preventive therapies in type 2 diabetes. A randomized clinical trial. JAMA 2023;329:1261-70.
6. https://www.fhf.fr/la-fhf-en-action-responsabilite-populationnelle-tous-acteurs-de-notre-sante
7. https://www.fondationdescartes.org/2023/10/information-et-sante/
8. Raffray M, Campéon A, Bricard D, Augé E, Raynaud D, Couchoud C et al. Incentivize and implement multidisciplinary care for chronic kidney disease: what can we learn from the french CKD capitation payment program? Soumis.
9. Hamroun A, Glowacki F, Frimat L. Comprehensive conservative care: what doctors say, what patients hear. Nephrol Dial Transplant 2023;38:2428-43.
10. Groupe de travail de la SFNDT. Traitement conservateur de la maladie rénale chronique stade 5 : guide pratique. Nephrol Ther 2022;18:155-71.
11. Devictor B, Cremades A, Izaaryene G, Mazoue F, Brunet P, Gentile S. Accès géographique à l’hémodialyse : une analyse sur le choix des patients. Nephrol Ther 2024;20:1-13.
En collaboration avec :