En 2000, l’Organisation mondiale de la santé définit un perturbateur endocrinien « comme une substance exogène ou un mélange qui altère les fonctions du système endocrinien et qui, par conséquent, cause des effets délétères à un organisme intact, sa progéniture ou des (sous)-populations ». Plus de 100 000 produits chimiques différents nous entourent, et parmi eux environ 1 000 sont considérés comme de possibles perturbateurs endocriniens. Ces substances ont pourtant permis de nombreux progrès concernant la qualité de nos vies. Le bisphénol A,utilisé comme film isolant à l’intérieur des boîtes de conserve, évite le contact des aliments avec le métal, source d’altération de ceux-ci. Les phtalates, donnant de la souplesse aux plastiques, ont permis de générer de multiples objets utiles à notre quotidien. La question se pose donc : que faire ? les remplacer ? mais par quelles autres substances, souvent encore insuffisamment étudiées ? ou s’en priver et retourner à la situation d’« avant » ?
Quelles sont les conséquences de la présence de certaines substances dans l’environnement ?
C’est en 1962 que survient la première alarme, quand Rachel Carson signale, dans plusieurs régions des États-Unis, la disparition d’oiseaux et un taux élevé de pesticides dans les sols et rivières. L’auteur, inquiète, parle alors d’un « volcan assoupi » ! Ultérieurement, dans de nombreuses zones côtières,on note des anomalies des organes génitaux d’animaux marins, et on met en cause le tributylétain utilisé dans les peintures pour coques de bateau : ce produit est anti-estrogénique. En Floride, le lac Apopka est contaminé par des polluants, dont du DDT ; 3 ans plus tard, on note le déclin des alligators : femelles avec malformations ovariennes et micropénis chez les mâles. Parallèlement,dans les eaux polluées issues d’usines à pâte à papier ou sortant de stations d’épuration, on note des troubles divers de différenciation sexuelle chez les poissons. Toutes les atteintes répertoriées concernent alors le système reproducteur des animaux. Un lien est ainsi établi entre la présence de certains produits chimiques et des effets sur le vivant.1
Alerte chez l’homme
Dans les années 1970, du diéthylstilbestrol (DES ; Distilbène) est prescrit à des femmes enceintes en vue de prévenir des fausses couches. En 1971, un lien est fait entre la prise de ce médicament par la mère pendant la grossesse et la survenue d’un nombre inhabituel de cancers du tractus génital, utérus, trompes,vagin chez les filles de ces femmes, âgées de 15 à 22 ans. Ultérieurement, des problèmes seront trouvés chez les enfants, et même chez les petits-enfants des femmes atteintes.1,2
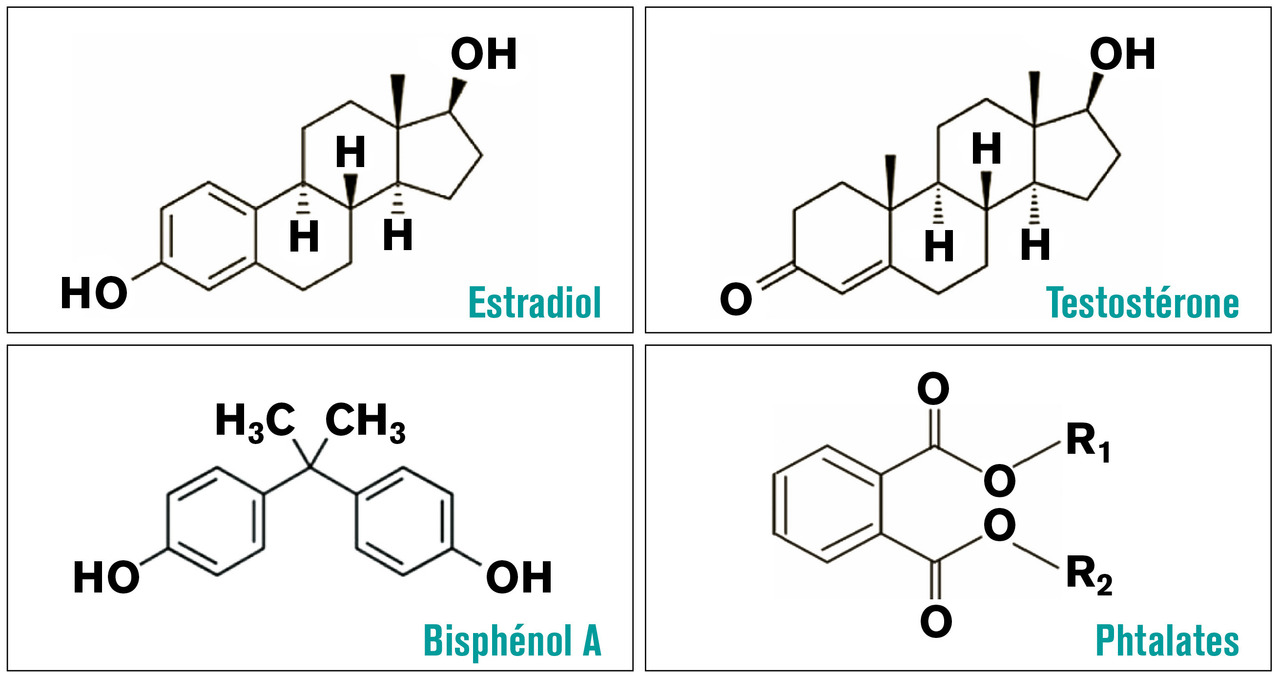
D’autres substances sont suspectées comme la chlordécone, utilisée contre le charançon et incriminée chez les travailleurs impliqués dans sa fabrication : troubles neurologiques, oligospermie, atteintes des spermatozoïdes ; ce produit a une activité estrogénique. On évoque alors, à l’instar de ce qui a été vu chez les animaux, la possibilité que ces anomalies touchant les systèmes reproducteurs masculin et féminin puissent être en lien avec la structure chimique de substances proches de celle des hormones masculine (testostérone) ou féminine (estradiol), et interférant avec leurs récepteurs. Il existe de multiples sources de perturbateurs endocriniens, certains d’entre eux peuvent provenir de produits manufacturés ou d’aliments d’origine végétale ou animale. Ils sont cependant, pour la plupart, issus de l’industrie agro-chimique (pesticides, plastiques, pharmacie) et de leurs rejets. Beaucoup sont rémanents, pouvant persister de longues années dans l’environnement.
D’autres substances sont suspectées comme la chlordécone, utilisée contre le charançon et incriminée chez les travailleurs impliqués dans sa fabrication : troubles neurologiques, oligospermie, atteintes des spermatozoïdes ; ce produit a une activité estrogénique. On évoque alors, à l’instar de ce qui a été vu chez les animaux, la possibilité que ces anomalies touchant les systèmes reproducteurs masculin et féminin puissent être en lien avec la structure chimique de substances proches de celle des hormones masculine (testostérone) ou féminine (estradiol), et interférant avec leurs récepteurs. Il existe de multiples sources de perturbateurs endocriniens, certains d’entre eux peuvent provenir de produits manufacturés ou d’aliments d’origine végétale ou animale. Ils sont cependant, pour la plupart, issus de l’industrie agro-chimique (pesticides, plastiques, pharmacie) et de leurs rejets. Beaucoup sont rémanents, pouvant persister de longues années dans l’environnement.
Mécanismes d’action des perturbateurs endocriniens
Ces molécules interfèrent du fait de leur proximité structurale avec les hormones sexuelles (fig. 1 ). Plusieurs mécanismes d’action sont définis :3
– les perturbateurs agonistes miment l’action d’une hormone naturelle en se liant au récepteur et en l’activant. Son action est inférieure à celle de l’hormone naturelle;
– les perturbateurs antagonistes se fixent au récepteur et bloquent la réponse de l’hormone naturelle. Par exemple, le DDE, principal métabolite du dichlorodiphényltrichloroéthane (DDT), est un antagoniste des récepteurs aux androgènes ;
– d’autres ont des effets perturbant la production ou le transport hormonal ;
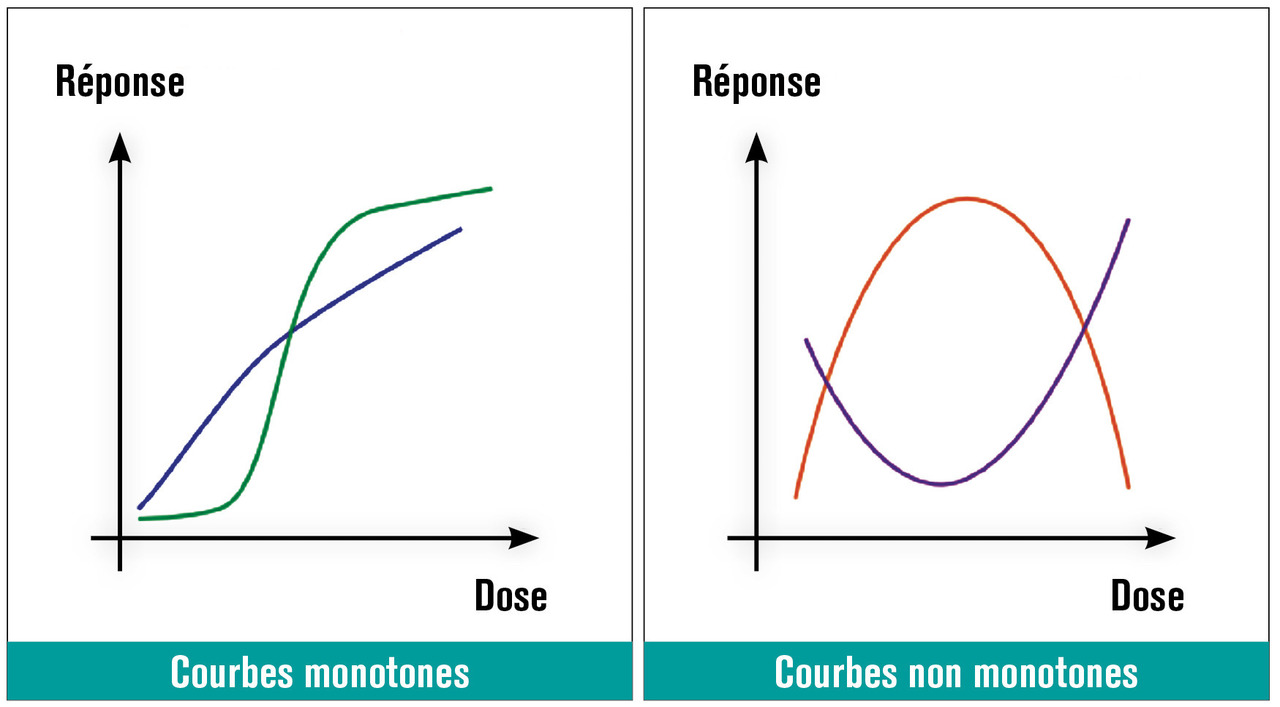
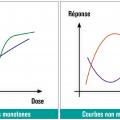
– l’épigénétique a aussi une place, avec la possibilité de modification de la méthylation des gènes, de modification des histones et de la production des micro-ARN. La transmission de ces anomalies aux générations ultérieures est possible. Ainsi, ces substances induisent des effets néfastes, propres à chacune : principalement l’altération des fonctions de reproduction, la malformation des organes reproducteurs, le développement de tumeurs au niveau des tissus producteurs ou cibles des hormones (sein, prostate, testicule, utérus...), et au niveau de la thyroïde. La toxicité des substances est considérée comme fonction de la dose ; ainsi ont été précisées des doses à ne pas dépasser, risquant d’entraîner des troubles. La notion de seuil toxique est importante, car elle sert à fixer des normes d’utilisation. La valeur seuil représente la quantité minimale sous laquelle il ne se produit pas d’effet. Toutes ces données sont fixées après études sur divers modèles animaux. Des données récentes laissent entendre que les effets des perturbateurs endocriniens pourraient apparaître à des doses très faibles ne paraissant pas dangereuses selon les lois de la toxicité classique fondées sur la relation dose-effet.4 Les courbes dose-réponse sont donc soit monotones, soit non monotones (fig. 2 ).Cela fait suggérer l’existence d’autres mécanismes en cause en cours d’évaluation.
– les perturbateurs agonistes miment l’action d’une hormone naturelle en se liant au récepteur et en l’activant. Son action est inférieure à celle de l’hormone naturelle;
– les perturbateurs antagonistes se fixent au récepteur et bloquent la réponse de l’hormone naturelle. Par exemple, le DDE, principal métabolite du dichlorodiphényltrichloroéthane (DDT), est un antagoniste des récepteurs aux androgènes ;
– d’autres ont des effets perturbant la production ou le transport hormonal ;
– l’épigénétique a aussi une place, avec la possibilité de modification de la méthylation des gènes, de modification des histones et de la production des micro-ARN. La transmission de ces anomalies aux générations ultérieures est possible. Ainsi, ces substances induisent des effets néfastes, propres à chacune : principalement l’altération des fonctions de reproduction, la malformation des organes reproducteurs, le développement de tumeurs au niveau des tissus producteurs ou cibles des hormones (sein, prostate, testicule, utérus...), et au niveau de la thyroïde. La toxicité des substances est considérée comme fonction de la dose ; ainsi ont été précisées des doses à ne pas dépasser, risquant d’entraîner des troubles. La notion de seuil toxique est importante, car elle sert à fixer des normes d’utilisation. La valeur seuil représente la quantité minimale sous laquelle il ne se produit pas d’effet. Toutes ces données sont fixées après études sur divers modèles animaux. Des données récentes laissent entendre que les effets des perturbateurs endocriniens pourraient apparaître à des doses très faibles ne paraissant pas dangereuses selon les lois de la toxicité classique fondées sur la relation dose-effet.4 Les courbes dose-réponse sont donc soit monotones, soit non monotones (
Difficultés rencontrées dans l’étude des effets des perturbateurs endocriniens
Leur activité dépend de multiples facteurs plus ou moins intriqués, comme les fenêtres d’exposition : prénatale, périnatale, pubertaire ; les voies d’exposition : orale, cutanée, aérienne ; l’effet « cocktail », la durée d’exposition, etc.
Nature des perturbateurs endocriniens environnementaux, chimiques ou naturels
Voir le tableau p. 437 .
Quels effets sur le système reproducteur ?
Les perturbateurs endocriniens ont des effets délétères sur le système reproducteur chez les garçons et chez les filles.1,3, 5-8
Dans le sexe masculin
Diminution du nombre de spermatozoïdes
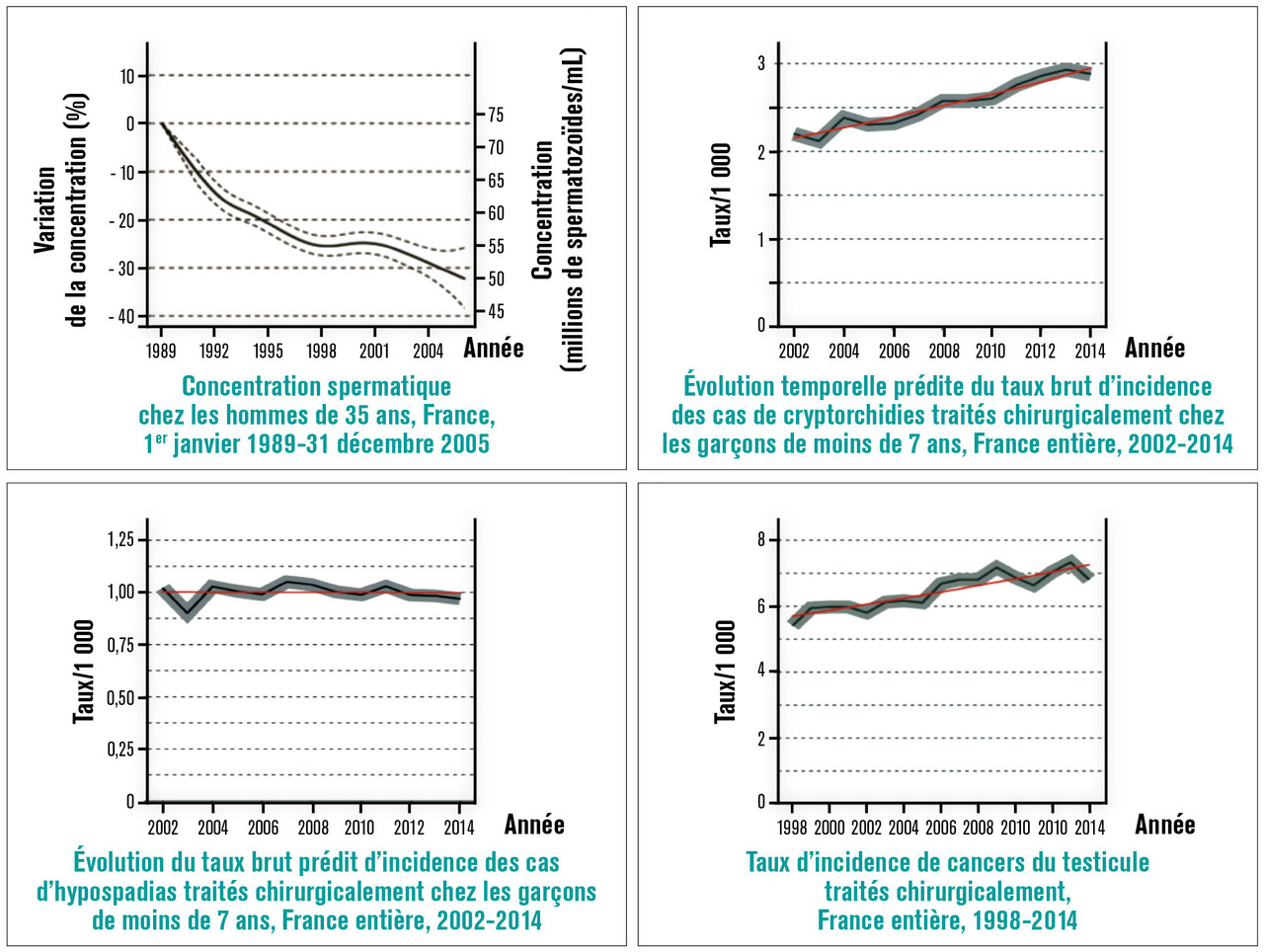
Cette diminution a été notée chez des pilotes d’avion d’épandage. Une méta-analyse de 61 études publiées entre 1940 et 1990 a montré une diminution du nombre de spermatozoïdes, passant de 113 millions/mL en 1940 à 66 millions/mL en1990.Une étude danoise conduite entre 1950 et 1992 a montré une diminution globale du nombre de spermatozoïdes d’environ 2 % par an sur les années étudiées.Diminution du sex-ratio homme-femme
Ce rapport est passé de 1,053 à 1,049 aux États-Unis de 1969 à 1995.Cryptorchidies
Des dérivés organochlorés (DTT, polychlorobiphényles [PCB], pesticides, insecticides, fongicides) en concentration plus élevée ont été trouvés chez des nourrissons cryptorchides par rapport aux témoins.Cancer du testicule
Depuis 1940,la fréquence des cancers du testicule chez l’adulte de type caucasien a été multipliée par 3 à 4. Or la cryptorchidie augmente le risque de ce cancer 3 à 5 fois.Le concept de syndrome de dysgénésie testiculaire a été proposé, associant plus ou moins 4 composants : hypo- spadias, cryptorchidie, oligospermie, cancer du testicule.9Malformations génitales
La fréquence des malformations génitales chez les garçons est plus élevée chez ceux vivant dans une zone agricole riche en pesticides ou dont les pères sont agriculteurs ou jardiniers. Des études récentes montrent une corrélation entre contamination fœtale aux pesticides et hypospadias, avec augmentation du risque relatif d’environ 1,4. Une étude concernant 995 nouveau-nés masculins a montré que 25 d’entre eux avaient des malformations génitales et que 8 de ces malformations survenaient chez des enfants d’agriculteurs ou vivant dans une zone à risque.3 Une publication récente du Bulletin épidémiologique hebdomadaire10 fait le point, en France, sur les données concernant les quatre composantes du syndrome de dysgénésie testiculaire. Pour ce faire, ils ont utilisé les données du PMSI et du Registre des fécondations in vitro de l’association Fivnat. Les résultats de ce travail reflètent une altération globale de la santé reproductive masculine en France, cohérente avec la littérature internationale. Ils sont compatibles avec des changements environnementaux ou de modes de vie, parmi lesquels l’exposition croissante aux perturbateurs endocriniens de la population générale. À ce stade, ils ne permettent pas d’argumenter un rôle éventuel d’expositions géographiquement déterminées. L’étude ne permet pas d’identifier le rôle spécifique de telle ou telle substance (Dans le sexe féminin
Avance de l’âge d’apparition des caractères sexuels
Dans de nombreux pays dont la France, l’incidence du développement prématuré et isolé des seins (thélarche prématurée), du développement prématuré isolé de la pilosité pubienne (pubarche prématurée) mais aussi de pubertés précoces vraies a augmenté.11-13 La fréquence des cas de puberté précoce centrale chez les enfants adoptés a également augmenté.14, 15 Une relation entre le contact avec le bisphénol A et des difficultés à la procréation médicalement assistée a été notée.Effets sur la production hormonale thyroïdienne
Les hormones thyroïdiennes semblent également voir leur activité modifiée par certains perturbateurs endocriniens. En pédiatrie, on connaît le rôle essentiel de ces hormones dans la constitution du cerveau de l’embryon et du fœtus, et l’on conçoit que toute perturbation à ce niveau puisse avoir des conséquences graves sur le développement de l’enfant. Or, dans notre environnement, un certain nombre de substances présentent des analogies structurales avec les hormones thyroïdiennes, qui comportent deux noyaux phénoliques substitués par un halogène, l’iode. Les retardateurs de flamme qui comporte un halogène, le brome, et le PCB font partie de ces substances (lePCB a été interdit il y a 40 ans, mais persiste encore dans l’environnement).Dans le lait maternel, quatre substances chimiques présentes ont montré des associations significatives avec la dysfonction thyroïdienne chez le nouveau-né, en particulier les composés de type dioxine, mais aussi le DDT. Par ailleurs, beaucoup d’équipes évoquent le rôle de perturbateurs endocriniens dans l’augmentation nette de l’incidence des hypothyroïdies congénitales dans le monde, secondaires à des anomalies de développement de la thyroïde, amenant à évoquer d’autres mécanismes portant sur le développement glandulaire. Enfin, la baisse de quelques points du quotient intellectuel n’a pas encore d’explication claire.16
Perturbateurs endocriniens : ce qui les accuse...
Les données épidémiologiques mettent en évidence une augmentation d’anomalies concernant le développement et le fonctionnement des organes reproducteurs, suggérant une perturbation des mécanismes hormonaux qui les sous-tendent. Ces anomalies, à l’instar de ce qui se passe chez les animaux, font évoquer le rôle des perturbateurs endocriniens environnementaux. Cependant, un lien direct avec une substance particulière n’est que rarement confirmé. Un effet « cocktail » est possible mais très difficile à apprécier. Il existe sans doute une sensibilité plus grande de certains sujets à ces produits. C’est pendant la grossesse ou en période néonatale que le risque semble maximum pour les enfants du fait d’une plus grande susceptibilité à ces produits durant cette période de la vie.
Perturbateurs fréquemment rencontrés
Dans les plastiques alimentaires
Les plastiques alimentaires sont fabriqués à partir de dérivés du pétrole, ils comportent des noyaux phénol, trouvés également dans certaines hormones. Ils sont constitués de très longues chaînes carbonées structurées de façons diverses, soit régulièrement organisées, soit enchevêtrées, soit réticulées, leur conférant des propriétés spécifiques. Ils sont classés en sept catégories, dont certaines contiennent du bisphénol A et/ou des phtalates.17
– sur la fonction reproductrice par diminution de la sécrétion d’estrogènes : anomalie de la commande hypothalamo-hypophysaire, avec des cycles longs et irréguliers chez la femelle et un risque de baisse de fertilité chez le mâle ;
– sur le développement du tissu cérébral et des fonctions cognitives, avec des troubles de l’apprentissage et de la mémoire chez les rongeurs et les singes ;
– sur le métabolisme : risque d’augmentation du diabète insulinodépendant de type 2 ;
– sur le développement de la glande mammaire, conduisant à une susceptibilité accrue aux substances cancérogènes. Au total, en 2017, l’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail (Anses) déclarait que « les données disponibles étayent la plausibilité que le BPA module les effets agonistes des estrogènes et des progestatifs et, par là, puissent augmenter la susceptibilité au cancer ». À noter que le mécanisme d’action du bisphénol A passe sans doute par des voies différentes des voies classiques, expliquant qu’il puisse avoir des effets pervers à des doses considérées jusqu’à présent comme non dangereuses, avec des courbes de réponse non monotones. Depuis 2015, une loi interdit en France la fabrication, l’importation, l’exportation de conditionnements alimentaires contenant du bisphénol A. Cette loi n’est pas (encore ?) acceptée au niveau européen. À noter que le remplacement du bisphénol A par le bisphénol S, beaucoup moins étudié, pose problème car des travaux semblent montrer qu’il pourrait avoir des effets similaires à ceux du bisphénol A.21, 22
L’utilisation des phtalates a été interdite dans le matériel médical, et de certains phtalates dans les articles de puériculture ou les jouets destinés aux enfants de moins de 3 ans. Concernant les autres matières plastiques, pas d’interdiction dans la mesure où les expositions restent très basses. Dans le domaine des produits cosmétiques, l’Union européenne interdit l’utilisation du di-2-éthylhexyle phthalate (DEHP) dont le potentiel toxique est le plus élevé. Concernant le bisphénol A et les phtalates, rien n’est encore clairement démontré au niveau épidémiologique, mais les résultats de l’étude Eden25 montrent que chez des enfants dont la mère avait des taux urinaires élevés de bisphénol A ou de DHEP pendant la grossesse il existe une augmentation de la survenue de troubles émotionnels, relationnels, et plus d’état d’hyperactivité en bas âge.
Au niveau européen, la réglementation encadre l’utilisation des parabènes dans les cosmétiques : leur concentration maximale ne doit pas dépasser 0,4 % pour un parabène seul et 0,8 % lorsque plusieurs sont utilisés. Le méthylparabène et l’éthylparabène sont sans danger lorsqu’ils sont utilisés à leur concentration maximale autorisée (v. supra). Le butylparabène et le propylparabène sont sans danger si la somme de leurs concentrations individuelles ne dépasse pas 0,19 %.
Bisphénol A
C’est le principal composant de nombreuses substances plastiques.18-20 Il fait aussi partie de la constitution des résines époxy qui tapissaient l’intérieur des boîtes de conserve. Il est utilisé dans de très nombreux domaines : produits électriques et électroniques, industrie automobile, construction, électroménager, optique... Sa voie principale de contamination est la voie orale en raison de son utilisation dans les conditionnements alimentaires. Son action serait environ 1 000 fois inférieure à celle de l’estradiol, mais il est très présent dans notre environnement. L’expérimentation animale a mis en évidence la possibilité de risques d’effets néfastes dans quatre domaines :– sur la fonction reproductrice par diminution de la sécrétion d’estrogènes : anomalie de la commande hypothalamo-hypophysaire, avec des cycles longs et irréguliers chez la femelle et un risque de baisse de fertilité chez le mâle ;
– sur le développement du tissu cérébral et des fonctions cognitives, avec des troubles de l’apprentissage et de la mémoire chez les rongeurs et les singes ;
– sur le métabolisme : risque d’augmentation du diabète insulinodépendant de type 2 ;
– sur le développement de la glande mammaire, conduisant à une susceptibilité accrue aux substances cancérogènes. Au total, en 2017, l’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail (Anses) déclarait que « les données disponibles étayent la plausibilité que le BPA module les effets agonistes des estrogènes et des progestatifs et, par là, puissent augmenter la susceptibilité au cancer ». À noter que le mécanisme d’action du bisphénol A passe sans doute par des voies différentes des voies classiques, expliquant qu’il puisse avoir des effets pervers à des doses considérées jusqu’à présent comme non dangereuses, avec des courbes de réponse non monotones. Depuis 2015, une loi interdit en France la fabrication, l’importation, l’exportation de conditionnements alimentaires contenant du bisphénol A. Cette loi n’est pas (encore ?) acceptée au niveau européen. À noter que le remplacement du bisphénol A par le bisphénol S, beaucoup moins étudié, pose problème car des travaux semblent montrer qu’il pourrait avoir des effets similaires à ceux du bisphénol A.21, 22
Phtalates
Les phtalates23 sont des plastifiants rendant le plastique souple et flexible. Ils entrent dans la composition de jouets et de nombreux produits industriels. Ils sont faiblement estrogéniques. Chez les animaux de laboratoire, ils induisent des troubles du développement testiculaire. Ils ont été incriminés dans des cas de puberté précoce chez des jeunes filles. Le risque d’hypospadias serait multiplié par 3 en cas de prise importante par la mère pendant la grossesse. Selon l’Anses, le rôle des phtalates dans la survenue de cancers reste controversé. Certaines données leur font évoquer un rôle dans le développement de l’obésité. Si une origine fœtale de malformations congénitales telles que l’hypospadias et la cryptorchidie semble assez évidente, il en va différemment pour une diminution de la fertilité qui survient à l’âge adulte. Le syndrome de dysgénésie testiculaire reste à ce jour non démontré chez l’homme.24L’utilisation des phtalates a été interdite dans le matériel médical, et de certains phtalates dans les articles de puériculture ou les jouets destinés aux enfants de moins de 3 ans. Concernant les autres matières plastiques, pas d’interdiction dans la mesure où les expositions restent très basses. Dans le domaine des produits cosmétiques, l’Union européenne interdit l’utilisation du di-2-éthylhexyle phthalate (DEHP) dont le potentiel toxique est le plus élevé. Concernant le bisphénol A et les phtalates, rien n’est encore clairement démontré au niveau épidémiologique, mais les résultats de l’étude Eden25 montrent que chez des enfants dont la mère avait des taux urinaires élevés de bisphénol A ou de DHEP pendant la grossesse il existe une augmentation de la survenue de troubles émotionnels, relationnels, et plus d’état d’hyperactivité en bas âge.
Phytoestrogènes
Les phytoestrogènes sont des substances présentes naturellement dans les plantes ou issues du métabolisme dans l’organisme d’un précurseur végétal. Ces molécules présentent une similarité de structure chimique avec le 17-bêta-estradiol. Cette similarité structurale est à l’origine de similarités fonctionnelles. Il en existe 6 familles représentées par 3 000 substances dans l’environnement...Graines de soja, lentilles, pois...
Ces végétaux contiennent des isoflavones considérées comme perturbateurs endocriniens. Chez l’animal, certaines études les ont incriminées dans la survenue de cancers mammaires et de l’utérus. Chez l’homme, divers risques ont été évoqués : augmentation du risque de diabète insulinodépendant, ou d’hypospadias chez les enfants de mère végétarienne. Mais ils auraient un rôle de protection contre le cancer du sein (4 fois moins de cancer du sein au Japon vs aux États-Unis). Ils induisent une légère diminution du LDL-cholestérol. En Asie, où ces produits sont couramment utilisés, on note que le cycle des femmes chinoises et japonaises est plus long de 2 ou 3 jours ; que l’ostéoporose et les fractures chez les femmes japonaises sont moins fréquentes qu’en Occident, et qu’il existe une incidence plus basse des cancers hormono-dépendants. L’état de santé des nourrissons nourris par du lait de soja ne montre pas de différence avec celui des enfants nourris au lait maternel, et aucune toxicité n’a été constatée chez ces enfants.26Parabènes : paraoxybenzoates
Les parabènes27 sont utilisés comme conservateurs, ayant une forte activité antibactérienne et antimycosique. Leur origine est soit naturelle, présents dans l’orge, la fraise, la vanille, la gelée royale, soit artificielle de structure diverse : méthyl, propyl, éthyl, et butylparabène. On les trouve dans les shampoings, les déodorants, les masques pour le visage, les crèmes pour la peau... Ils sont suspects d’être des perturbateurs endocriniens. Des expériences chez l’animal montrent des effets sur l’appareil reproducteur avec certains d’entre eux comme le butylparabène. Des publications font évoquer leur rôle dans la survenue de cancers du sein chez des femmes les utilisant, mais ces études n’ont pas été validées. À titre de précaution, il est conseillé de ne pas les utiliser en région axillaire après rasage, ce qui fragilise la peau.Au niveau européen, la réglementation encadre l’utilisation des parabènes dans les cosmétiques : leur concentration maximale ne doit pas dépasser 0,4 % pour un parabène seul et 0,8 % lorsque plusieurs sont utilisés. Le méthylparabène et l’éthylparabène sont sans danger lorsqu’ils sont utilisés à leur concentration maximale autorisée (v. supra). Le butylparabène et le propylparabène sont sans danger si la somme de leurs concentrations individuelles ne dépasse pas 0,19 %.
En guise de synthèse…
Au sein des 100 000 produits chimiques nous environnant, environ 1 000 sont potentiellement des perturbateurs endocriniens. Depuis 2013, tous ces produits sont interdits en utilisation phytosanitaire. Les études chez l’homme montrant des effets délétères l’ont été tout d’abord dans des conditions de contacts importants et prolongés. La mise en évidence dans la population générale d’anomalies de la fertilité et des organes génitaux, voire l’augmentation des cancers hormono-dépendants, font suspecter le rôle des perturbateurs endocriniens. La glande thyroïde et sa production hormonale pourraient également être impactées par certaines de ces substances. Actuellement,un certain nombre d’éléments concordants semblent confirmer leur rôle dans la survenue de ces problèmes. Si le bisphénol A a été interdit en France dans tout ce qui concerne les conditionnements alimentaires, la question se pose pour d’autres substances. Une interrogation surgit alors : par quoi les remplacer ? Car leur utilité n’est pas contestée par ailleurs. Une attitude prudentielle est nécessaire chez les femmes enceintes, les enfants de moins de 3 ans et en période pubertaire. Il reste beaucoup de travail à réaliser pour préciser l’importance de l’effet « cocktail » et de l’effet des très petites doses.
Références
1. Les perturbateurs endocriniens. Première partie : L’hypothèse d’un danger commun à la faune et à l’espèce humaine. Rev Prescrire 2011;31:222-8. Deuxième partie : Une hypothèse plausible pas encore vérifiée. Rev Prescrire 2011;31:378-85.
2. Fénichel P, Brucker-Davis F, Chevalier N. The history of Distilbene (Diethyl stilbestrol) told to grandchildren-the trangenerational effect. An Endocrinol 2015;76:253-9.
3. Sultan C, Gaspari l, Kalfa N, Philibert P, Paris F. Perturbateurs endocriniens environnementaux et maladies endocriniennes de l’enfant. Med Enf 2013;10:272-5.
4. Loupare D. Le bisphénol A peut-il être plus toxique à faible dose qu’à forte dose ? https://sciencetonnante.wordpress.com ou https://bit.ly/3bmPX19
5. Chevalier N. Les perturbateurs endocriniens : de nouveaux acteurs dans l’épidémie d’obésité et de diabète type 2 ? Metab Horm Diab Nutr 2014;18:248-52.
6. Wagner-Mahler K, Kurzenne JY, Delattre I et al. Incidence of cryptorchidism at birth: a prospective study at the University Hospital of Nice. Presse Med 2010;39:981-2.
7. Mauduit C, Sideek B, Benahmed M. Origine développementale de l’infertilité masculine. Rôle des perturbateurs endocriniens. Med Sci 2016;32:45-50.
8. Rochefort H, Jouannet P, au nom d’un groupe de travail Perturbateurs endocriniens (PEs) et cancers. Analyse des risques et des mécanismes, propositions pratiques. Bull Acad Nat Med 2011;195:1783-5.
9. Skakkebaek NE, Rajpert-De Meyts E, Main KM. Testicular dysgenesis syndrome: an increasingly common developmental disorder with environmental aspects. Hum Reprod 2001;16:972-8.
10. Le Moal J, Rigou A, de Crouy-Chanel P, et al. Analyse combinée des quatre indicateurs du syndrome de dysgénésie testiculaire en France dans le contexte de l’exposition aux perturbateurs endocriniens : cryptorchidie, hypospadias, cancer du testicule et qualité du sperme. BEH 2018;22-23:452-63.
11. Rigou A, Le Moal J, Le Tertre A, et al. L’incidence de la puberté précoce centrale idiopathique en France révèle une hétérogénéité géographique importante. BEH 2018;22-3:464-71.
12. Kim SH, Huh K, Won S, Lee KW, Park MJ. A significant increase in the incidence of central precocious puberty among Korean girls from 2004 to 2010. PLoS One 2015;10:e0141844.
13. Yum T, Lee S, Kim Y Association between precocious puberty and some endocrine disruptors in human plasma. J Environ Sci Health A Tox Hazard Subst Environ Eng 2013;48(8):912-7
14. Krstevska-Konstantinova M, Charlier C, Craen M, et al 2001 ; Sexual precocity after immigration from developing countries to Belgium: evidence of previous exposure to organochlorine pesticides. Hum Reprod 16:1020 –1026 18.
15. Parent AS, Teilmann G, Juul A et al 2003 ; The Timing of Normal Puberty and the Age Limits of Sexual Precocity: Variations around the World, Secular Trends, and Changes after Migration. Endoc Rev 2003 ; 24(5):668 – 693
16. Demeneix B. Le cerveau endommagé. Paris : Odile Jacob sciences, 2016.
17. Houdeau E. Plastiques alimentaires : comment s’y retrouver ? Ped Abstract impact santé 2011;44:11-5.
18. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail. Effets sanitaires du bisphénol A. Rapport d’expertise collective : Connaissances relatives aux usages du bisphénol A. Rapport d’étude Anses 2011.
19. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail. Évaluation des risques du bisphénol A (BPA) pour la santé humaine. Avis de l’Anses. Rapport d’expertise collective Anses 2013.
20. Agence nationale de sécurité sanitaire de l’alimentation de l’environnement et du travail. Avis de l’Anses relatif à l’identification en tant que substance extrêmement préoccupante (SVHC) du bisphénol A pour son caractère de perturbateur endocrinien. Maisons-Alfort, 2017.
21. Ahmed S, Atlas E. Bisphenol S and bisphenol A induced adipogenesis of murine preadipocytes occurs through direct peroxisome proliferator-activated receptor gamma activation. Int J Obes (Lond) 2016;40:1566-73.
22. Dinda S. Exposure to BPA substitute, BPS, multiplies breast cancer cells. Endocrine Society’s April 2017.
23. Duty SM, Silva MJ, Barr DB, et al. Phthalate exposure and human semen parameters. Epidemiol 2003;14:269-77.
24. Rousselle C, Bellanger M, Fiore K, et al. Évaluation de l’impact sur la santé reproductive masculine et des coûts associés de deux phtalates : le DEHP et le DINP. BEH 2018;22-23:472-9.
25. Philippat C, Nakiwala D, Calafat A. Prenatal exposure to non persistent endocrine disruptors and behavior in boys at 3 and 5 years. Environ Health Perspect 2017;125:097014.
26. Vandenplas Y, Castrellon PG, Rivas R, et al. Safety of soya-based infant formula in children. Br J Nutr 2014;111:1340-60.
27. Académie nationale de pharmacie. Parabènes et médicaments : un problème de santé publique ? Recommandations du 22 mai 2013.
2. Fénichel P, Brucker-Davis F, Chevalier N. The history of Distilbene (Diethyl stilbestrol) told to grandchildren-the trangenerational effect. An Endocrinol 2015;76:253-9.
3. Sultan C, Gaspari l, Kalfa N, Philibert P, Paris F. Perturbateurs endocriniens environnementaux et maladies endocriniennes de l’enfant. Med Enf 2013;10:272-5.
4. Loupare D. Le bisphénol A peut-il être plus toxique à faible dose qu’à forte dose ? https://sciencetonnante.wordpress.com ou https://bit.ly/3bmPX19
5. Chevalier N. Les perturbateurs endocriniens : de nouveaux acteurs dans l’épidémie d’obésité et de diabète type 2 ? Metab Horm Diab Nutr 2014;18:248-52.
6. Wagner-Mahler K, Kurzenne JY, Delattre I et al. Incidence of cryptorchidism at birth: a prospective study at the University Hospital of Nice. Presse Med 2010;39:981-2.
7. Mauduit C, Sideek B, Benahmed M. Origine développementale de l’infertilité masculine. Rôle des perturbateurs endocriniens. Med Sci 2016;32:45-50.
8. Rochefort H, Jouannet P, au nom d’un groupe de travail Perturbateurs endocriniens (PEs) et cancers. Analyse des risques et des mécanismes, propositions pratiques. Bull Acad Nat Med 2011;195:1783-5.
9. Skakkebaek NE, Rajpert-De Meyts E, Main KM. Testicular dysgenesis syndrome: an increasingly common developmental disorder with environmental aspects. Hum Reprod 2001;16:972-8.
10. Le Moal J, Rigou A, de Crouy-Chanel P, et al. Analyse combinée des quatre indicateurs du syndrome de dysgénésie testiculaire en France dans le contexte de l’exposition aux perturbateurs endocriniens : cryptorchidie, hypospadias, cancer du testicule et qualité du sperme. BEH 2018;22-23:452-63.
11. Rigou A, Le Moal J, Le Tertre A, et al. L’incidence de la puberté précoce centrale idiopathique en France révèle une hétérogénéité géographique importante. BEH 2018;22-3:464-71.
12. Kim SH, Huh K, Won S, Lee KW, Park MJ. A significant increase in the incidence of central precocious puberty among Korean girls from 2004 to 2010. PLoS One 2015;10:e0141844.
13. Yum T, Lee S, Kim Y Association between precocious puberty and some endocrine disruptors in human plasma. J Environ Sci Health A Tox Hazard Subst Environ Eng 2013;48(8):912-7
14. Krstevska-Konstantinova M, Charlier C, Craen M, et al 2001 ; Sexual precocity after immigration from developing countries to Belgium: evidence of previous exposure to organochlorine pesticides. Hum Reprod 16:1020 –1026 18.
15. Parent AS, Teilmann G, Juul A et al 2003 ; The Timing of Normal Puberty and the Age Limits of Sexual Precocity: Variations around the World, Secular Trends, and Changes after Migration. Endoc Rev 2003 ; 24(5):668 – 693
16. Demeneix B. Le cerveau endommagé. Paris : Odile Jacob sciences, 2016.
17. Houdeau E. Plastiques alimentaires : comment s’y retrouver ? Ped Abstract impact santé 2011;44:11-5.
18. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail. Effets sanitaires du bisphénol A. Rapport d’expertise collective : Connaissances relatives aux usages du bisphénol A. Rapport d’étude Anses 2011.
19. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail. Évaluation des risques du bisphénol A (BPA) pour la santé humaine. Avis de l’Anses. Rapport d’expertise collective Anses 2013.
20. Agence nationale de sécurité sanitaire de l’alimentation de l’environnement et du travail. Avis de l’Anses relatif à l’identification en tant que substance extrêmement préoccupante (SVHC) du bisphénol A pour son caractère de perturbateur endocrinien. Maisons-Alfort, 2017.
21. Ahmed S, Atlas E. Bisphenol S and bisphenol A induced adipogenesis of murine preadipocytes occurs through direct peroxisome proliferator-activated receptor gamma activation. Int J Obes (Lond) 2016;40:1566-73.
22. Dinda S. Exposure to BPA substitute, BPS, multiplies breast cancer cells. Endocrine Society’s April 2017.
23. Duty SM, Silva MJ, Barr DB, et al. Phthalate exposure and human semen parameters. Epidemiol 2003;14:269-77.
24. Rousselle C, Bellanger M, Fiore K, et al. Évaluation de l’impact sur la santé reproductive masculine et des coûts associés de deux phtalates : le DEHP et le DINP. BEH 2018;22-23:472-9.
25. Philippat C, Nakiwala D, Calafat A. Prenatal exposure to non persistent endocrine disruptors and behavior in boys at 3 and 5 years. Environ Health Perspect 2017;125:097014.
26. Vandenplas Y, Castrellon PG, Rivas R, et al. Safety of soya-based infant formula in children. Br J Nutr 2014;111:1340-60.
27. Académie nationale de pharmacie. Parabènes et médicaments : un problème de santé publique ? Recommandations du 22 mai 2013.
Dans cet article
- Quelles sont les conséquences de la présence de certaines substances dans l’environnement ?
- Alerte chez l’homme
- Mécanismes d’action des perturbateurs endocriniens
- Difficultés rencontrées dans l’étude des effets des perturbateurs endocriniens
- Nature des perturbateurs endocriniens environnementaux, chimiques ou naturels
- Quels effets sur le système reproducteur ?
- Effets sur la production hormonale thyroïdienne
- Perturbateurs endocriniens : ce qui les accuse...
- Perturbateurs fréquemment rencontrés
- En guise de synthèse…