Optimiser la prise en charge du lymphœdème limite la survenue de ses complications. Elle repose sur la physiothérapie décongestive complète soutenue par un programme d’éducation thérapeutique.
Les lymphœdèmes des membres sont la conséquence d’un dysfonctionnement du système lymphatique responsable d’une stase de la lymphe, puis de l’augmentation de volume du membre atteint. Le système lymphatique a pour fonction de réabsorber les protéines, les liquides, les cellules immunitaires et les métabolites cellulaires passés dans l’espace extracellulaire au niveau des capillaires. Cette stase liquidienne, riche en protéines, entraîne une accumulation de macrophages, polynucléaires neutrophiles, cellules dendritiques qui stimule la production de collagène par les fibroblastes, induit une rupture des fibres élastiques et une activation des kératinocytes et des adipocytes.1 L’évolution se fait ainsi vers une augmentation du tissu adipeux, un épaississement et une « fibrose » cutanés, rendant le lymphœdème en grande partie irréversible car la partie liquidienne – lymphatique – est minoritaire. Connaître cette composition tissulaire permet d’optimiser la prise en charge de cette maladie chronique dont les risques les plus fréquents, sans traitement, sont l’augmentation progressive de volume et la survenue de complications infectieuses (érysipèle).
Primaire ou secondaire ?
Les lymphœdèmes peuvent être classés en deux types : les lymphœdèmes primaires (sans notion d’intervention sur le système lymphatique) et les lymphœdèmes secondaires.
Les lymphœdèmes primaires sont des anomalies constitutionnelles du système lymphatique, apparaissant le plus souvent chez l’adolescent ou l’adulte jeune.2 Ils peuvent être isolés ou parfois familiaux d’origine génétique (ex : maladie de Milroy, liée à un variant pathogène du gène du récepteur 3 du vascular endothelial growth factor 3, VEGFR-3) ou syndromique dans le cadre de maladies plus complexes et associé à d’autres signes cliniques (ex : syndrome de Turner).
Les lymphœdèmes secondaires (les plus fréquents en France) font suite à des lésions des voies lymphatiques principalement dues à des traitements de cancers avec curage ganglionnaire associé ou non à une irradiation. Ainsi, environ 20 % des femmes développent un lymphœdème du membre supérieur après traitement d’un cancer du sein ; 25 % des lymphœdèmes des membres inférieurs font suite à un traitement de cancer pelvien.3, 4 Il existe toutefois d’autres causes, plus rares, de lymphœdèmes secondaires (
Affirmer le diagnostic de lymphœdème primaire
Le diagnostic de lymphœdème est avant tout clinique. Il est facile lorsqu’il existe des antécédents de cancer comprenant un curage ganglionnaire, associé ou non à une radiothérapie.
Éliminer une cause
Avant de retenir le diagnostic de lymphœdème primaire des membres inférieurs, les autres causes d’œdèmes « classiques » (cardiaques, rénales, hépatiques, liées à une hypoalbuminémie) doivent avoir été éliminées.
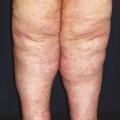
De même, le lipœdème, principal diagnostic différentiel, est fréquemment confondu avec les lymphœdèmes primaires des membres inférieurs.5 Il s’agit d’une répartition anormale du tissu adipeux des hanches jusqu’aux genoux ou chevilles (
En cas de doute diagnostique, un scanner abdomino-pelvien est nécessaire pour éliminer un syndrome compressif.
Une clinique évocatrice
Le diagnostic de lymphœdème du membre supérieur en consultation est posé lorsque la différence de circonférence est d’au moins 2 cm par rapport au membre controlatéral.
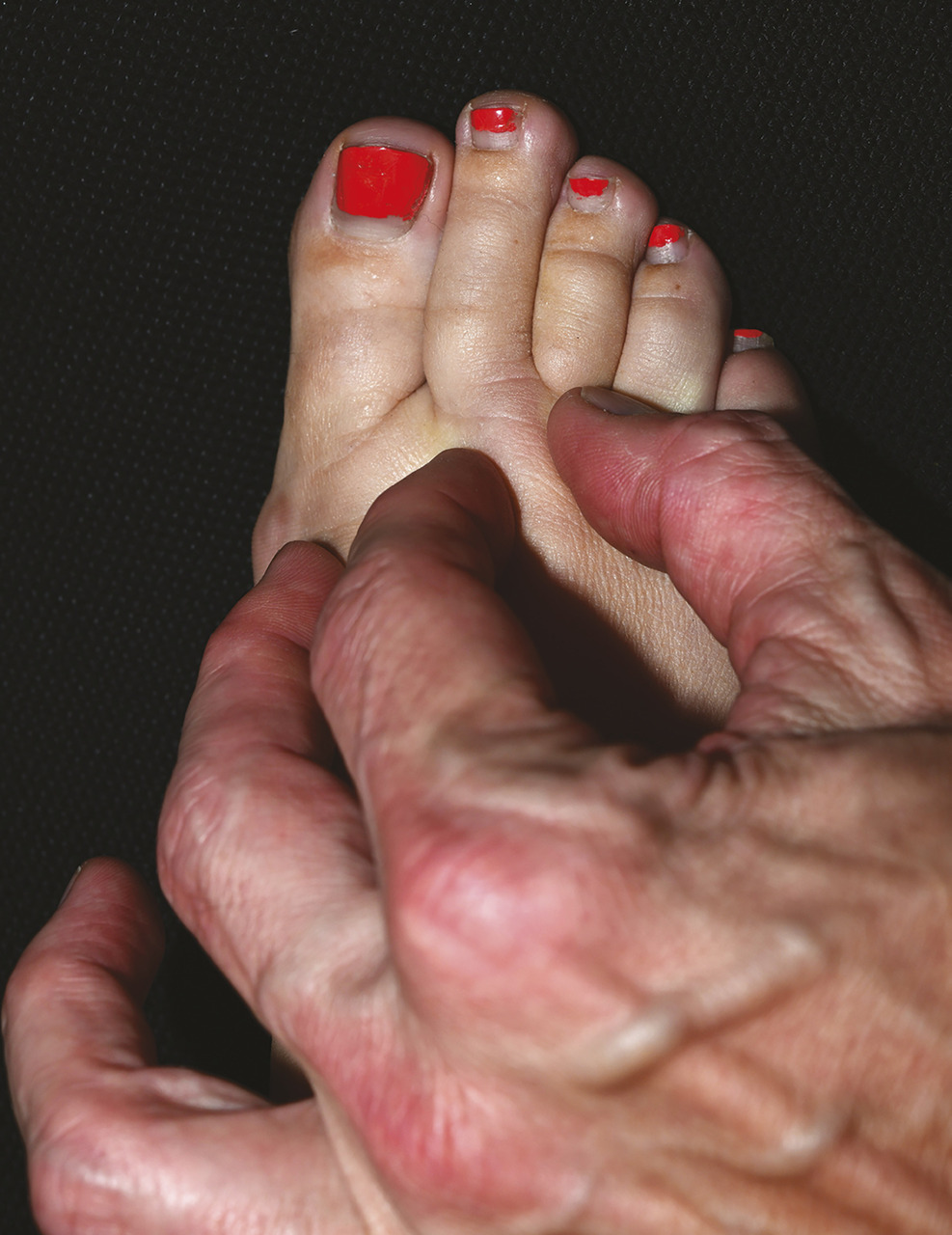
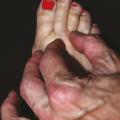
Pour les membres inférieurs, les lymphœdèmes étant fréquemment bilatéraux, le principal élément diagnostique est la présence d’un signe de Stemmer (épaississement ou impossibilité de plisser la peau de la face dorsale du 2e orteil) [
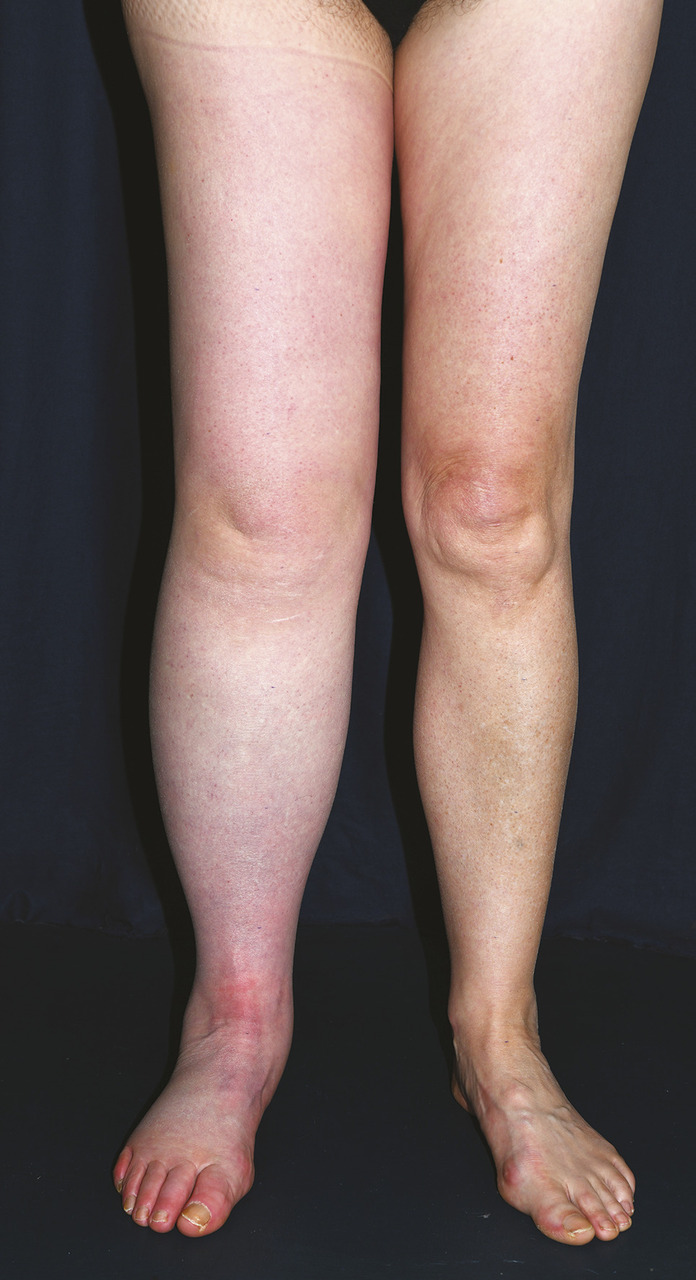
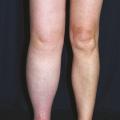
Dans les lymphœdèmes primaires, l’atteinte est soit unilatérale de tout le membre inférieur (
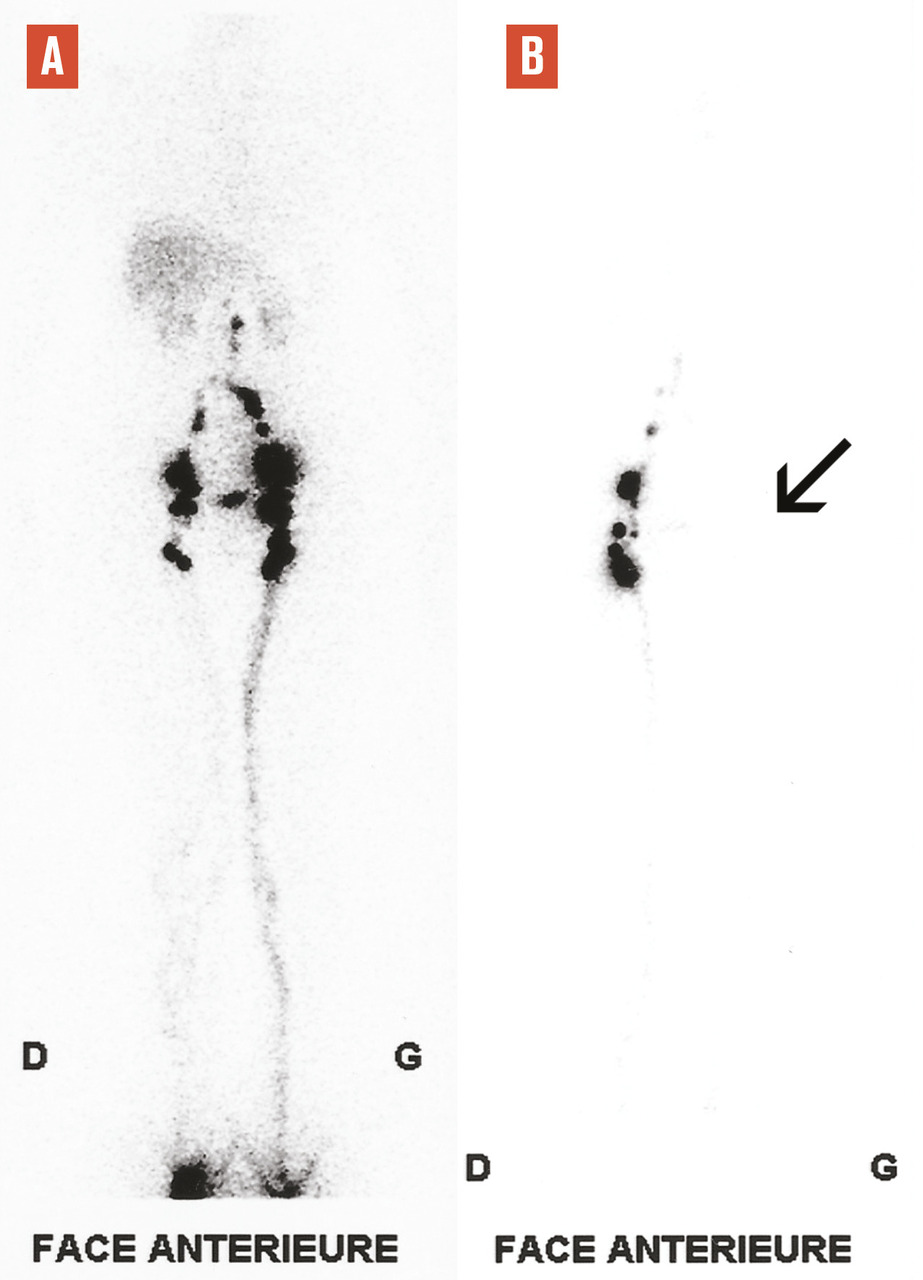
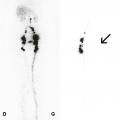
La confirmation diagnostique de lymphœdème primaire peut être apportée par une lymphoscintigraphie dans un centre spécialisé ; cet examen permet de mettre en évidence une hypo- ou une absence de fixation du traceur radioactif au niveau inguinal (
Physiothérapie décongestive, clé de la prise en charge
La physiothérapie décongestive complète est le terme utilisé pour définir le traitement combiné du lymphœdème ; elle se divise en deux phases :6
– la première, dite « intensive », destinée à réduire le volume du lymphœdème, est fondée avant tout sur la pose de bandages peu élastiques monotypes. La physiothérapie décongestive complète peut être effectuée en hospitalisation avec des bandages portés 24 heures sur 24 et renouvelés 5 jours sur 7, ou en ambulatoire avec des bandages renouvelés trois fois par semaine et conservés pendant 48 heures ;
– la deuxième, dite d’« entretien », vise à maintenir le volume réduit à long terme, voire à poursuivre la réduction volumétrique. Elle associe le port d’une compression élastique la journée, la réalisation de bandages peu élastiques la nuit à une fréquence inférieure à celle du traitement intensif, et des soins de peau (hydratation par une crème émolliente). Le patient peut être autonome à cette étape de la prise en charge, après apprentissage avec un kinésithérapeute (
Si les indications de traitement ne sont pas clairement définies, il est toutefois important de prendre en charge les lymphœdèmes afin d’éviter une aggravation volumétrique et la survenue de complications, et espérer ainsi améliorer la qualité de vie. La Haute Autorité de santé (HAS) a publié des recommandations en 2010 sur le traitement des lymphœdèmes avec les bandages composés exclusivement de bandes à allongement court et les a confirmées en 2020.8, 9
Quels bandages ?
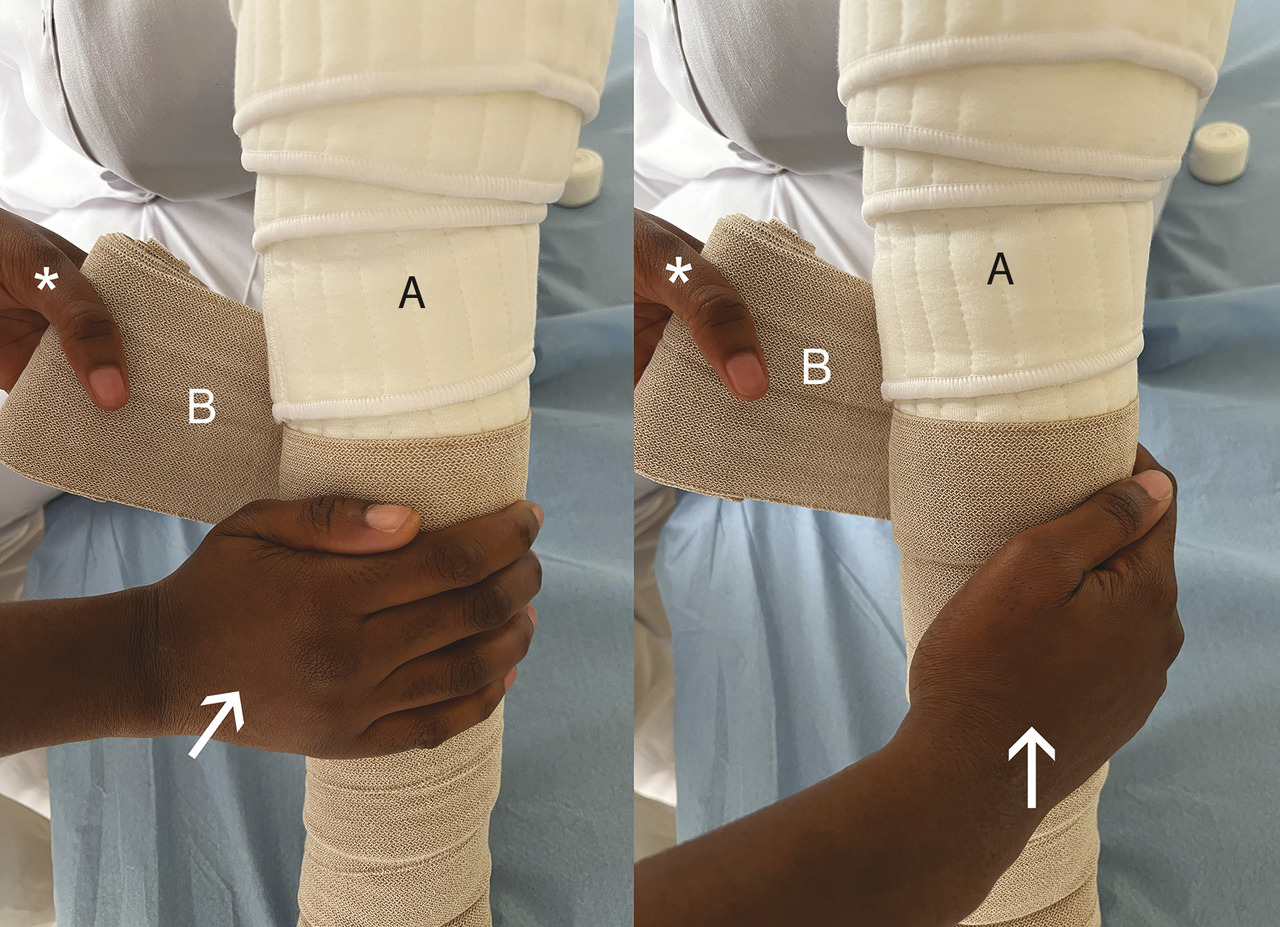
Les bandages constituent l’élément essentiel destiné à réduire le volume du lymphœdème. Il s’agit de poser, sans les serrer, des bandes à allongement court (< 100 %) sur un capitonnage fait soit de coton, soit de mousse (simple, tissée, alvéolée), soit des deux. Ces bandages sont appelés « multicouches monotypes » du fait de la superposition de deux à quatre épaisseurs du même type de bandes (
Le bandage est un acte coté de kinésithérapie, et la technique doit être bien maîtrisée, car ces bandages sont maintenus en place pendant vingt-quatre à trente-six heures et ne doivent surtout pas induire de douleur.10 La pression exercée au repos est faible, permettant de les supporter sur l’ensemble du nycthémère (à la différence des bandes élastiques, difficiles à supporter la nuit), mais augmente nettement lors de la contraction musculaire puisque ces bandes sont peu extensibles. La réduction de volume est comprise entre 30 à 40 %, en fonction de la composante liquidienne du lymphœdème.
Les bandages multicouches multitypes associent des bandes de caractéristiques et d’allongement différents (dont des bandes élastiques) utilisées en pathologie vasculaire. Il n’existe, à ce jour, qu’une étude de qualité satisfaisante ayant évalué l’efficacité sur la réduction volumétrique et la tolérance des bandages comprenant une bande à allongement long dans le traitement du lymphœdème.11
D’autres types de bandes, cohésives ou collées, n’ont fait l’objet que de très peu d’évaluation dans le traitement du lymphœdème et ne sont donc pas recommandées.8
La pratique d’une activité physique adaptée avec les bandages permettrait d’augmenter le débit lymphatique et ainsi l’efficacité du traitement sans que le type d’exercices soit clairement défini.
Une place limitée pour les drainages lymphatiques manuels
Bien que considérés comme le gold standard du traitement des lymphœdèmes, il est maintenant établi que les drainages lymphatiques manuels (DLM) n’ont pas d’effet en prévention du lymphœdème ni d’impact sur le volume d’un lymphœdème traité en association avec des bandages peu élastiques.12, 13 Ils sont pratiqués par des kinésithérapeutes formés à ces techniques (dont il existe plusieurs variantes), durent environ trente minutes et débutent théoriquement par le tronc et la racine du membre atteint pour finir en distalité (main, pied).
S’ils peuvent apporter à certains patients un confort, un effet relaxant et une diminution de la tension cutanée, ils ne doivent pas être le traitement de première intention des lymphœdèmes débutants ; la prise en charge comprend alors les bandages peu élastiques ou le port d’une compression élastique.
Les DLM peuvent être utiles dans les lymphœdèmes proximaux au niveau du sein ou de la paroi thoracique, difficilement accessibles à la compression. Ils permettent également un suivi régulier par un professionnel de santé, aidant à maintenir la motivation des patients pour le traitement de cette maladie chronique.
Ils restent donc utiles en phase intensive de réduction de volume mais sont facultatifs en phase d’entretien.14
Personnaliser le traitement grâce à l’éducation thérapeutique
Les lymphœdèmes constituent une maladie chronique qui nécessite l’adhésion au traitement et l’implication du patient. L’intégration d’un programme d’éducation thérapeutique du patient (ETP), élaboré selon les recommandations de la HAS et prenant en compte l’ensemble des difficultés rencontrées et ressenties ainsi que les objectifs pédagogiques, permet de proposer un traitement personnalisé. Le patient acquiert ainsi les compétences nécessaires pour mieux vivre avec sa maladie dans les domaines du savoir, du savoir-faire et du savoir-être. L’ETP s’appuie sur des ateliers collectifs et individuels, notamment pour l’apprentissage des autobandages.15 Ces autobandages peu élastiques sont simplifiés pour être utilisés au moins trois fois par semaine, la nuit, en complément de la compression diurne.
À distance du traitement intensif, les patients peuvent revoir les techniques d’autobandages sur des tutoriels vidéos, tournés dans le service de lymphologie de l’hôpital Cognacq-Jay et disponibles sur internet.10
L’utilisation de dispositif de compression nocturne (appelé aussi wrap et disposant de bandes Velcro), que le patient met lui-même en place, semblerait aussi efficace que la réalisation de bandages nocturnes pour stabiliser, voire réduire, le lymphœdème, en maintenant le port d’une compression élastique la journée (
Indispensable port d’une compression élastique au long cours
Le terme de « compression élastique » est plus approprié que le terme de « contention », qui ne devrait plus être utilisé. En effet, la pression s’exerce en permanence sur le membre à traiter en raison de la présence des fibres élastiques. Le port de la compression n’est pas facilement accepté, car il s’agit de dispositifs contraignants mais indispensables au long cours pour maintenir le bénéfice obtenu après la réduction de volume acquise par les bandages peu élastiques lors de la phase intensive.8
Il n’est généralement pas conseillé de les garder la nuit.
Les compressions élastiques seules entraînent une diminution modeste et lente du volume du lymphœdème. Cependant, en présence d’un lymphœdème de petit volume (moins de 20 % d’excès de volume par rapport au membre controlatéral) ou récent (moins d’un an), il est possible de mettre en place une compression élastique comme seul traitement, sans phase de réduction intensive.17
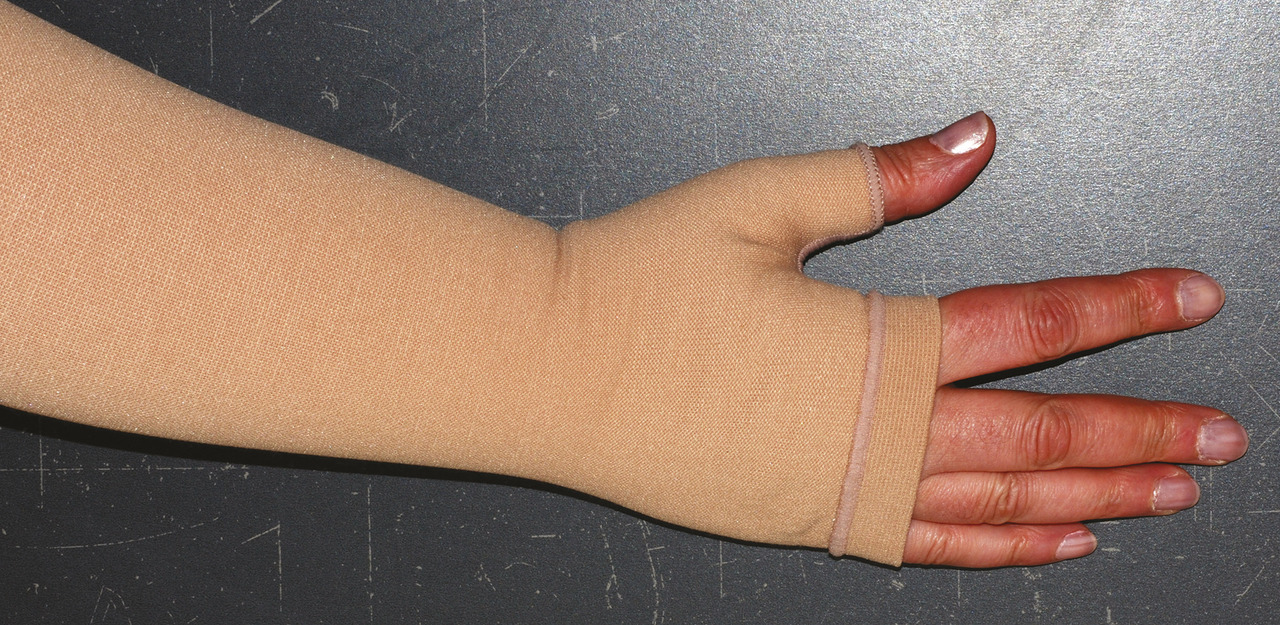
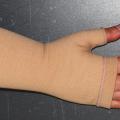
Le type de compression est adapté au lymphœdème : manchon avec ou sans mitaine attenante (couvrant la main, préférable pour éviter que la main et les doigts ne gonflent) [
Il existe deux types de tricotage des compressions : circulaire ou tubulaire, sans couture, plus facile à enfiler et rectiligne. Le tricotage rectiligne, plus rigide que le circulaire, est surtout utilisé pour les membres dysmorphiques ou avec des plis marqués au niveau de la cheville, de la jambe ou du poignet, ou lorsqu’il est nécessaire de comprimer individuellement les orteils (couvre-orteils) ou les doigts (gantelet).18
Au niveau du membre supérieur, les compressions de classe 3 ou 4 peuvent être proposées (éventuellement une classe 2 si l’enfilage est difficile).
Au niveau du membre inférieur, il faut privilégier une classe 3 ou 4 (recours fréquent à la superposition de deux compressions de classe 3) avec parfois la nécessité d’utiliser des dispositifs d’aide à l’enfilage. Il est préférable de préconiser des bas ou chaussettes avec pied fermé pour éviter l’aggravation du lymphœdème des orteils et l’apparition éventuelle de vésicules responsables d’écoulements parfois prolongés et invalidants. En cas de superposition, la première compression sur la peau est « pied fermé » et la seconde « pied ouvert » pour diminuer l’hyperpression sur les zones osseuses peu touchées par le lymphœdème et éviter ainsi les douleurs.
Dans la plupart des cas, il est nécessaire de faire réaliser par un orthésiste ou un pharmacien orthopédiste-orthésiste des compressions sur mesure qui sont remplacées tous les trois à quatre mois.
Érysipèle, la plus fréquente des complications
En dehors des importants retentissements psychosocial, esthétique et fonctionnel, les principales complications dermatologiques des lymphœdèmes sont de trois types : infectieuses, dysimmunitaires et néoplasiques. La plus sévère est l’angiosarcome qui doit être redouté et dépisté mais reste exceptionnelle ; la plus fréquente est l’érysipèle, qui complique de 20 à 30 % des lymphœdèmes.19
Le risque d’érysipèle (ou dermohypodermite bactérienne non nécrosante) au cours d’un lymphœdème est très important, augmenté d’un facteur 70 environ par comparaison avec un membre sain.20 Toute effraction cutanée, même minime, peut constituer une porte d’entrée infectieuse : griffures, morsures, brûlures, piqûres d’insecte ou d’aiguille à coudre... Le port de gants, de chaussures est recommandé dans les situations à risque de blessures. Les érysipèles peuvent être récidivants et participer à l’augmentation du volume du lymphœdème. L’application de crèmes émollientes est très souvent nécessaire et reste possible avant la pose d’une compression élastique, sans risque de la détériorer, mais à la condition de laver régulièrement les dispositifs.
Le traitement de l’érysipèle repose sur l’amoxicilline (50 mg/kg/j en 3 prises, maximum 6 g/j pendant 7 jours) ; ou, en cas d’allergie à la pénicilline, sur la pristinamycine (3 g/j en 3 prises pendant 7 jours) ou la clindamycine (600 mg 3 fois par jour et jusqu’à 600 mg 4 fois par jour si le poids est supérieur à 100 kg, pendant 7 jours).21
La fréquence des érysipèles varie d’un seul épisode à de multiples récidives nécessitant alors une prophylaxie anti-infectieuse par une pénicilline à libération prolongée (benzathine benzylpénicilline [G retard]), en l’absence d’allergie à la pénicilline, à la dose de 2,4 MUI toutes les deux à quatre semaines ou par phénoxyméthylpénicilline (pénicilline V) orale, 1 à 2 MUI selon le poids en deux prises. En cas d’allergie à la pénicilline, l’azithromycine (250 mg/j) est préconisée.21 La durée de l’antibioprophylaxie n’est pas définie, mais une durée prolongée (plus de 18 à 24 mois) semble nécessaire. Aucune résistance du streptocoque à la pénicilline n’a été rapportée dans l’érysipèle, et elle est toujours efficace à doses curatives dans le traitement des récidives, même sous antibioprophylaxie.
Au niveau des pieds, il est indispensable de dépister et prévenir les intertrigos et de les traiter par antimycosiques ; et de prendre en charge les hyperkératoses par des soins de pédicurie réguliers, car ces lésions représentent les principales portes d’entrée infectieuses. Au niveau du membre supérieur, les portes d’entrée sont beaucoup plus rarement retrouvées.
Des conseils hygiénodiététiques actualisés
Les données actuelles de la littérature rendent caducs de nombreux conseils et mesures de prévention classiques et empiriques pour les femmes opérées d’un cancer du sein, ou en présence d’un lymphœdème. Ainsi, le port de charges, les mouvements répétitifs, les prélèvements sanguins, les perfusions, la prise de la pression artérielle sur le bras atteint, les voyages en avion quelle qu’en soit la durée, les expositions au soleil ou au froid ne semblent pas préjudiciables.22-24 De même, la surélévation du membre avec le lymphœdème n’a pas d’intérêt pour la réduction de volume.
Le contrôle du poids est en revanche nécessaire car la prise de poids augmente le volume d’un lymphœdème, qui comprend une partie adipeuse. Une perte de poids, en cas d’obésité, peut aussi favoriser une diminution de volume.
Toutes les activités physiques, sans aucune restriction médicale en raison du lymphœdème, peuvent être pratiquées, idéalement avec une compression élastique, mais si celle-ci est mal tolérée pendant l’effort, elle peut être retirée et remise au décours.25
Les autres traitements physiques (pressothérapie pneumatique, endermologie, kinésio-taping), les prises en charge chirurgicales (transfert ganglionnaire, anastomose lymphoveineuse, liposuccion) et l’acupuncture n’ont pas fait l’objet d’évaluation suffisante ou ne sont pas suffisamment consensuelles pour pouvoir être recommandés dans le traitement du lymphœdème en dehors d’essais cliniques.26-28
Enfin, les veinotoniques n’ont pas montré d’utilité dans la réduction ou la stabilisation des lymphœdèmes, et les diurétiques sont proscrits.
Susciter l’adhésion du patient pour la prise en charge sur le long terme
Après une phase intensive de physiothérapie décongestive complète basée sur des bandages peu élastiques monotypes, la phase d’entretien associe le port d’une compression élastique et des bandages peu élastiques la nuit. Les drainages lymphatiques manuels apportent principalement un confort au patient. Apprentissage de la pose des bandages et éducation thérapeutique permettent aux patients d’accepter la prise en charge au long cours que nécessitent les lymphœdèmes.
1. Zampell JC, Yan A, Elhadad S, Avraham T, Weitman E, Mehrara BJ. CD4(+) cells regulate fibrosis and lymphangiogenesis in response to lymphatic fluid stasis. PLoS One 2012;7(11):e49940.
2. Brouillard P, Witte MH, Erickson RP, Damstra RJ, Becker C, Quéré I, et al. Primary lymphoedema. Nat Rev Dis Primers 2021;7(1):77.
3. DiSipio T, Rye S, Newman B, Hayes S. Incidence of unilateral arm lymphoedema after breast cancer: a systematic review and meta-analysis. Lancet Oncol 2013;14(6):500-15.
4. Bernas M, Thiadens SRJ, Smoot B, Armer JM, Stewart P, Granzow J. Lymphedema following cancer therapy: overview and options. Clin Exp Metastasis 2018;35(5-6):547-51.
5. Vignes S. Lipœdème. Obésité 2019;14(3):124-30.
6. Lasinski BB, McKillip Thrift K, Squire D, Austin MK, Smith KM, Wanchai A, et al. A systematic review of the evidence for complete decongestive therapy in the treatment of lymphedema from 2004 to 2011. PM R 2012;4(8):580-601.
7. Cheville AL, McGarvey CL, Petrek JA, Russo SA, Taylor ME, Thiadens SR. Lymphedema management. Semin Radiat Oncol 2003;13:290-301.
8. Haute Autorité de santé, Bon usage des technologies de santé, La compression médicale dans le traitement du lymphoedeme. Décembre 2010. Disponible sur : https://has-sante.fr/upload/docs/application/pdf/2010-12/fiche_de_bon_usage_-_compression_medicale_dans_les_affections_veineuses_chroniques_2010-12-16_11-04-22_128.pdf
9. Haute Autorité de santé. Commission nationale d’évaluation des dispositifs médicaux et des technologies de santé (CNEDiMTS). Avis du 14 janvier 2020. Disponible sur : https://has-sante.fr/upload/docs/application/pdf/2020-02/avis_bandes_allongement_long_dm_eval_244.pdf
10. Tutoriels à destination des patients sur l’autobandage. Chaïne Youtube de l’hôpital Cognacq-Jay. Paris. Disponible sur : https://www.youtube.com/channel/UCzrjQrIBuoioABzApq0E9GA
11. Torres-Lacomba M, Navarro-Brazález B, Prieto-Gómez V, Ferrandez JC, Bouchet JY, Romay-Barrero H. Effectiveness of four types of bandages and kinesio-tape for treating breast-cancer-related lymphoedema: a randomized, single-blind, clinical trial. Clin Rehabil 2020;34(9):1230-41.
12. Wanchai A, Armer JM. Manual lymphedema drainage for reducing risk for and managing breast cancer-related lymphedema after breast surgery: a systematic review. Nurs Womens Health 2021;25(5):377-83.
13. De Vrieze T, Gebruers N, Nevelsteen I, Fieuws S, Thomis S, De Groef A, et al. Manual lymphatic drainage with or without fluoroscopy guidance did not substantially improve the effect of decongestive lymphatic therapy in people with breast cancer-related lymphoedema (EFforT-BCRL trial): a multicentre randomised trial. J Physiother 2022, doi: 10.1016/j.jphys.2022.03.010.
14. Institut national du cancer. Cancers du sein. 10 novembre 2021. Disponible sur : https://www.e-cancer.fr/Professionnels-de-sante/Recommandations-et-outils-d-aide-a-la-pratique/Cancers-du-sein
15. Vignes S, Arrault M. Prise en charge des patients atteints de lymphœdème. In: Simon D, Traynard PY, Bourdillon F, Gagnayre R, Grimaldi A, Éducation thérapeutique. Paris: Elsevier Masson, 2013, p. 261-70.
16. McNeely ML, Dolgoy ND, Rafn BS, Ghosh S, Ospina PA, Al Onazi MM, et al. Nighttime compression supports improved self-management of breast cancer-related lymphedema: A multicenter randomized controlled trial. Cancer 2022;128(3):587-96.
17. Dayes IS, Whelan TJ, Julian JA, Parpia S, Pritchard KI, D’Souza DP, et al. Randomized trial of decongestive lymphatic therapy for the treatment of lymphedema in women with breast cancer. J Clin Oncol 2013;31(30):3758-63.
18. Vignes S, Albuisson J, Champion L, Constans J, Tauveron V, Malloizel J, et al; French National Referral Center for Primary Lymphedema. Primary lymphedema French National Diagnosis and Care Protocol (PNDS; Protocole National de Diagnostic et de Soins). Orphanet J Rare Dis 2021;16(1):18.
19. Devillers C, de la Brassinne M. Complications cutanées des lymphœdèmes. Rev Med Suisse 2007;136(3):2082-5.
20. Dupuy A, Benchikhi H, Roujeau JC, Bernard P, Vaillant L, Chosidow O, et al. Risk factors for erysipelas of the leg (cellulitis): case-control study. BMJ 1999;318(7198):1591-4.
21. Haute autorité de santé. Synthèse de la recommandation de bonne pratique. Prise en charge des infections cutanées bactériennes courantes. Février 2019. Disponible sur : https://has-sante.fr/upload/docs/application/pdf/2019-03/fiche_de_synthese_infections_cutanees_mel.pdf
22. Ferguson CM, Swaroop MN, Horick N, Skolny MN, Miller CL, Jammallo LS, et al. Impact of ipsilateral blood draws, injections, blood pressure measurements, and air travel on the risk of lymphedema for patients treated for breast cancer. J Clin Oncol 2016;34(7):691-8.
23. Asdourian MS, Swaroop MN, Sayegh HE, Brunelle CL, Mina AI, Zheng H, et al. Association between precautionary behaviors and breast cancer-related lymphedema in patients undergoing bilateral surgery. J Clin Oncol 2017;35(35):3934-41.
24. Prescrire.org. Lymphœdème après cancer du sein : ne pas compliquer inutilement la vie quotidienne. 1er août 2019. Disponible sur : https://www.prescrire.org/fr/3/31/57471/0/NewsDetails.aspx
25. Hasenoehrl T, Palma S, Ramazanova D, Kölbl H, Dorner TE, Keilani M, Crevenna R. Resistance exercise and breast cancer-related lymphedema-a systematic review update and meta-analysis. Support Care Cancer 2020;28(8):3593-603.
26. Rodrick JR, Poage E, Wanchai A, Stewart BR, Cormier JN, Armer JM. Complementary, alternative, and other non-complete decongestive therapy (CDT) treatment methods in the management of lymphedema: a systematic search and review. PM R 2014 ;6(3):250-74; quiz 274.
27. Tran K, Argáez C. Intermittent pneumatic compression devices for the management of lymphedema: A review of clinical effectiveness and guidelines [Internet]. Ottawa (ON): Canadian Agency for Drugs and Technologies in Health; 2017 May 12.
28. Chang DW, Dayan J, Greene AK, MacDonald JK, Masia J, Mehrara B, et al. Surgical treatment of lymphedema: A systematic review and meta-analysis of Controlled trials. Results of a consensus conference. Plast Reconstr Surg 2021;147(4):975-93.
Dans cet article
- Primaire ou secondaire ?
- Affirmer le diagnostic de lymphœdème primaire
- Physiothérapie décongestive, clé de la prise en charge
- Personnaliser le traitement grâce à l’éducation thérapeutique
- Indispensable port d’une compression élastique au long cours
- Érysipèle, la plus fréquente des complications
- Des conseils hygiénodiététiques actualisés
- Susciter l’adhésion du patient pour la prise en charge sur le long terme