Les situations d’urgence en dermatologie pédiatrique sont variées et fréquentes. Il est essentiel pour le médecin généraliste de savoir repérer immédiatement des lésions purpuriques ou des décollements bulleux en particulier, et d’envisager une possible maltraitance devant des lésions incompatibles avec l’anamnèse. Le caractère aspécifique de certains symptômes peut faire retarder la prise en charge devant la diversité de leurs causes possibles. Le type de lésion et l’état général de l’enfant permettent au moins de déterminer si la situation relève d’une urgence thérapeutique ou non.
La peau est l’organe le plus accessible et peut vite susciter une forte inquiétude de la part du médecin, de l’enfant ou de ses parents. Cependant, l’étendue des lésions cutanées n’est pas toujours corrélée à la gravité de la pathologie sous-jacente : une urticaire virale généralisée est spectaculaire mais bénigne, alors qu’un purpura fulminans peut se manifester initialement par une atteinte très discrète. L’examen cutané et muqueux doit donc être minutieux et complet chez un enfant entièrement déshabillé. Le type de lésion élémentaire et l’état général de l’enfant permettent, par une première orientation diagnostique, de décider rapidement si la prise en charge doit être immédiate ou peut être différée (tableau 1 ).
Pathologies engageant le pronostic vital immédiat
Purpura fulminans
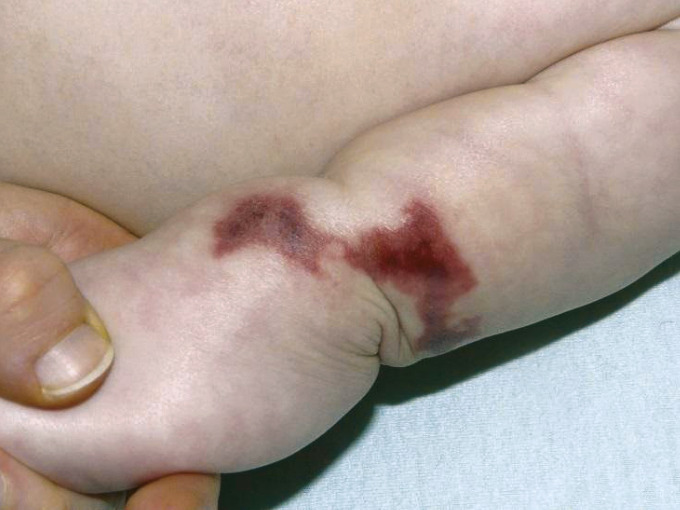
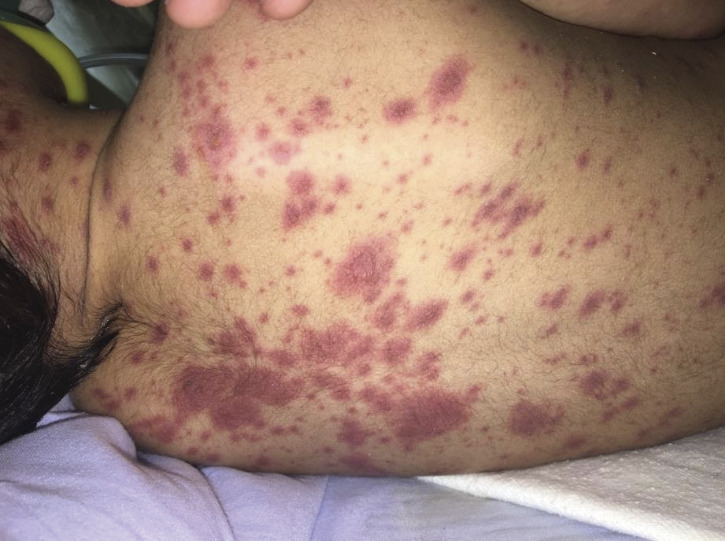
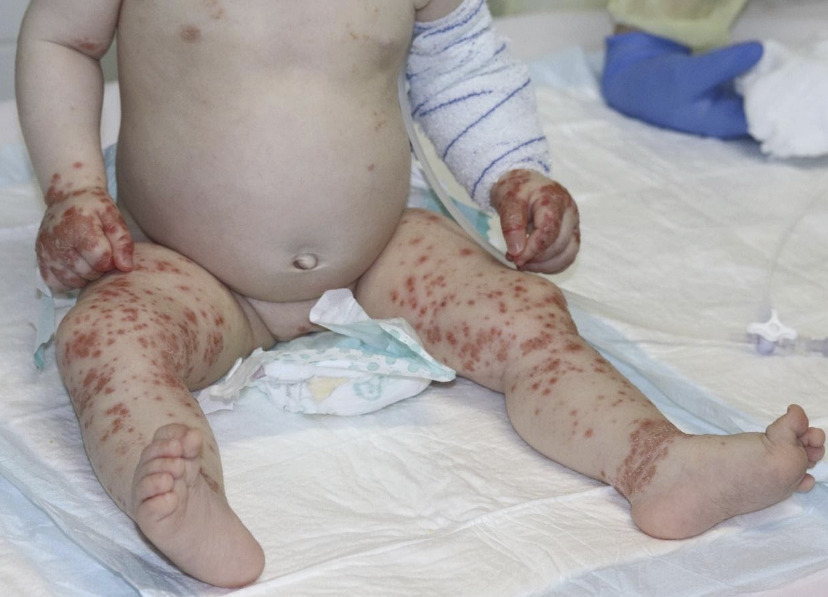
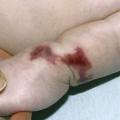
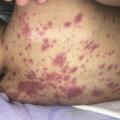
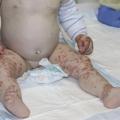
Urgence vitale, ce diagnostic doit être évoqué devant tout purpura fébrile. Il est le plus souvent lié à une infection invasive à méningocoque B ou C favorisée par une infection virale des voies respiratoires hautes concomitante, comme la grippe. Le purpura fulminans peut également être secondaire à d’autres agents infectieux (pneumocoque ou, plus rarement, varicelle). Les premières lésions cutanées sont parfois discrètes : pétéchies, macules érythémateuses ou purpura classiquement en « étoile », d’apparition brutale, prédominant souvent aux extrémités (fig. 1 ). L’extension peut être très rapide (« fulminante »). Les symptômes associés initiaux sont peu spécifiques (irritabilité, douleurs des membres inférieurs, douleurs abdominales ou nausées). L’absence de syndrome méningé n’élimine pas l’hypothèse d’une méningococcémie. La survenue de signes de choc peut être rapide : tachycardie, polypnée, altération de la conscience et temps de recoloration cutanée augmenté. L’hypotension est de survenue plus tardive et impose une prise en charge sans délai.
Une antibiothérapie systémique précoce (ceftriaxone à la dose de 50-100 mg/kg, ou céfotaxime à 50 mg/kg ou, à défaut, amoxicilline à 25-50 mg/kg) est recommandée avant même le transfert à l’hôpital devant tout purpura rapidement extensif ou comportant au moins un élément nécrotique ou ecchymotique de diamètre supérieur ou égal à 3 mm. La trousse d’urgence du médecin généraliste doit donc contenir de la ceftriaxone. Le traitement du choc (remplissage, amines, correction de l’hypoglycémie) doit être débuté le plus rapidement possible, et l’enfant vite pris en charge dans un service de réanimation prévenu de son arrivée, après un transport médicalisé par Samu.
Une antibiothérapie systémique précoce (ceftriaxone à la dose de 50-100 mg/kg, ou céfotaxime à 50 mg/kg ou, à défaut, amoxicilline à 25-50 mg/kg) est recommandée avant même le transfert à l’hôpital devant tout purpura rapidement extensif ou comportant au moins un élément nécrotique ou ecchymotique de diamètre supérieur ou égal à 3 mm. La trousse d’urgence du médecin généraliste doit donc contenir de la ceftriaxone. Le traitement du choc (remplissage, amines, correction de l’hypoglycémie) doit être débuté le plus rapidement possible, et l’enfant vite pris en charge dans un service de réanimation prévenu de son arrivée, après un transport médicalisé par Samu.
Chocs toxiniques staphylococcique et streptococcique
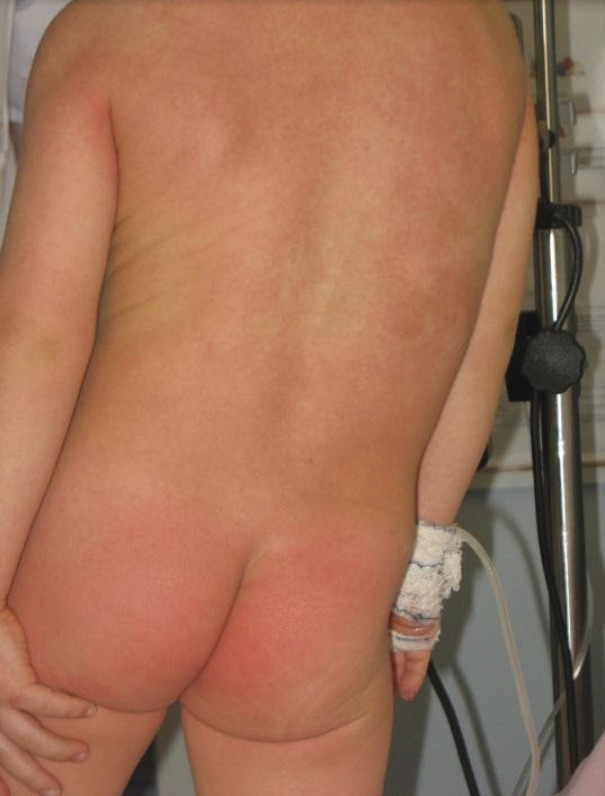
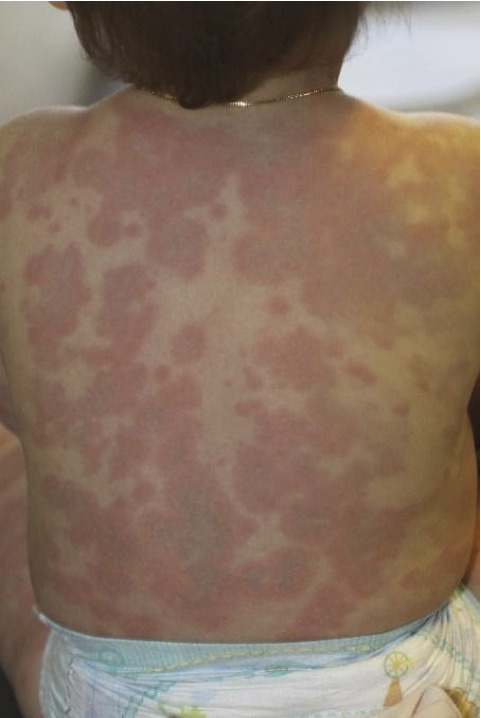
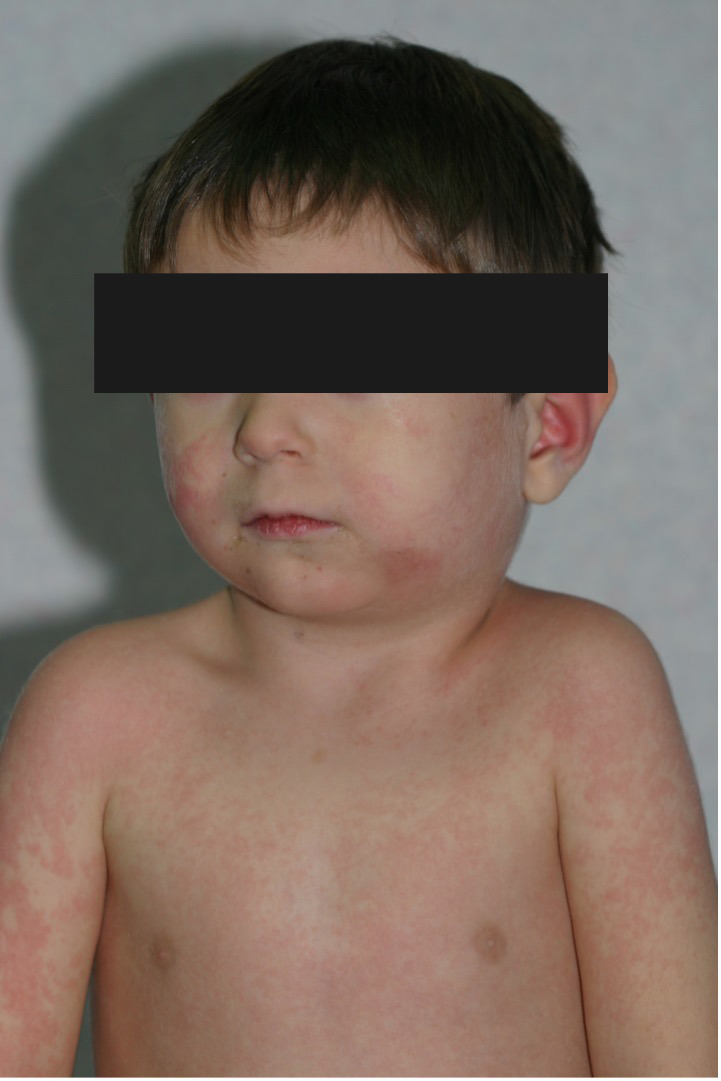
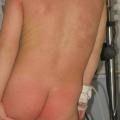
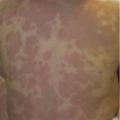
Certaines toxines (toxic shock syndrome toxin 1 [TSST-1] ou entérotoxines du staphylocoque doré ; exotoxines A, B, C du streptocoque A) peuvent être responsables d’un syndrome toxinique redoutable. Il se manifeste par une éruption cutanée érythémateuse scarlatiniforme (confluente, peu d’intervalles de peau saine, avec renforcement au niveau des grands plis, ou prédominante au périnée ; fig. 2 ), accompagnée de fièvre élevée mal tolérée, d’un énanthème muqueux (langue framboisée, conjonctivite) et souvent de douleurs abdominales avec diarrhées. La porte d’entrée de la bactérie peut être cutanée ou muqueuse : infection ORL, plaie cutanée, varicelle, port prolongé de tampon hygiénique chez l’adolescente (choc toxinique staphylococcique menstruel).
Dans les formes sévères du choc toxinique, une défaillance hémodynamique ou multiviscérale peut conduire au décès. Le traitement consiste à diminuer l’inoculum bactérien sécréteur de toxine par traitement de la porte d’entrée (parage d’une plaie infectée, retrait d’un tampon hygiénique) et à instaurer une antibiothérapie à visée antitoxinique (clindamycine 40 mg/kg/j en 3 ou 4 prises) et bactéricide (amoxicilline-acide clavulanique 150 mg/kg/j en 3 prises). Le patient doit être admis en réanimation au moins 48 heures pour surveillance et/ou prise en charge d’éventuelles défaillances d’organes. Un traitement par immunoglobulines polyvalentes (à la dose de 2 g/kg) peut être discuté (rôle de « super-antigène » des toxines).
Dans les formes sévères du choc toxinique, une défaillance hémodynamique ou multiviscérale peut conduire au décès. Le traitement consiste à diminuer l’inoculum bactérien sécréteur de toxine par traitement de la porte d’entrée (parage d’une plaie infectée, retrait d’un tampon hygiénique) et à instaurer une antibiothérapie à visée antitoxinique (clindamycine 40 mg/kg/j en 3 ou 4 prises) et bactéricide (amoxicilline-acide clavulanique 150 mg/kg/j en 3 prises). Le patient doit être admis en réanimation au moins 48 heures pour surveillance et/ou prise en charge d’éventuelles défaillances d’organes. Un traitement par immunoglobulines polyvalentes (à la dose de 2 g/kg) peut être discuté (rôle de « super-antigène » des toxines).
Choc anaphylactique
Le choc anaphylactique est peu fréquent chez l’enfant, et rarement inaugural. Il survient le plus souvent dans un contexte d’allergie connue (arachide, crustacés, bêtalactamines, etc.). L’association d’une urticaire ou d’un angiœdème avec des signes hémodynamiques (tachycardie, hypotension), une forte agitation ou des signes respiratoires (bronchospasme) doit faire évoquer une anaphylaxie et conduire à l’administration immédiate d’adrénaline (0,01 mg/kg en intramusculaire), qui peut être renouvelée en cas de persistance des symptômes. La trousse d’urgence du médecin généraliste doit donc contenir de l’adrénaline (éventuellement en stylo auto-injectable). En raison du risque de réaction biphasique, le patient est ensuite surveillé en service de soins continus.
Pathologies pouvant nécessiter une orientation vers un service d’urgences pédiatriques
Purpura
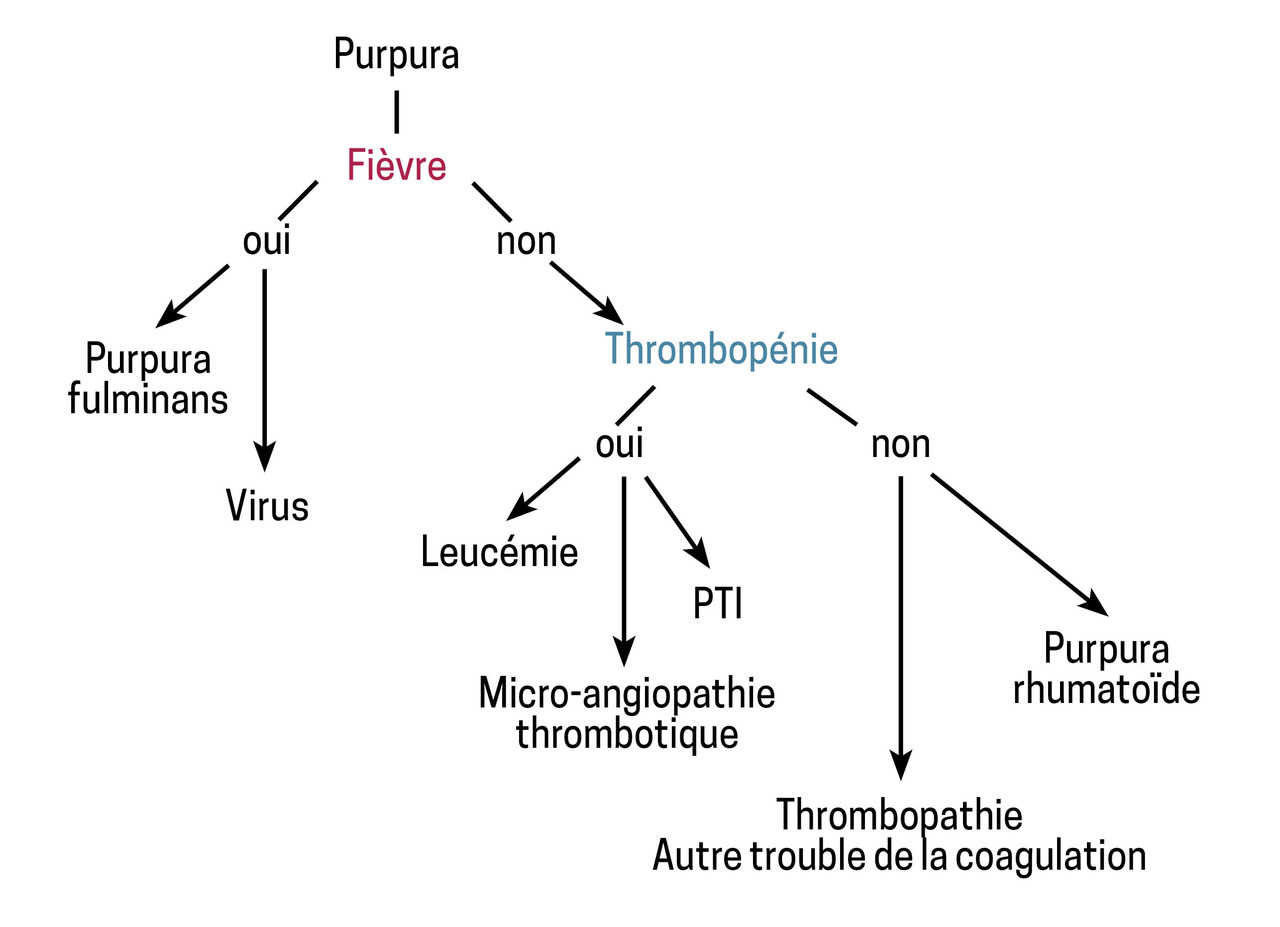
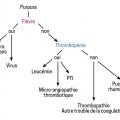
Tout purpura fébrile doit faire immédiatement évoquer un purpura fulminans. Une fois cette urgence vitale éliminée, les autres causes de lésions purpuriques sont envisagées. La démarche diagnostique distingue alors le purpura hématologique du purpura vasculaire, selon les signes cliniques et le bilan biologique de coagulation (fig. 3 ).
Dans les micro-angiopathies thrombotiques, la thrombopénie s’accompagne d’une anémie hémolytique, d’un syndrome œdémateux et de diarrhées glairo-sanglantes.
Plus fréquemment, la thrombopénie est isolée et fait poser le diagnostic de purpura thrombopénique idiopathique (PTI). La décision thérapeutique (immunoglobulines polyvalentes ou corticothérapie en l’absence de cause tumorale) dépend du score de Buchanan (tableau 2 ) et de la numération plaquettaire. Chez le grand enfant et en cas d’antécédents familiaux de maladies auto-immunes, un bilan immunologique est nécessaire.
L’œdème aigu hémorragique du nourrisson, considéré comme un équivalent de purpura rhumatoïde, se manifeste par l’apparition rapide et prédominante de lésions purpuriques en cocarde ou en nappes aux extrémités, associées à un œdème, chez un enfant de moins de 2 ans à l’état général conservé.
Un purpura pétéchial et ecchymotique en nappe, non infiltré, des lésions muqueuses pétéchiales ou bulleuses hémorragiques, des saignements spontanés ou pour des traumatismes minimes sont en faveur d’un trouble de la coagulation.
En cas de thrombopénie
Il faut rechercher un syndrome tumoral (hépatosplénomégalie, adénopathies, altération de l’état général) et une atteinte des autres lignées sanguines par envahissement médullaire.Dans les micro-angiopathies thrombotiques, la thrombopénie s’accompagne d’une anémie hémolytique, d’un syndrome œdémateux et de diarrhées glairo-sanglantes.
Plus fréquemment, la thrombopénie est isolée et fait poser le diagnostic de purpura thrombopénique idiopathique (PTI). La décision thérapeutique (immunoglobulines polyvalentes ou corticothérapie en l’absence de cause tumorale) dépend du score de Buchanan (
Purpura vasculaire
Il est plus déclive et infiltré et n’atteint pas les muqueuses. Le purpura rhumatoïde, vascularite à dépôts d’IgA touchant plutôt le jeune enfant, associe des arthralgies et des douleurs abdominales à un purpura vasculaire avec œdème, prédominant aux extrémités et favorisé par l’orthostatisme et l’activité physique. L’atteinte cutanée du siège et l’orchite sont très évocatrices. La bandelette urinaire est régulièrement contrôlée, à la recherche de protéinurie ou d’hématurie. La corticothérapie est indiquée seulement en cas d’atteinte viscérale grave (hématome de paroi, invagination intestinale aiguë, orchite, néphropathie glomérulaire).L’œdème aigu hémorragique du nourrisson, considéré comme un équivalent de purpura rhumatoïde, se manifeste par l’apparition rapide et prédominante de lésions purpuriques en cocarde ou en nappes aux extrémités, associées à un œdème, chez un enfant de moins de 2 ans à l’état général conservé.
Un purpura pétéchial et ecchymotique en nappe, non infiltré, des lésions muqueuses pétéchiales ou bulleuses hémorragiques, des saignements spontanés ou pour des traumatismes minimes sont en faveur d’un trouble de la coagulation.
Autres causes
Après avoir éliminé ces principales causes de purpura, on s’oriente vers une origine mécanique (purpura du visage après effort de toux ou de vomissements) ou vers une origine virale (infection par le Parvovirus B19, rougeole purpurique, etc.). La prise en charge n'a pas alors le même caractère d'urgence, sauf altération de l’état général associé.Vésicules, bulles et décollements cutanés douloureux
Épidermolyse bulleuse staphylococcique
Chez le nourrisson et l’enfant, la première cause de dermatose bulleuse est l’infection par Staphylococcus aureus, par production d’exfoliatines A ou B, toxines responsables du clivage et du décollement superficiel intra-épidermique. Le staphylocoque n’est pas présent dans les bulles, et les bactériémies sont rares. La toxine se diffuse par voie sanguine à partir d’un foyer infectieux cutané (omphalite, plaie, impétigo) ou ORL. L’apparition de fièvre et d’un exanthème scarlatiniforme est suivie dans les vingt-quatre heures par une desquamation ou un décollement prédominant autour du foyer infectieux initial ou aux zones de frottement (siège, creux axillaires, plis inguinaux).Dans les formes sévères (staphylococcal scalded skin syndrome [SSSS]), l’enfant est irritable, douloureux, et l’érythrodermie « en coup de soleil », suivie d’un décollement généralisé avec signe de Nikolsky, donne un aspect de peau « ébouillantée » (
Syndromes de Lyell et de Stevens-Johnson
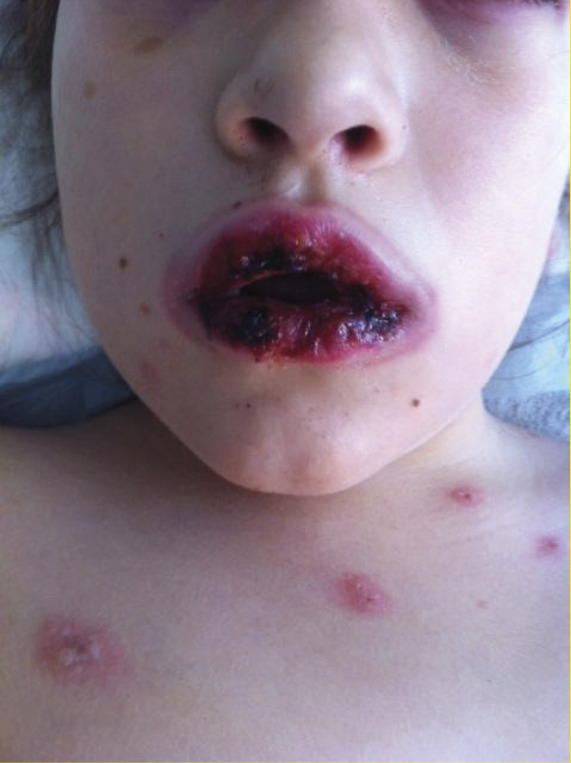
Dans la nécrolyse épidermique toxique (syndrome de Lyell) ou le syndrome de Stevens-Johnson, une fièvre élevée, une kératoconjonctivite et des érosions muqueuses multifocales sont suivies en quelques jours d’une éruption cutanée maculeuse douloureuse, purpurique ou en pseudococardes, qui débute au visage et au tronc avant de confluer (Selon la surface cutanée atteinte, on distingue le syndrome de Stevens-Johnson (décollement < 10 %) du syndrome de Lyell (> 30 %). Un décollement de l’épithélium digestif ou pulmonaire peut être associé. Les causes de nécrolyse épidermique sont surtout médicamenteuses (anticomitiaux, cotrimoxazole et certains anti-inflammatoires non stéroïdiens). Les symptômes apparaissent entre le 7e et le 21e jour d’introduction. Chez l’enfant, le mycoplasme peut également être en cause. L’importance du décollement cutané met en jeu le pronostic vital (risque de pertes hydro-électrolytiques et de surinfections bactériennes). Outre l’arrêt des médicaments suspects, la prise en charge associe antalgiques, compensation des pertes hydriques et prévention des surinfections. Les synéchies doivent être éliminées quotidiennement, en particulier au niveau des yeux, les séquelles à long terme étant essentiellement liées à l’atteinte oculaire et aux synéchies muqueuses.
L’érythème polymorphe majeur est parfois difficile à distinguer du syndrome de Stevens-Johnson. L’état général est habituellement conservé, et l’atteinte muqueuse (buccale, génitale et oculaire) y est fréquente mais moins grave (
L’atteinte cutanée est plus distale, à disposition symétrique et classiquement en cocardes à centre bulleux, elle doit être distinguée de l’urticaire annulaire et échymotique du nourrisson qui peut donner un aspect en cocardes mais avec des lésions fugaces sans évolution bulleuse (
Les causes sont habituellement infectieuses (mycoplasme, herpès), et les récurrences sont fréquentes.
Eczéma herpeticum et eczéma coxsackium
L’eczéma herpeticum (anciennement appelé « pustulose varioliforme de Kaposi-Juliusberg ») correspond à la surinfection d’une dermatite atopique par Herpes simplex virus de type 1 (HSV1). Il doit être évoqué devant une modification rapide des lésions cutanées (apparition de vésiculo-pustules ombiliquées, confluentes et douloureuses), associée à une altération fébrile de l’état général (
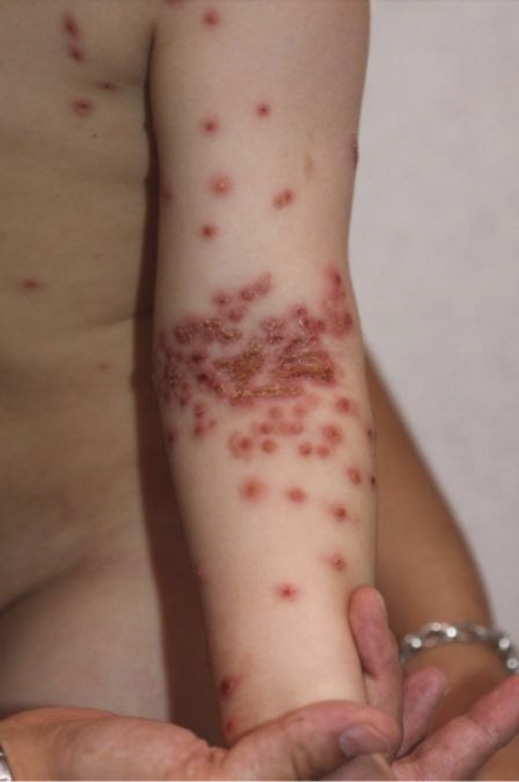
L’eczéma coxsackium correspond à une surinfection des lésions de dermatite atopique chez des enfants d’âge préscolaire par les virus Coxsackie (le plus souvent les souches A6 et A16), souvent au printemps et en été. La symptomatologie est très proche de celle de l’eczéma herpeticum : éruption vésiculeuse, bulleuse ou érosive au niveau des zones atteintes par la dermatite atopique, et plus spécifiquement au niveau des mains, des pieds, du visage (notamment en péribuccal), du tronc, des fesses et de l’aine (
Zona
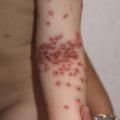
Le zona est la récurrence clinique du virus varicelle-zona (VZV), responsable de la varicelle, survenant en général plusieurs années après. La majorité des cas concernent les enfants de plus de 5 ans. L’éruption, située sur un métamère, est typiquement unilatérale, en plaques érythémateuses vésiculo-bulleuses, pustuleuses, séparées ou confluentes. Les vésicules deviennent ensuite croûteuses ou érosives, parfois nécrotiques. Elles disparaissent en une dizaine de jours, laissant parfois place à des cicatrices hypochromiques et atrophiques.Le zona est le plus souvent hémithoracique de D5 à D12 (50 % des cas), mais tous les métamères ainsi que les nerfs crâniens peuvent être concernés. Des prodromes (fièvre, céphalées) peuvent être observés. Le zona ophtalmique, situé sur le territoire V1 du trijumeau, est une urgence thérapeutique, en raison du risque de complications ophtalmiques. Il nécessite un traitement oral dans les 72 heures suivant l’éruption par aciclovir pendant sept jours (800 mg 5 fois par jour chez l’enfant de plus de 2 ans, et demi-dose avant l’âge de 2 ans), avec une prise en charge ophtalmique urgente, des soins locaux antiseptiques et des antalgiques. Pour tout autre zona métamérique classique, des soins locaux antiseptiques suffisent, car les algies post-zostériennes sont exceptionnelles chez l’enfant.
Gingivostomatite herpétique
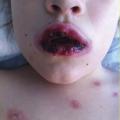
Elle correspond à une primo-infection herpétique, le plus souvent par HSV1. Asymptomatique dans 90 % des cas, l’infection peut rarement débuter par de la fièvre, puis provoquer l’apparition de nombreuses vésicules coalescentes étendues sur la muqueuse buccale et en région péribuccale. Des ulcérations douloureuses à base jaunâtre cernées d’un halo érythémateux y font suite. Les gencives et les lèvres sont érythémateuses, œdématiées et saignent facilement au contact. L’enfant peut avoir une anorexie avec risque de déshydratation. Le diagnostic peut être confirmé par une PCR cutanée sur les vésicules. L’aciclovir doit être administré précocement après le début de l’éruption, pour une durée de cinq à dix jours (100 mg 5 fois par jour avant l’âge de 2 ans ; 200 mg 5 fois par jour après 2 ans). En cas d’anorexie sévère, une hydratation par voie intraveineuse est indiquée.
Exanthème avec fièvre mal tolérée
Maladie de Kawasaki
Il s’agit d’une vascularite systémique touchant principalement les artères de moyen calibre avec un tropisme particulier pour les coronaires. La forme typique touche l’enfant de 6 mois à 5 ans et associe une fièvre en plateau durant plus de cinq jours avec au moins 4 des 5 critères suivants (ABCDE) :– adénopathies cervicales de plus de 1,5 cm, souvent unilatérales ;
– atteinte buccale : pharyngite, angine, chéilite, langue dépapillée ;
– hyperhémie conjonctivale bilatérale non purulente et possible uvéite antérieure ;
– atteinte des extrémités, avec érythème palmoplantaire vers le 5e jour, œdème vers le 7e jour, puis desquamation des extrémités (doigts et orteils, parfois palmoplantaire) au cours de la 3e semaine suivant le début des symptômes ;
– éruption cutanée polymorphe : exanthème urticarien avec pseudococardes, morbiliforme, scarlatiniforme ou purpurique ; fréquente atteinte du siège (érythème « en culotte » bien limité, parfois douloureux, rapidement suivi d’une desquamation périnéale) (
L’altération de l’état général est constante : l’enfant est irritable et difficile à examiner. Les formes incomplètes (fièvre depuis plus de 5 jours avec moins de 4 critères majeurs sur 5) sont plus fréquentes chez les enfants de moins de 6 mois. Les examens complémentaires initiaux peuvent révéler un important syndrome inflammatoire (augmentation de la vitesse de sédimentation [VS] et de la protéine C-réactive [CRP]), une anémie (la thrombocytose est tardive après le 7e jour), une hypoalbuminémie, une cytolyse hépatique, un hydrocholécyste, une leucocyturie aseptique ou une méningite aseptique.
L’échographie cardiaque recherche des anévrismes coronariens, complication principale de la maladie de Kawasaki, survenant habituellement dans les dix à trente jours après le début des symptômes. Le traitement doit être entrepris dès la suspicion diagnostique pour prévenir la survenue des complications coronariennes : dose unique d’immunoglobulines intraveineuses (2 g/kg) et aspirine à dose anti-inflammatoire (30 à 50 mg/kg/j) pendant 48 à 72 heures, puis à dose antiagrégante (3 à 5 mg/kg/j) pendant 6 à 8 semaines (voire plus longtemps en cas d’anévrisme coronarien).
Le suivi est prolongé : la maladie de Kawasaki est en effet la première cause de pathologie cardiaque acquise de l’enfant dans les pays industrialisés.
Syndrome inflammatoire multisystémique pédiatrique
Le syndrome inflammatoire multisystémique pédiatrique (PIMS : pediatric inflammatory multisytem syndrome ; ou MIS-C : multisystem inflammatory syndrome in children) est une maladie inflammatoire récemment décrite dans le contexte de la pandémie de Covid-19. Les premiers cas décrits datent de mars 2020. Il s’agit d’une manifestation post-infectieuse du Covid-19 apparaissant plusieurs semaines après l’infection, décelée par la sérologie dans la majorité des cas. C’est une pathologie rare : entre le 1er mars 2020 et le 22 août 2021, 640 cas ont été signalés, selon Santé publique France.Le tableau clinique est généralement proche de celui de la maladie de Kawasaki : fièvre aiguë souvent mal tolérée de plus de quatre jours, symptômes gastro-intestinaux (douleurs abdominales, vomissements, diarrhées), éruption cutanée polymorphe et, plus rarement, atteinte des muqueuses et modification des extrémités. Les autres critères de la maladie de Kawasaki, tels que les adénopathies cervicales et la conjonctivite, sont plus rares. Certains patients développent un choc cardiogénique par défaillance myocardique qui fait toute la gravité du syndrome, dans les trois à cinq jours suivant le début de la fièvre.
Les examens complémentaires objectivent typiquement une lymphopénie, une thrombopénie, un syndrome inflammatoire majeur ainsi que des signes de souffrance myocardique (troponine et NT-proBNP élevés). Toute suspicion de PIMS doit faire réaliser une échographie cardiaque en urgence pour mettre en place le traitement spécifique si besoin : corticothérapie intraveineuse et perfusion d’immunoglobulines polyvalentes. Malgré la sévérité potentielle de cette pathologie, une prise en charge précoce assure un excellent pronostic à moyen terme à la grande majorité des enfants, sans séquelle cardiaque.
Syndrome DRESS
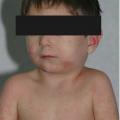
Le syndrome DRESS (drug reaction with hypereosinophilia and systemic symptoms), réaction grave d’hypersensibilité médicamenteuse, survient dans les deux à six semaines suivant l’introduction du médicament responsable. Ce délai peut être raccourci en cas de sensibilisation préalable (par le même médicament ou un apparenté). Les médicaments concernés sont principalement les antiépileptiques (diphénylhydantoïne, phénobarbital, carbamazépine, acide valproïque, lamotrigine), la minocycline, le sulfaméthoxazole, l’allopurinol ou la dapsone. La réaction d’hypersensibilité serait favorisée par une infection ou une réactivation aux virus Herpes (cytomégalovirus, virus d’Epstein-Barr, virus herpès humain de type 6).Un syndrome DRESS doit être évoqué devant l’apparition brutale d’une fièvre élevée mal tolérée avec malaises, d’un œdème facial, périorbitaire et du cou, d’un exanthème maculopapuleux prurigineux du tronc et de la racine des membres, voire d’une érythrodermie, et de polyadénopathies avec souvent une hépatosplénomégalie. L’atteinte buccale (énanthème ou pharyngite) peut être responsable d’une dysphagie. Plus rarement, l’atteinte cutanée peut comporter des pustules, des vésicobulles ou un purpura.
Rare chez l’enfant, le diagnostic en est parfois retardé.
Le bilan biologique recherche une hyperleucocytose avec lymphocytes atypiques, une hyperéosinophilie (souvent supérieure à 1,5 G/L), une cytolyse hépatique ou une atteinte rénale.
L’atteinte viscérale (hépatite fulminante avec insuffisance hépatocellulaire, néphrite interstitielle, pneumopathie interstitielle, myocardite) signe une forme grave, devant être traitée par corticothérapie systémique.
Les traitements suspects (ainsi que les traitements apparentés à risque de réaction croisée) doivent être arrêtés et contre-indiqués jusqu’à une consultation d’allergologie spécialisée.
Viroses : rougeole et varicelle surinfectées
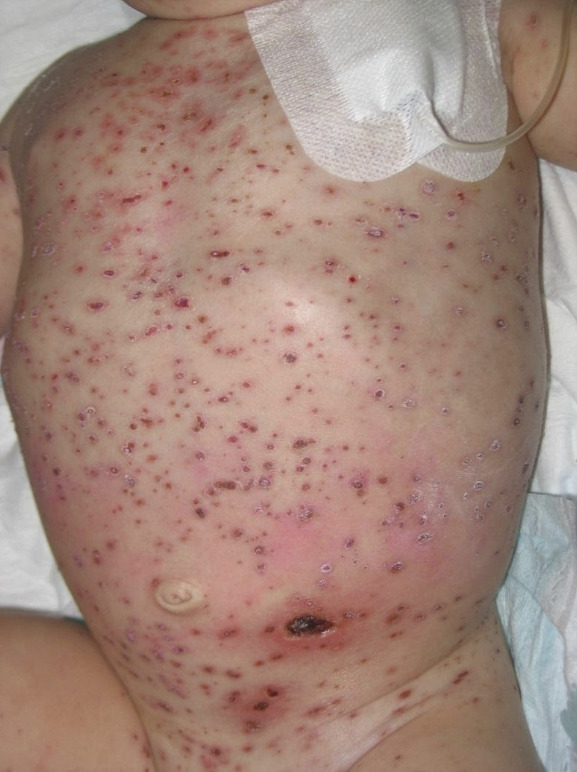
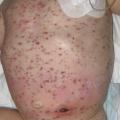
Du fait d’une couverture vaccinale insuffisante, des cas de rougeole surviennent encore en France. La phase d’invasion (fièvre élevée, asthénie, catarrhe oculonasal, toux) dure quatre à sept jours et survient sept à quinze jours après un contage aérien ou par contact. L’éruption apparaît en moyenne quatorze jours après le contage. Le signe de Köplick (maculopapules blanchâtres sur fond érythémateux à la face interne des joues en regard des molaires) est pathognomonique, mais inconstant et fugace. Apparaît ensuite un exanthème maculopapuleux rétro-auriculaire qui progresse en trois jours au tronc, à la racine des membres, puis aux extrémités. Il disparaît en cinq à six jours. Le patient est considéré contagieux cinq jours avant et jusqu’à cinq jours après le début de l’éruption cutanée. La rougeole favorise les surinfections (otites notamment) et peut se compliquer d’atteintes graves (pneumopathie, encéphalite, ou cécité en cas de carence en vitamine A). Le traitement est symptomatique, sauf pour les patients immunodéprimés, les femmes enceintes et les enfants de moins de 6 mois dont la mère n’est pas immunisée, pour lesquels un traitement par immunoglobulines polyvalentes est recommandé. Les vaccinations de l’entourage doivent être mises à jour, et une déclaration obligatoire doit être faite à l’agence régionale de santé.Les symptômes de varicelle débutent dix à vingt et un jours après un contage par gouttelettes ou contact : fièvre souvent modérée, suivie d’une éruption prurigineuse et vésiculeuse sur fond érythémateux débutant au cuir chevelu puis s’étendant au reste du corps, avec possibles ulcérations buccales rendant difficile l’alimentation. La persistance ou la survenue secondaire de fièvre élevée et mal tolérée doit faire évoquer une surinfection ORL, pulmonaire ou cutanée favorisée par les démangeaisons (
Maladies inflammatoires : lupus et dermatomyosite
Le lupus se révèle rarement dans l’enfance, mais, si c’est le cas, il est souvent plus sévère au diagnostic que chez l’adulte. Des signes généraux (fièvre, altération de l’état général) s'associent aux divers tableaux cutanés. Le lupus aigu se manifeste par une éruption érythémateuse œdémateuse, parfois squameuse et papuleuse, localisée au décolleté et au visage (éruption en « loup » ou en « ailes de papillon » épargnant les sillons nasogéniens et la région périorale) et aux autres zones photo-exposées. L’atteinte du dos des mains prédomine aux zones interarticulaires, à la différence de la dermatomyosite. L’apparition de lésions buccales érosives peut gêner l’alimentation. Un phénomène de Raynaud, un livedo des membres inférieurs et des engelures sont possibles. Comme pour l’adulte, il existe des atteintes extracutanées : polyarthrite, cytopénie auto-immune, épanchement des séreuses (pleurésie, péricardite), symptômes neuropsychiatriques ou digestifs ; l’atteinte rénale est plus fréquente chez l’enfant que chez l’adulte, et d’emblée sévère.La dermatomyosite juvénile est une vascularite systémique auto-immune associant une atteinte des muscles striés, une atteinte cutanée et des signes généraux (asthénie, amaigrissement, fièvre). L’atteinte cutanée prédomine sur les zones photo-exposées. On peut observer au niveau du visage un érythème lilacé périorbitaire pathognomonique, un œdème palpébral ou facial, plus rarement une alopécie squameuse. L’érythème violacé des zones d’extension (genoux, coudes) est majoré par l’exposition solaire. L’examen des mains peut montrer un érythème violacé en bande (sur le dos des articulations interphalangiennes ou métacarpophalangiennes) papuleux, voire squameux (papules de Gottron), un érythème périunguéal douloureux à la palpation avec atteinte des cuticules, des télangiectasies périunguéales ou des lésions de vascularite nécrotiques. La maladie se manifeste par l’apparition progressive d’un déficit musculaire symétrique prédominant aux racines des membres, une fatigabilité à l’effort, des myalgies d’horaire inflammatoire et une amyotrophie. En cas d’atteinte sévère, les muscles de l’oropharynx ou le diaphragme peuvent être touchés, entraînant voix nasonnée, troubles de la déglutition ou insuffisance respiratoire. Les atteintes cardiaque ou digestive sont possibles et graves. Les bilans biologiques mettent en évidence un syndrome inflammatoire (augmentation de la VS et de la CRP) et une cytolyse musculaire (augmentation des créatine phosphokinase [CPK], transaminases ASAT et lactate déshydrogénase [LDH]).
Placard inflammatoire douloureux
Érysipèle, fasciite nécrosante
L’érysipèle débute par l’apparition d’un placard érythémateux induré et douloureux, rapidement progressif, parfois limité par un bourrelet périphérique et accompagné de pics fébriles. Une traînée de lymphangite ou des adénopathies satellites signent l’extension locorégionale. Il est le plus souvent dû à une infection streptococcique. La porte d’entrée est à rechercher : plaie cutanée, traumatisme, morsure, lésion de varicelle, intertrigo, etc. Le traitement associe soins locaux et antibiothérapie (amoxicilline-acide clavulanique avec 80 mg/kg/j d’amoxicilline, en 3 prises pendant 7 jours).La présence de douleurs intenses, de troubles sensitivomoteurs débutant par une hypoesthésie, de troubles vasculaires, de lésions purpuriques ou bulleuses, d’une crépitation neigeuse à la palpation et des signes généraux de sepsis sévère font craindre une fasciite nécrosante, habituellement multibactérienne. La prise en charge est alors médicochirurgicale : parage précoce des tissus nécrosés sans que l’antibiothérapie intraveineuse en soit retardée.
Dermohypodermites staphylococciques
Chez le petit enfant, les dermohypodermites staphylococciques (Écthyma gangréneux
Il apparaît initialement comme une lésion vésiculopustuleuse évoluant vers une bulle hémorragique puis vers une ulcération non douloureuse à centre nécrotique noir entouré d’un halo érythémateux. Il est principalement dû à la bactérie Pseudomonas aeruginosa, dont la diffusion se fait par voie hématogène ou par contiguïté au niveau du périnée, chez un patient immunodéprimé (neutropénie profonde le plus souvent) et fébrile.Le traitement associe une antibiothérapie adaptée (ceftazidime et aminoside), des soins chirurgicaux si besoin et la prise en charge de l’immunosuppression (facteurs de croissance granulocytaires).
Syndrome du tourniquet ou du « cheveu étrangleur »
L’apparition brutale d’un œdème érythémateux et douloureux d’un orteil, d’un doigt ou du pénis d’un nourrisson peut être liée à la striction cutanée par un cheveu ou un fil, dont le retrait doit être rapide pour éviter la nécrose.Brûlures
La prise en charge immédiate consiste à refroidir la zone brûlée par rinçage abondant (en faisant couler l’eau sur la lésion durant au moins 15 minutes avec une eau entre 15 et 25 °C), retirer les vêtements (sauf s’ils collent à la peau) puis couvrir la brûlure d’un linge propre. L’évaluation de la surface corporelle atteinte (table de Lund et Browder) et de la profondeur (degré) guident la suite de la prise en charge : cicatrisation dirigée (atteinte superficielle) ou traitement chirurgical précoce (atteinte profonde) par détersion des tissus nécrosés et greffe de peau. Le suivi doit être prolongé en raison du risque de séquelles à long terme : brides et rétractions (traitées par chirurgie, attelles), cicatrices hypertrophiques (nécessitant massages avec une crème cicatrisante, vêtements compressifs) ou hyperpigmentées (imposant une protection solaire).
Tumeur de croissance rapide
Hémangiome à risque
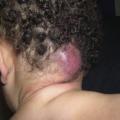
L’hémangiome infantile, tumeur vasculaire bénigne, apparaît dans les semaines suivant la naissance comme une tuméfaction ferme, élastique, indolore, chaude et non pulsatile. Il peut être superficiel (de couleur rouge vif et saillant sur une peau normale), profond (tuméfaction recouverte d’une peau normale ou bleutée), ou mixte. Après une phase de croissance puis de stagnation, la majorité des hémangiomes involue spontanément en laissant souvent une séquelle esthétique.L’ulcération est la complication la plus fréquente et survient préférentiellement sur les hémangiomes faciaux ou périnéaux, entraînant d’importantes douleurs et un risque cicatriciel. Elle est aussi favorisée par d'autres facteurs : phase de croissance de l’hémangiome, taille étendue, croissance rapide, distribution segmentaire, forme superficielle et télangiectasique.
La survenue d’une détresse respiratoire chez un nourrisson peut être liée à une obstruction des voies aériennes supérieures par un hémangiome sous-glottique, parfois associé à un hémangiome en « barbe ». Enfin, la croissance d’un hémangiome en zone périorificielle est susceptible d’entraîner une séquelle fonctionnelle : strabisme, amblyopie (hémangiome palpébral, péri- ou rétro-orbitaire) ; déformation de la cloison nasale ; surdité par obstruction du conduit auditif ; altération du bourgeon mammaire.
Une hémangiomatose multifocale, associant au moins cinq hémangiomes, doit faire pratiquer une échographie abdominale à la recherche d’hémangiomes hépatiques qui peuvent se compliquer d’insuffisance cardiaque à haut débit ou d’hypothyroïdie. Enfin, un hémangiome de localisation segmentaire peut s’associer à d’autres anomalies de développement extracutanées dans le cadre d’un syndrome PHACES (hémangiome de plus de 5 cm² localisé sur la tête, le cou ou la partie supérieure du thorax) ou d’un syndrome PELVIS (ou SACRAL, hémangiome périnéal ou lombosacré).
Le traitement oral par bêtabloquant (propranolol 3 mg/kg/j en 2 prises) est indiqué pour tout hémangiome à risque fonctionnel ou vital et est proposé en cas de risque de séquelle esthétique importante.
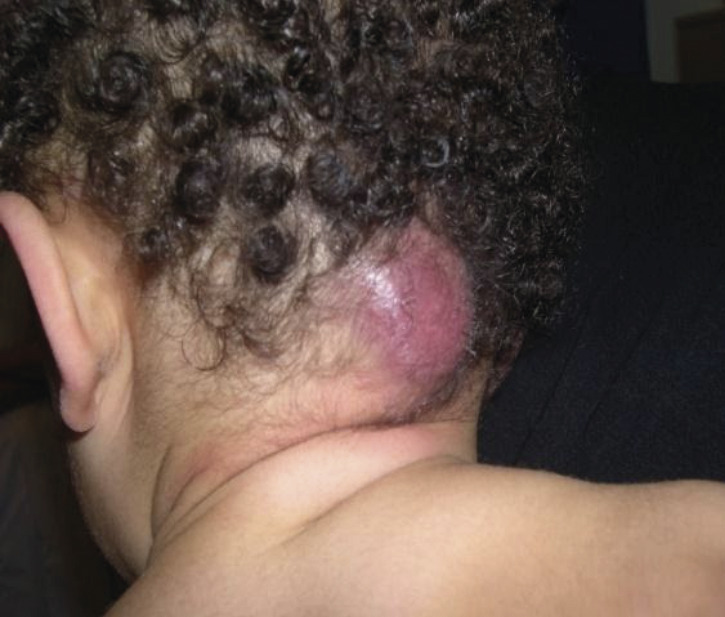
Tumeurs malignes (lymphome, leucémie, neuroblastome)
L’apparition de papules ou de nodules indurés brun-rouge ou violacés, indolores, préférentiellement localisées sur le crâne doit faire évoquer la possibilité de tumeurs malignes : leucémie aiguë (Signes de maltraitance
Il est impératif de savoir évoquer une maltraitance devant un comportement inapproprié de l’enfant, une méfiance de sa famille, un délai tardif de consultation, une anamnèse discordante avec les signes cliniques constatés, des lésions suspectes ou de localisation inhabituelle (voir fiche p. 393 « Signes dermatologiques chez l’enfant : savoir évoquer une maltraitance » ).
Encadre
Ce qu’il faut dire aux patients
Toute éruption associée à une altération de l’état général doit faire consulter en urgence.
L’étendue des lésions cutanées n’est pas toujours corrélée à la gravité.
Une brûlure doit être immédiatement refroidie (sous l’eau courante à 15 °C pendant au moins 15 minutes).
Le calendrier vaccinal de l’enfant doit être rigoureusement suivi pour prévenir les maladies infectieuses graves.
Pour en savoir plus :
Aractingi S, Dupin N, Petit A. Thérapeutique dermatologique. Un manuel de référence en dermatologie. En ligne, disponible sur
https://www.therapeutique-dermatologique.org/
Cohen R (coord.), Groupe de pathologie infectieuse pédiatrique. Guide de prescription d’antibiotique en pédiatrie. Archives de pédiatrie 2016;23:S1-S55.
HAS, SPILF. Prise en charge des infections cutanées bactériennes courantes. Volet 1. Synthèse de la recommandation de bonne pratique. Février 2019. Rev Prat Med Gen 2019;33(1032);869-70.
HAS, SPILF. Prise en charge des infections cutanées bactériennes courantes. Volet 2. Synthèse de la recommandation de bonne pratique. Février 2019. Rev Prat Med Gen 2020;34(1033);9-10.
Orphanet, portail des maladies rares : https://www. orpha.net/consor/cgi-bin/index.php
Cohen R (coord.), Groupe de pathologie infectieuse pédiatrique. Guide de prescription d’antibiotique en pédiatrie. Archives de pédiatrie 2016;23:S1-S55.
HAS, SPILF. Prise en charge des infections cutanées bactériennes courantes. Volet 1. Synthèse de la recommandation de bonne pratique. Février 2019. Rev Prat Med Gen 2019;33(1032);869-70.
HAS, SPILF. Prise en charge des infections cutanées bactériennes courantes. Volet 2. Synthèse de la recommandation de bonne pratique. Février 2019. Rev Prat Med Gen 2020;34(1033);9-10.
Orphanet, portail des maladies rares : https://www. orpha.net/consor/cgi-bin/index.php

 Encadrés
Encadrés