Le contact avec la nature n’est pas sans danger et impose toujours quelques précautions
L’urbanisation aidant, les activités de loisirs sont davantage orientées vers le plein air (promenade, baignades) et/ou la mise en contact avec des animaux (visite de fermes pédagogiques, colombophilie…). Elles peuvent exposer à des risques zoonotiques, en facilitant le rapprochement (ou les interactions directes ou indirectes) entre l’homme et les animaux sauvages et/ou domestiques. La méconnaissance de certains dangers par des populations urbaines, voire une certaine idéalisation de la nature, peuvent même conduire à une augmentation du risque. L’objet de cet article est de donner un bref aperçu des principales zoonoses pouvant être contractées dans le cadre d’activités de loisirs.1
Zoonoses associées aux piqûres de tique
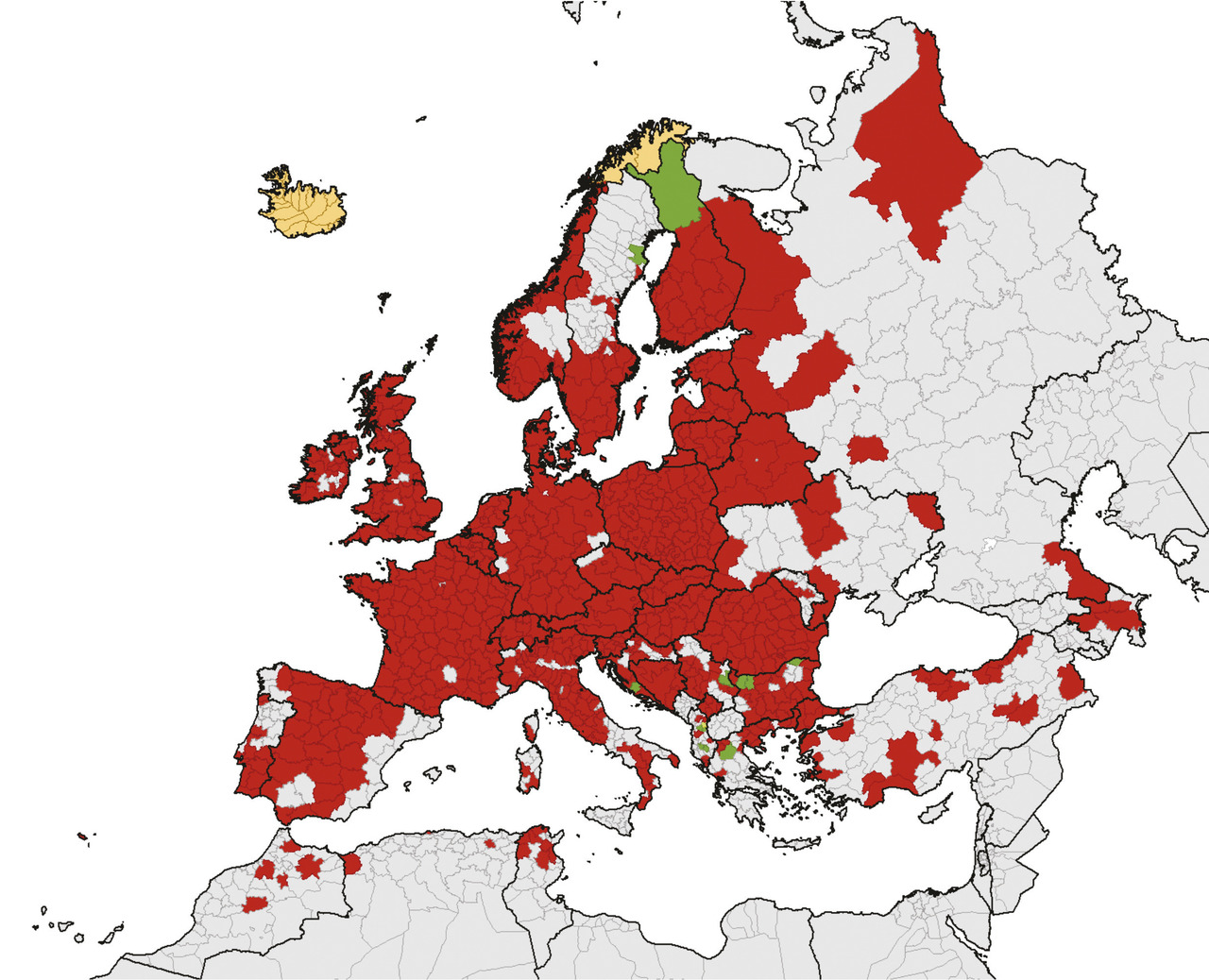
Se promener et plus encore s’asseoir dans des zones herbeuses expose inévitablement à des piqûres de tique durant les saisons où elles sont actives (été et automne), en particulier à la piqûre d’Ixodes ricinus (fig. 1), espèce la plus répandue (fig. 2) et la plus impliquée dans la transmission d’agents vectorisés dans les zones tempérées d’Europe occidentale.
La fièvre Q et la tularémie sont également transmissibles par piqûre de tique, essentiellement I. ricinus, mais c’est une modalité de transmission qui reste rare (v. infra).
Maladie de Lyme
C’est la plus connue des zoonoses concernées. Elle est causée par diverses bactéries du genre Borrelia, trouvées chez de nombreuses espèces de mammifères sauvages, notamment les micromammifères* et même d’oiseaux sauvages, ainsi que chez environ 10 % des I. ricinus testées en France, lesquelles jouent également le rôle de réservoir, la femelle adulte infectée étant capable de transmettre la bactérie à sa descendance (transmission transovarienne). Environ 27 000 cas humains sont déclarés par an.** À l’échelle individuelle, des mesures de prévention sont préconisées (v. tableau). Une meilleure connaissance épidémiologique s’impose, à la fois chez l’homme et chez I. ricinus, en vue d’une maîtrise accrue du risque. Un Plan national de lutte a été mis en place en 2016,2 avec diverses actions orientées vers la recherche, le diagnostic précoce, la prise en charge des malades, la prévention et la surveillance.Encéphalite à tiques
Parmi les autres maladies concernées par ce plan, l’encéphalite à tiques, endémique en Europe centrale et de l’Est, figure en bonne place. En effet, si les cas humains signalés en France, surtout dans l’Est, restent sporadiques, une accélération récente est perceptible, et l’émergence de l’encéphalite à tiques est très sensible dans deux pays voisins, les Pays-Bas et la Suisse. L’encéphalite à tiques est due à un Flavivirus, le tick-borne encephalitis virus (TEBV), dont le vecteur principal en France est I. ricinus, qui est aussi réservoir (transmission transovarienne). Des micromammifères sont également impliqués dans la pérennisation du virus dans la nature. L’homme est surtout contaminé par piqûre de tique, même si les ruminants domestiques peuvent excréter le virus dans leur lait. Un vaccin efficace permet de protéger l’homme, et son usage a été rendu obligatoire dans certains pays comme l’Autriche et pourrait le devenir en Suisse.Plus rarement
Outre ces deux maladies, l’anaplasmose granulocytaire humaine, encore très peu décrite en France et due à Anaplasma phagocytophilum, implique aussi I. ricinus comme vecteur, sans transmission transovarienne. Le ou les réservoirs animaux n’ont pas encore été identifiés à ce jour.La fièvre Q et la tularémie sont également transmissibles par piqûre de tique, essentiellement I. ricinus, mais c’est une modalité de transmission qui reste rare (v. infra).
Zoonoses associées à l’inhalation d’aérosols infectieux
Respirer l’air supposé pur des lieux de promenade ou s’adonner à des activités de plein air n’est pas non plus dénué de tout risque. Deux maladies en particulier peuvent être contractées par inhalation d’aérosols infectieux.
Fièvre Q
La fièvre Q est due à une petite bactérie très ubiquitaire, Coxiella burnetii, qui a pour réservoirs de nombreuses espèces animales sauvages (au sein desquelles elle circule surtout grâce à I. ricinus). L’infection est fréquente et peut se pérenniser au sein des élevages de ruminants domestiques, chez qui elle peut être inapparente ou se manifester par des atteintes génitales, l’excrétion étant particulièrement massive en cas d’avortement. Or C. burnetii est libérée sous forme de pseudospores très résistantes dans l’environnement. Ainsi les cas les plus récemment décrits en France l’ont été chez des personnes se promenant à proximité d’élevages, sans autre facteur de risque connu. L’exemple le plus emblématique est celui des Pays-Bas, principal foyer mondial jamais connu de fièvre Q animale, mais aussi humaine avec 4 108 cas déclarés entre 2007 et 2011, la plupart urbains. Les autorités sanitaires ont estimé à 40 000 le nombre total d’humains infectés. Le processus n’a pu être enrayé que grâce à des actions très énergiques pour éliminer les sources animales de contamination. La forte concentration des élevages de chèvres laitières (« méga-fermes ») infectées, la densité humaine et des étés chauds et secs, propices à la fois à la diffusion des pseudospores dans l’air et aux barbecues qui ont favorisé l’exposition, ont probablement contribué à la genèse de cet épisode exceptionnel.3Hantaviroses
En Europe occidentale, un Hantavirus, le virus Puumala, est responsable de la fièvre hémorragique avec syndrome rénal. En France, ce virus circule surtout dans le Nord-Est, au sein des populations de campagnols roussâtres. Il est excrété par leurs urines et leurs fèces et se retrouve en suspension dans l’air. Le nettoyage peu régulier des greniers des résidences forestières fréquentées par les campagnols est un facteur de risque d’infection puisqu’il est source d’émission d’aérosols infectieux, une promenade en forêt pouvant être beaucoup plus rarement une circonstance de contamination. À noter que les touristes qui se rendent dans certains parcs nationaux d’Amérique du Nord, notamment le Yosemite National Park, peuvent être contaminés par un Hantavirus beaucoup plus redoutable, le virus Sin nombre.Zoonoses associées à des activités particulières
Activités aquatiques et leptospirose
Cette zoonose, qui peut être sévère, est liée à une contamination directe ou indirecte à partir d’urines de mammifères. Les rongeurs constituent le réservoir de la plupart des sérovars pathogènes, dont le plus ubiquitaire et le plus virulent est Leptospira icterohaemorrhagiae. La contamination de plans d’eau par des urines de rongeurs infectés peut ainsi être à l’origine de cas, groupés ou pas, signalés à la suite d’une baignade dans des eaux douces et les berges boueuses ou à d'activités nautiques (kayak, planche à voile…). En France métropolitaine, la fréquence est relativement faible, mais une augmentation préoccupante de l’incidence est perceptible depuis quelques années, avec une moyenne actuelle de 600 cas par an. En outre-mer, le taux d’incidence est de 5 (La Réunion) à plus de 70 fois (Mayotte) plus élevé qu’en métropole en raison notamment de l’existence de rizières humides dans lesquelles hommes et rongeurs peuvent se croiser. À l’échelle mondiale, les changements climatiques, l’urbanisation grandissante et l’augmentation de la pratique des sports nautiques sont incriminés dans l’augmentation du nombre de cas.4Chasse et tularémie
Francisella tularensis circule à l’état naturel au sein de populations de micromammifères, avec là encore l’implication de tiques vectrices, en particulier I. ricinus. En Europe occidentale, le scénario le plus fréquent de contamination humaine incrimine un (mauvais) chasseur, qui ramasse un lièvre (espèce particulièrement sensible), tiré ou non, qui gît sur son chemin ou est ramassé sans difficulté par son chien. La bactérie traversant la peau saine, c’est surtout la personne qui prépare le lièvre en vue de sa consommation, qu’il s’agisse du chasseur ou d’un membre de sa famille, qui sera contaminée, la cuisson détruisant la bactérie. La prévention passe par l’évitement de tout contact avec un lièvre d’apparence malade et par une vigilance accrue lorsque des cadavres de lièvre sont observés en nombre anormalement élevé.Visite de fermes pédagogiques et de foires agricoles et contamination par contact avec les animaux
L’urbanisation croissante est à l’origine d’un engouement pour les visites de fermes pédagogiques ou de foires rendant accessibles au public des animaux domestiques, en particulier des ruminants.5 Ils peuvent excréter par leurs fèces, le plus souvent asymptomatiquement, de nombreux germes qui peuvent souiller leur pelage et entraîner une contamination oro-fécale si les personnes qui touchent les animaux, en particulier les enfants, portent ensuite la main à la bouche sans s’être préalablement lavé les mains. Il peut en résulter des troubles digestifs liés à l’ingestion de bactéries (Salmonella, Campylobacter, Yersinia…) ou de parasites protistes*** (Cryptosporidium, Giardia…). Le danger le plus redoutable est constitué par les Escherichia coli entéro-hémorragiques (ECEH), qui produisent une toxine cytolytique (shigatoxine) capable d’entraîner une diarrhée hémorragique, voire une insuffisance rénale définitive, en particulier chez les enfants les plus jeunes.5Par ailleurs, le contact avec des bovins porteurs de lésions dues à Trichophyton verrucosum peut occasionner une teigne chez l’homme.
Colombophilie et zoonoses
Enfin, plusieurs zoonoses peuvent être théoriquement contractées à partir des pigeons, comme la maladie de Newcastle, la psittacose et la grippe aviaire zoonotique. Pour des raisons diverses, ces risques restent mineurs, mais il convient néanmoins d’attirer l’attention des colombophiles à cet égard, dans la mesure où ces animaux voyagent et rencontrent d’autres pigeons, générant des risques d’exposition non négligeables, surtout si le contexte épidémiologique est celui d’une circulation de l’un ou l’autre de ces agents dans l’avifaune.MIEUX INFORMER LE PUBLIC
L’essor des activités de loisirs, notamment de plein air, expose de façon accrue à des maladies zoonotiques diverses (v. tableau). Les piqûres de tiques peuvent transmettre divers agents zoonotiques, dont le plus répandu est l’agent de la maladie de Lyme. L’élimination de ces agents une fois présents sur un territoire est impossible, car ils circulent dans des écosystèmes complexes impliquant à la fois de nombreux hôtes vertébrés et invertébrés (les tiques). Cela est d’autant plus préoccupant qu’une augmentation de l’incidence des maladies à tiques, voire des émergences de maladies encore inconnues dans le pays sont à craindre, comme l’illustre l’apparition récente en Espagne de cas autochtones de fièvre de Crimée-Congo. De même, des agents transmis selon d’autres modalités sont très ubiquitaires, comme les leptospires et divers agents présents dans les fèces d’animaux sauvages et domestiques, rendant non réaliste la perspective de leur élimination. La lutte passe par une meilleure connaissance de l’épidémiologie de ces infections, un diagnostic le plus précoce possible, des méthodes appropriées de prévention (v. tableau) et de surveillance, la recherche de moyens de lutte innovants, mais aussi par la bonne information des publics concernés en vue de leur participation active à la mise en œuvre de mesures préventives mais aussi à la collecte de données sur le terrain.
* On désigne ainsi classiquement les petits mammifères et notamment les rongeurs.** D’après les statistiques de Santé publique France (anciennement Institut de veille sanitaire), en l’occurrence sur les données 2009-2014, qui ont été proches de 27 000 cas déclarés par an et ce, de façon assez stable durant cette période. Les chiffres communiqués en 2016 par la même structure correspondent au double, soit environ 54 000 cas. *** Nom actuel des protozoaires (= parasites monocellulaires)