Introduction
En France, la maladie rénale chronique (MRC) touche 10 % de la population globale et 28 % des plus de 65 ans.1 Il existe un lien très étroit entre la MRC et la mortalité cardiovasculaire.2 Le suivi prospectif de grandes cohortes de patients montre que l’avenir des patients porteurs de MRC est non seulement marqué par la progression de leur maladie rénale vers le stade terminal, nécessitant une prise en charge en dialyse ou une greffe rénale, mais aussi par une mortalité élevée, principalement de cause cardiovasculaire.2,3 Il est maintenant bien établi que le risque de mortalité cardiovasculaire augmente dès les premiers stades de la maladie rénale et devient exponentiel à partir du stade 3.
La prise en charge de la MRC au stade de la suppléance (dialyse ou transplantation) est un traitement onéreux. En France près de 90 000 patients bénéficient d’un traitement de suppléance dont le coût global annuel est estimé à 4 milliards d’euros. Les prédictions épidémiologiques pour les années à venir annoncent un doublement de la population nécessitant une prise en charge par traitement de suppléance des suites d’une MRC arrivée au stade terminal.4
Ainsi, l’impact considérable de la MRC sur la mortalité toutes causes, sur la morbidité cardiovasculaire et sur l’économie de la santé en fait un véritable enjeu de santé publique.
Des stratégies doivent être mises en place pour réduire le nombre de patients arrivant chaque année au stade terminal de la MRC.
Le dépistage : une étape essentielle dans la prévention de la MRC
Selon l’Organisation mondiale de la santé, la prévention regroupe l’ensemble des mesures visant à éviter ou à réduire le nombre et la gravité des maladies et accidents. Les mesures de prévention peuvent être répertoriées en trois catégories : primaire, secondaire et tertiaire.
Dans le cas de la MRC, la prévention primaire viserait à diminuer l’incidence de la MRC en supprimant les facteurs de risque modifiables de la maladie : diabète, hypertension artérielle, tabac… Il s’agit d’une stratégie efficace mais dont le coût économique est élevé et les résultats obtenus sur le long terme. Cet axe de prévention nécessite une approche globale, nationale, mais elle implique peu le médecin traitant.
Le rôle du médecin traitant s’inscrit plutôt dans la prévention secondaire et tertiaire.
La prévention secondaire consiste à diminuer la prévalence de la maladie par l’identification et le traitement des cas précoces. C’est donc par des actions de dépistage en population générale ou en population à risque que cet objectif sera atteint. Dans le cadre de la MRC, le dépistage ciblé dans les populations à risque est économiquement soutenable et très efficace.
La prévention tertiaire consiste à limiter les incapacités chroniques dues à la maladie en les corrigeant. Dans cette ultime étape, le médecin traitant a un rôle central à jouer dans la mise en place et dans le suivi des mesures de néphroprotection, qui visent à ralentir la progression de la maladie.
Le dépistage, pour qui et comment ?
Le dépistage de la MRC fait partie intégrante des missions du médecin généraliste selon la Haute Autorité de santé (HAS). Les recommandations de la HAS sont d’effectuer un dépistage annuel de la MRC chez tous les patients à risque, c’est-à-dire ceux porteurs de diabète, d’hypertension artérielle, de maladie cardiovasculaire athéromateuse, d’insuffisance cardiaque, d’obésité, de maladie de système, etc. (HAS, 2021).
Le dépistage doit être fait au moyen d’un dosage de créatinine couplé à une estimation du débit de filtration glomérulaire (DFG) selon la formule de la Chronic Kidney Disease-Epidemiology Collaboration (CKD-EPI) et à une mesure du rapport albumine/créatinine (RAC).
Ces éléments (créatininémie + DFG et RAC) sont indispensables pour la recherche d’une MRC. En effet, une MRC est définie :
- soit par l’existence d’une insuffisance rénale chronique avec baisse du DFG (< 60 mL/min) depuis au moins trois mois ;
- soit par l’existence d’une albuminurie supérieure au ratio considéré comme normal (> 30 mg/g ou 3 mg/mmol) ;
- soit par l’association des deux anomalies précitées.
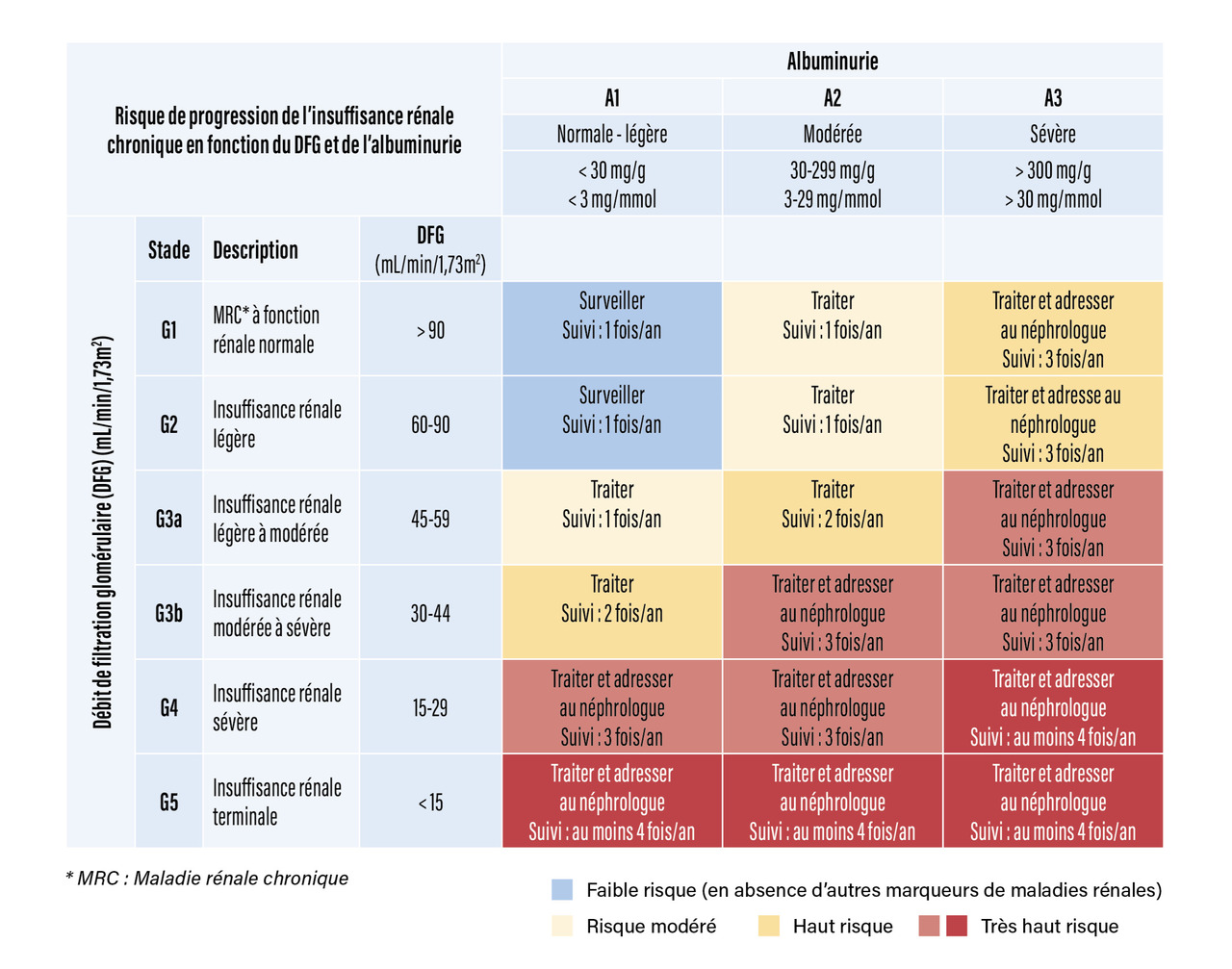
Après obtention des résultats, la nécessité de l’adressage au médecin spécialiste dépend du risque de progression de la MRC. L’évaluation du risque de progression tient compte du DFG et de la protéinurie. La « heat map » (fig. 1) et le calcul du score de risque rénal (KFRE) [fig. 2] sont deux outils qui permettent une évaluation facile et rapide du risque de progression.
L’efficacité de ces outils de dépistage sur la prise en charge de la MRC est maintenant bien établie. Ainsi, une étude canadienne a permis d’établir une augmentation du taux d’adressage au néphrologue depuis la mise en place du rendu systématique de la clairance selon le CKD-EPI, suggérant que cet outil permet un meilleur dépistage de la MRC.5 De même, dans le Limousin, une étude rétrospective en 2019 a permis d’observer que dans 90 % des cas l’adressage des patients au néphrologue était réalisé au stade 3 de la MRC, totalement en accord avec les recommandations.15
Prise en charge de la MRC une fois diagnostiquée : place du médecin généraliste
Une fois la MRC diagnostiquée, l’avis néphrologique doit être parfois demandé en urgence par consultation ou par télé-expertise. Ces situations sont :
- s’il existe une urgence à établir un diagnostic précis de la maladie rénale ;
- s’il y a un déclin rapide du DFG (> 5 mL/min/an) ;
- s’il y a une hypertension artérielle non contrôlée ;
- ou s’il existe une protéinurie > 500 mg/g (50 mg/mmol).
Pour tous les autres cas, le rôle du médecin généraliste est d’instaurer précocement des mesures de néphroprotection dans le but de ralentir la progression de la maladie rénale ; son rôle est également de prévenir l’iatrogénie.
Néphroprotection par le biais de la réduction de l’hyperfiltration glomérulaire
Le mécanisme physiopathologique commun à toutes les MRC indépendamment de la cause est l’installation progressive d’une hyperfiltration glomérulaire compensatrice. Cette hyperfiltration participe à la protéinurie et est également responsable de l’activation locale de mécanismes pro-inflammatoires et profibrotiques. Certaines mesures néphroprotectrices doivent leur efficacité à la réduction de l’hyperfiltration : il s’agit des mesures diététiques, telles que la limitation de l’apport sodé (< 85 mmol/24 h, soit 5 g/24 h) et la limitation des apports de protéines.6 La restriction des apports de protéines à 0,6 - 0,8 g/kg de poids par jour chez les diabétiques et 0,4 - 0,6 g/kg/j chez les non-diabétiques contribue significativement à retarder l’échéance des traitements de suppléance rénale. Une restriction plus drastique des apports de protéines est possible sous couvert d’une surveillance nutritionnelle et d’une supplémentation en céto-analogues.7
Équilibre tensionnel
De façon similaire, la normalisation de la pression artérielle systémique permet une baisse de la pression intraglomérulaire. L’activation inappropriée du système rénine-angiotensine-aldostérone (SRAA) au cours des MRC est aussi un élément physiopathologique qui contribue à l’hyperfiltration et à la fibrose rénale. L’utilisation des classes thérapeutiques antagonistes du SRAA sont donc à privilégier afin de normaliser la pression artérielle, réduire la pression intraglomérulaire et ralentir la progression de la maladie rénale. L’objectif tensionnel en cas de MRC est de maintenir une pression artérielle (PA) < 130/80 mmHg, par le biais de l’utilisation en première intention d’une molécule de la classe des inhibiteurs de l’enzyme de conversion (IEC) ou des antagonistes des récepteurs de l’angiotensine 2 (ARA2) [KDIGO 2024 et HAS 2021].6
Néphroprotection par le biais de la correction des complications métaboliques de la MRC
Le dépistage des complications de la MRC est préconisé au stade 3 de la MRC :
- anémie : la présence d’une anémie au cours de la MRC est associée à une progression plus rapide de la maladie, une augmentation des événements cardiovasculaires et un amoindrissement de la qualité de vie. L’avis du néphrologue est utile pour initier le traitement par un agent stimulant l’érythropoïèse associé ou non à une supplémentation martiale ;8
- acidose métabolique : la présence d’une acidose est associée à un déclin plus rapide du DFG, à une fonte musculaire plus importante et à une déminéralisation osseuse prononcée. La supplémentation par gélules de bicarbonate de sodium doit permettre de maintenir une bicarbonatémie à 23 mmol/L ;9
- vitamine D : la carence en 25 -OH vitamine D est fréquente à tous les stades de la MRC et est associée à une évolution plus rapide de la maladie rénale et une mortalité plus élevée. La supplémentation pour obtenir une concentration supérieure à 30 ng/mL permet de limiter l’hyperparathyroïdie.10,11
Prévention des épisodes d’insuffisance rénale aiguë et de la toxicité médicamenteuse
Une fois le diagnostic de MRC posé, il est important de limiter les épisodes d’insuffisance rénale aiguë qui peuvent contribuer à l’aggravation de la MRC. Pour atteindre ce but, une première étape consiste à passer en revue tous les traitements du patient afin de remplacer les médicaments contre-indiqués et également d’adapter la posologie des médicaments au DFG du patient.
Il est essentiel de limiter les examens radiologiques nécessitant une injection de produit de contraste iodé. Si l’examen reste indispensable, il faudra veiller à une bonne hydratation du patient et à l’interruption transitoire de 24 à 48 heures des médicaments dit « néphrotoxiques » tels que la metformine, les diurétiques, les IEC et ARA2.6,12,13
La mise à jour des vaccinations, notamment antipneumococcique, permettra d’éviter la survenue d’épisode infectieux dont la gravité est plus prononcée au sein de la population porteuse de MRC.
Néphroprotection médicamenteuse : place des inhibiteurs du cotransporteur sodium-glucose
Ces dernières années, plusieurs essais thérapeutiques ont prouvé l’efficacité des inhibiteurs du cotransporteur sodium-glucose (iSGLT2) dans la réduction de la progression de la MRC toutes causes confondues.14,15 Les recommandations KDIGO 2024 mettent en avant la nécessité d’instaurer, dès les stades précoces de la maladie, un traitement par iSGLT2 en association avec les IEC/ARA2.6 La néphroprotection médicamenteuse sera abordée dans le chapitre suivant.
Conclusion
La MRC est une affection en constante progression. Son impact sur l’altération de la fonction rénale, les complications cardiovasculaires et la qualité de vie nécessite une prise en charge pluridisciplinaire. Le rôle du médecin généraliste est central pour le dépistage de la MRC. Après le diagnostic, un faible nombre de ces patients devront être adressés en urgence au néphrologue pour investigations et prise en charge. Mais dans tous les cas, la mise en place rapide par le médecin généraliste de mesures de néphroprotection permettra une stabilisation efficace de la maladie avant adressage au spécialiste.
Cet article fait partie d'un supplément ayant bénéficié du soutien strictement institutionnel du laboratoire AstraZeneca , sans intervention de leur part dans l’élaboration du sommaire, le choix des auteurs et la rédaction des articles.
2. Go AS, Chertow GM, Fan D, McCulloch CE, Hsu C. Chronic kidney disease and the risks of death, cardiovascular events, and hospitalization 2004; N Engl J Med 351:1296-305.
3. Keith DS, Nichols G, Gullion CM, Brown JB, Smith DH. Longitudinal follow-up and outcomes among a population with chronic kidney disease in a large managed care organization. Arch Intern Med 2004;164:659-63.
4. Liyanage T, Ninomiya T, Jha V, Neal B, Patrice HM, Okpechi I, et al. Worldwide access to treatment for end-stage kidney disease: a systematic review. Lancet Lond Engl 2015; 385:1975-82.
5. Akbari A, Grimshaw J, Stacey D, Hogg W, Ramsay T, Cheng-Fitzpatrick M, et al. Change in appropriate referrals to nephrologists after the introduction of automatic reporting of the estimated glomerular filtration rate. CMAJ 2012;184,E269-276.
6. KDIGO 2024 Clinical Practice Guideline for the evaluation and management of chronic kidney disease 2024; Kidney Int 2024;105:S117-S314.
7. Ikizler TA, Burrowes JD, Byham-Gray LD, Campbelle KL, Carrero JJ, Chan W et al. KDOQI Clinical Practice Guideline for Nutrition in CKD: 2020 Update. Am J Kidney Dis 2020;76:S1-S107.
8. Lankhorst CE, Wish JB. Anemia in renal disease: diagnosis and management. Blood Rev 2010; 24:39-47.
9. Raphael KL. Metabolic acidosis and subclinical metabolic acidosis in CKD. J Am Soc Nephrol 2018; 29: 376-82 (2018).
10. Duranton F, Rodriguez-Ortiz ME, Duny Y, Rodriguez M, Daurès JP, Argilès A et al. Vitamin D treatment and mortality in chronic kidney disease: a systematic review and meta-analysis. Am J Nephrol 2013;37:239-48.
11. Dusso AS. Kidney disease and vitamin D levels: 25-hydroxyvitamin D, 1,25-dihydroxyvitamin D, and VDR activation. Kidney Int Suppl 2011;1:136-4.
12. Vasman D. Prevention of iatrogenic risk and screening of chronic kidney disease. Nephrol Ther 2019;15(6):465-7.
13. Mongaret C, Aubert L, Lestrille A, Albault V, Kreit P, Herlem E, et al. The role of community pharmacists in the detection of clinically relevant drug-related problems in chronic kidney disease patients. Pharm Basel Switz 2020;8(2):89.
14. The EMPA-KIDNEY Collaborative Group; Herrington WG, Staplin N, Wanner C, Green JB, Hauske SJ et al. Empagliflozin in patients with chronic kidney disease. N Engl J Med 2023;388:117-27.
15. Heerspink HJL, Stefánsson BV, Correa-Rotter R, Chertow GM, Greene T, Hou FF, et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020;383:1436-46.
16. Bousquet JF. Thèse de médecine, université de Limoges. Les primoconsultations néphrologiques des patients adressés par leur médecin traitant au CHU de Limoges : besoins des médecins généralistes et apport des néphrologues, 2020.
En collaboration avec :