Les premiers cas de transplantation fécale décrits remontent au IVe siècle après J.-C. et concernaient des soldats chinois ayant des symptômes digestifs sur les champs de bataille, alors améliorés par la prise empirique d’échantillons de selles de collègues bien portants. Il faut ensuite attendre 1958 pour voir les premiers cas décrits dans la littérature médicale et initialement effectués pour des diarrhées post-infectieuses, puis, en 1983, le premier cas effectué pour une colite à Clostridioides difficile avérée. C’est la publication en 2013, par une équipe hollandaise, de la première étude randomisée contrôlée comparant l’utilisation de la transplantation fécale à un traitement par vancomycine, avec ou sans préparation colique, qui confirme l’efficacité de ce traitement dans les cas de colites à C. difficile récidivantes et met en lumière ce traitement.1
Quelles indications dans le soin courant ?
La seule indication de transplantation fécale validée dans le soin courant par les sociétés savantes européennes2 et nord-américaines concerne les colites à C. difficile récidivantes, à savoir au moins trois épisodes de colites confirmées par la présence de toxines dans les selles et avec un intervalle de moins de 8 semaines entre les épisodes, malgré un traitement bien conduit par fidaxomicine et/ou vancomycine.
Quels résultats ?
Une dizaine d’études randomisées contrôlées publiées depuis 2013 ont confirmé l’efficacité de ce traitement dans les colites à C. difficile récidivantes avec des taux de guérison sans rechute de l’ordre de 80 à 94 % sans différence notable entre les voies d’abord, haute ou basse, les volumes administrés (de 50 à 500 mL), l’utilisation de selles congelées ou non, le type de donneur, unique ou multiple.3 Par ailleurs, il n’y a, à l’heure actuelle, pas de données permettant de dire qu’un donneur serait supérieur à un autre (concept de « superdonneur ») dans les cas de colites à C. difficile récidivantes.
Quels sont les risques ?
Les données concernant le suivi après la transplantation fécale disponibles dans la littérature scientifique vont de quelques mois à 5 ans. La majeure partie des effets indésirables immédiats sont généralement une modification transitoire du transit, des ballonnements, spontanément résolutifs en quelques jours. Les effets indésirables graves sont rares, ils sont reliés au mode d’administration (inhalation en cas de voie haute, perforation clinique en cas de coloscopie) plus qu’à l’administration du microbiote fécal lui-même. Les effets indésirables à long terme décrits sont pour l’instant nuls.4 Néanmoins des registres de suivi sont en cours afin de recueillir plus d’information sur les suivis post- transplantation fécale. Enfin, les données de transplantation fécale réalisées chez des patients immunodéprimés ou ayant des comorbidités sont rassurantes et ne semblent pas montrer de sur-risque notamment infectieux lorsque les règles de bonnes pratiques sont respectées.*
Aspect logistique de la transplantation fécale en France
La transplantation fécale est considérée, en France, comme un médicament, ce qui implique par conséquent la responsabilité de la pharmacie hospitalière. Du fait de son caractère atypique, de la multiplicité des intervenants et de la logistique nécessaire à son bon déroulement, la mise en place de structures effectuant la transplantation fécale peut s’avérer complexe.
Concernant le donneur potentiel, le bilan de screening à effectuer dans le soin courant a été défini en concertation pluridisciplinaire par le Groupe français de transplantation fécale (GFTF) et a pour but de limiter la transmission d’agents pathogènes ou le risque de transmission de facteurs favorisant les pathologies digestives, auto-immunes, cancéreuses, dysmétaboliques. Par ailleurs, il est recommandé d’avoir recours à des donneurs ne prenant aucun traitement qui pourrait influencer le microbiote. Ces contre-indications aux dons restreignent le nombre de donneurs potentiels. La selle doit être acheminée dans les 6 heures après l’émission et homogénéisée avec du sérum physiologique puis filtrée de manière à retirer les résidus. L’ajout de glycérol 10 % permet une congélation de la préparation avec une péremption actuellement estimée à 1 an, facilitant la disponibilité de lots de transplantation fécale.
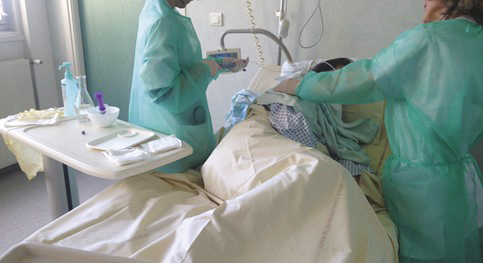
Pour le patient receveur, il est recommandé de poursuivre l’antibiothérapie curative jusqu’à 72 heures avant la transplantation fécale et de faire une préparation colique préalable afin de favoriser la clairance de C. difficile et de libérer l’espace nécessaire à l’implantation du microbiote transplanté.5 Le mode d’administration de la transplantation fécale dépend des habitudes des centres (fig. 1 et 2).
Concernant le donneur potentiel, le bilan de screening à effectuer dans le soin courant a été défini en concertation pluridisciplinaire par le Groupe français de transplantation fécale (GFTF) et a pour but de limiter la transmission d’agents pathogènes ou le risque de transmission de facteurs favorisant les pathologies digestives, auto-immunes, cancéreuses, dysmétaboliques. Par ailleurs, il est recommandé d’avoir recours à des donneurs ne prenant aucun traitement qui pourrait influencer le microbiote. Ces contre-indications aux dons restreignent le nombre de donneurs potentiels. La selle doit être acheminée dans les 6 heures après l’émission et homogénéisée avec du sérum physiologique puis filtrée de manière à retirer les résidus. L’ajout de glycérol 10 % permet une congélation de la préparation avec une péremption actuellement estimée à 1 an, facilitant la disponibilité de lots de transplantation fécale.
Pour le patient receveur, il est recommandé de poursuivre l’antibiothérapie curative jusqu’à 72 heures avant la transplantation fécale et de faire une préparation colique préalable afin de favoriser la clairance de C. difficile et de libérer l’espace nécessaire à l’implantation du microbiote transplanté.5 Le mode d’administration de la transplantation fécale dépend des habitudes des centres (fig. 1 et 2).
Une centaine d’essais cliniques
La transplantation fécale pourrait faire partie à l’avenir de l’arsenal thérapeutique dans de nombreuses patho- logies chroniques concernées par une dysbiose. Les études les plus robustes actuellement sont celles effectuées dans le domaine des maladies inflammatoires chroniques intestinales et principalement la rectocolite hémorragique avec quatre essais randomisés contrôlés évaluant la transplantation fécale dans le traitement d’une poussée. Elles mettent en évidence des taux de rémission de l’ordre de 30 % mais avec une grande hétérogénéité en termes de mode et de nombre d’administration.6 Une centaine d’essais cliniques sont en cours ou à venir dans des pathologies diverses notamment l’autisme, la réaction du greffon contre l’hôte, l’éradication de bactéries hautement résistantes. Pour autant, les données préliminaires ne semblent pas être aussi spectaculaires que les résultats obtenus dans les colites à C. difficile récidivantes, ce qui doit conduire à la prudence et à renforcer les données de la recherche avant une diffusion potentielle en pratique clinique dans d’autres indications.
UNE SEULE INDICATION VALIDÉE
Les colites à Clostridioides difficile récidivantes sont la seule indication de transplantation fécale actuellement validée dans le soin courant. La transplantation fécale nécessite une organisation et un réseau d’intervenants parfois complexe, ce qui peut limiter son application en pratique ; néanmoins la congélation permet de réduire les contraintes. Enfin, la transplantation fécale reste à l’heure actuelle en cours d’évaluation dans d’autres pathologies impliquant une dysbiose.
*Communiqué de presse du GFTF http://bit.ly/2S2qd1zRemerciements à Agnès Bellanger et Nathalie Kapel, pharmaciennes à l'hôpital de la Pitié-Salpêtrière à Paris pour le prêt de la photo ci-contre (fig. 2).
Références
1. Van Nood E, Vrieze A, Nieuwdorp M, et al. Duodenal infusion of donor feces for recurrent Clostridium difficile. N Engl J Med 2013;368:407 15.
2. Cammarota G, Ianiro G, Tilg H, et al. European consensus conference on faecal microbiota transplantation in clinical practice. Gut 2017;66:569 80.
3. Quraishi MN, Widlak M, Bhala N, et al. Systematic review with meta-analysis: the efficacy of faecal microbiota transplantation for the treatment of recurrent and refractory Clostridium difficile infection. Aliment Pharmacol Ther 2017;46:479 93.
4. Wang S, Xu M, Wang W, et al. Systematic review: adverse events of fecal microbiota transplantation. PLoS ONE 2016;11:e0161174.
5. Sokol H, Galperine T, Kapel N, et al. Faecal microbiota transplantation in recurrent Clostridium difficile infection: Recommendations from the French Group of Faecal microbiota Transplantation. Dig Liver Dis 2016;48:242 7.
6. Narula N, Kassam Z, Yuan Y, et al. Systematic review and meta-analysis: fecal microbiota transplantation for treatment of active ulcerative colitis. Inflamm Bowel Dis 2017;23:1702 9.
2. Cammarota G, Ianiro G, Tilg H, et al. European consensus conference on faecal microbiota transplantation in clinical practice. Gut 2017;66:569 80.
3. Quraishi MN, Widlak M, Bhala N, et al. Systematic review with meta-analysis: the efficacy of faecal microbiota transplantation for the treatment of recurrent and refractory Clostridium difficile infection. Aliment Pharmacol Ther 2017;46:479 93.
4. Wang S, Xu M, Wang W, et al. Systematic review: adverse events of fecal microbiota transplantation. PLoS ONE 2016;11:e0161174.
5. Sokol H, Galperine T, Kapel N, et al. Faecal microbiota transplantation in recurrent Clostridium difficile infection: Recommendations from the French Group of Faecal microbiota Transplantation. Dig Liver Dis 2016;48:242 7.
6. Narula N, Kassam Z, Yuan Y, et al. Systematic review and meta-analysis: fecal microbiota transplantation for treatment of active ulcerative colitis. Inflamm Bowel Dis 2017;23:1702 9.