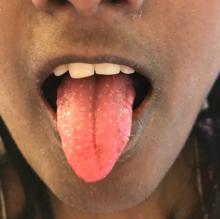Le 5 décembre 2021, vous recevez en consultation Mme M., 60 ans, adressée par son médecin généraliste pour fièvre. Elle exerce comme technicienne de laboratoire, ne fume pas, ne prend pas d’alcool. Son dernier voyage était en Birmanie en 2015. Elle vit avec son mari. Elle a une fille de 35 ans et une petite-fille de 19 mois qu’elle garde une fois par semaine lorsqu’elle n’est pas à la crèche. Elle a un chat à domicile et est une grande adepte des promenades en forêt.
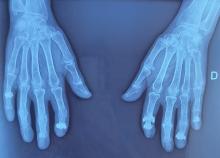
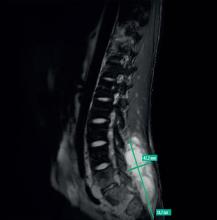
Elle a eu au cours de l’été 2021 divers problèmes rhumatologiques mécaniques avec notamment une lombosciatique L5 gauche infiltrée à plusieurs reprises, avec protrusion discale L4-L5, responsable d’un conflit disco-radiculaire concordant avec la clinique. Elle a également eu une lésion méniscale après avoir fait du trampoline à outrance avec son neveu. Elle ne prend actuellement aucun traitement.
Elle a depuis 10 jours une fièvre vespérale aux alentours de 39 °C avec altération de l’état général et grande asthénie. Elle n'a aucun signe fonctionnel respiratoire digestif ou urinaire, pas de céphalées. Absence de douleur.
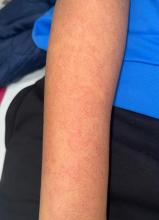
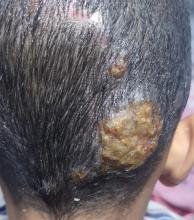
L’examen clinique est assez pauvre, en dehors de quelques ganglions sous-mentonniers infracentimétriques indolores et mobiles et d’un rash cutané roséoliforme du dos. Absence d’hépatosplénomégalie.
Son médecin généraliste vous l’adresse suite aux résultats de son bilan sanguin effectué en ville l’avant-veille : hémoglobine = 12,7 g/dL ; volume globulaire moyen (VGM) = 89 fL ; leucocytes = 13 G/L ; polynucléaires neutrophiles = 4,2 G/L ; polynucléaires éosinophiles 0,2 G/L ; polynucléaires basophiles = 0 G/L ; lymphocytes = 8 G/L ; plaquettes = 275 G/L ; frottis sanguin non vu ; ferritine = 1 213 µg/L ; aspartame aminotransférase (ASAT) = 111 UI/L ; alanine aminotransférase (ALAT) = 201 UI/L ; gamma glutamyl transférase (GGT) = 523 UI/L, bilirubine totale = 7,2 µmol/L ; phosphatases alcalines (PAL) = 415 UI/L ; protéine C réactive (CRP) = 32 mg/L ; taux de prothrombine (TP) = 93 %, temps de céphaline activée (TCA) ratio patient/témoin = 1 ; fibrinogène = 5,1 g/L ; facteurs antinucléaires = 1/160 sans spécificité ; anticorps anti-cytoplasme des polynucléaires neutrophiles (ANCA) positifs mais sans spécificité ni anti-protéinase 3 (anti-PR3) ni anti-myéloperoxydase (anti-MPO).
Elle a eu au cours de l’été 2021 divers problèmes rhumatologiques mécaniques avec notamment une lombosciatique L5 gauche infiltrée à plusieurs reprises, avec protrusion discale L4-L5, responsable d’un conflit disco-radiculaire concordant avec la clinique. Elle a également eu une lésion méniscale après avoir fait du trampoline à outrance avec son neveu. Elle ne prend actuellement aucun traitement.
Elle a depuis 10 jours une fièvre vespérale aux alentours de 39 °C avec altération de l’état général et grande asthénie. Elle n'a aucun signe fonctionnel respiratoire digestif ou urinaire, pas de céphalées. Absence de douleur.
L’examen clinique est assez pauvre, en dehors de quelques ganglions sous-mentonniers infracentimétriques indolores et mobiles et d’un rash cutané roséoliforme du dos. Absence d’hépatosplénomégalie.
Son médecin généraliste vous l’adresse suite aux résultats de son bilan sanguin effectué en ville l’avant-veille : hémoglobine = 12,7 g/dL ; volume globulaire moyen (VGM) = 89 fL ; leucocytes = 13 G/L ; polynucléaires neutrophiles = 4,2 G/L ; polynucléaires éosinophiles 0,2 G/L ; polynucléaires basophiles = 0 G/L ; lymphocytes = 8 G/L ; plaquettes = 275 G/L ; frottis sanguin non vu ; ferritine = 1 213 µg/L ; aspartame aminotransférase (ASAT) = 111 UI/L ; alanine aminotransférase (ALAT) = 201 UI/L ; gamma glutamyl transférase (GGT) = 523 UI/L, bilirubine totale = 7,2 µmol/L ; phosphatases alcalines (PAL) = 415 UI/L ; protéine C réactive (CRP) = 32 mg/L ; taux de prothrombine (TP) = 93 %, temps de céphaline activée (TCA) ratio patient/témoin = 1 ; fibrinogène = 5,1 g/L ; facteurs antinucléaires = 1/160 sans spécificité ; anticorps anti-cytoplasme des polynucléaires neutrophiles (ANCA) positifs mais sans spécificité ni anti-protéinase 3 (anti-PR3) ni anti-myéloperoxydase (anti-MPO).
Question 1 - Comment interprétez-vous ces résultats biologiques ? Une ou plusieurs réponse(s) possible(s).
De nombreuses pathologies peuvent s’accompagner d’une positivité des ANCA sans spécificité, notamment l’endocardite, les infections virales ou bactériennes chroniques, les cancers solides, les lymphomes. Les ANCA des vascularites sont le plus souvent de spécificité anti-PR3 ou anti-MPO et s’accompagnent de manifestations cliniques évocatrices.
Le diagnostic de syndrome d’activation macrophagique repose sur un faisceau d’arguments cliniques et biologiques. Les manifestations biologiques les plus fréquentes sont les cytopénies, l’augmentation majeure de la ferritine (souvent au-delà de 5 000) et l’élévation des triglycérides. Les autres manifestations sont plus variables, comme la cytolyse, les troubles ioniques, les troubles de la coagulation. Il existe un score (le « H-score de Saint-Antoine ») validé chez l’adulte pour prédire la probabilité de syndrome d’activation macrophagique. Ici au vu des données dont nous disposons, le H-score est à 0, ce qui correspond à une probabilité de SAM avoisinant les 0 %.
Ici il n’y a pas de cytopénies. Une élévation de la ferritine et une hépatite ne sont pas des arguments suffisants pour poser ce diagnostic.
Ici il n’y a pas de cytopénies. Une élévation de la ferritine et une hépatite ne sont pas des arguments suffisants pour poser ce diagnostic.
La présence d’anticorps antinucléaires est aspécifique en l’absence de contexte clinique évocateur de maladie de système. Ils peuvent se rencontrer en population générale en dehors de tout contexte pathologique et se positiver transitoirement à la faveur d’une infection.
Il y a une lymphocytose sur la formule mais rien ne vous permet d’affirmer qu’il s’agit de blastes ou au contraire de lymphocytes matures. Par argument de fréquence, il est plus probable qu’il s’agisse de lymphocytes matures.
L’ensemble du tableau (caractère aigu, fièvre altération de l’état général) est plutôt évocateur d’un syndrome mononucléosique avec expansion polyclonale de lymphocytes T activés. Le frottis vous permettra de vous orienter vers l’un ou l’autre de ces diagnostics.